-
من در مورد سوال اول جوابم به این شکله که اونی که میگه گرماگیر یعنی ما بعدش کاهش دمای محلول رو داریم و اونی که میگه گرماده هست یعنی ما افزایش دمای محلول رو داریم. در مورد سوال دوم جوابم اینه که مربوط میشه انتروپی قضیه. با حل شدنشون تو همدیگه فکر کنم ازادی عملشون نسبت به قبل بیشتر بشه ولی ایده دقیق ندارم برای این موضوع
و سوال دیگه که همین الان به ذهنم رسید اینه
 : دمای محلول مثلا در مورد گرماگیر گفتم کاهش پیدا میکنه. در مورد "گرمای محلول " چی میشه گفت؟
: دمای محلول مثلا در مورد گرماگیر گفتم کاهش پیدا میکنه. در مورد "گرمای محلول " چی میشه گفت؟
این همین طوری به ذهنم رسید. داشتم در مورد کاوشگر پارکر مطلبی رو میخوندم یاد این بحث افتادم که دما با گرما تفاوت داره.ممنون
-
dan-l اینایی که خودت گفتی درستن بنظرم...
ودرمورد گرمای محلول هم :خب طبیعتا گرمای هرچیزی با بالارفتن دماش بالا میره و با کاهش دما پایین میاد...
ولی در مورد دو جسم مجزا نمیشه صرفا با داشتن دمای اون دوجسم درمورد گرمای اونا اظهار نظر کرد چون باید تعداد ذره های اون دوجسم رو هم داشته باشیم تا بتونیم درمورد گرماشون صحبت کنیم -
@mohammad-666 در سوال محلول ها گفته است:
dan-l اینایی که خودت گفتی درستن بنظرم...
ودرمورد گرمای محلول هم :خب طبیعتا گرمای هرچیزی با بالارفتن دماش بالا میره و با کاهش دما پایین میاد...
ولی در مورد دو جسم مجزا نمیشه صرفا با داشتن دمای اون دوجسم درمورد گرمای اونا اظهار نظر کرد چون باید تعداد ذره های اون دوجسم رو هم داشته باشیم تا بتونیم درمورد گرماشون صحبت کنیمدر مورد دما و گرما این مورد هست که وابستگی زیادی به هم ندارن. بگذریم خارج بحثه.
در مورد سوال دوم من دقیقا متوجه نشدم چطور انتروپی باعث میشه فرایند انحلال خود به خودی بشه؟ -
dan-l درمورد دما و گرما اینکه زیاد وابستگی بهم ندارن درسته ولی در مورد اجسام مجزا.نه اینکه مثلا یه لیوان اب اگه دماش بالا بره نتونیم بگیم چه به سر گرماش اومده چون حتما گرماش هم بالا میره.
در مورد انتروپی .دوعامل موثر بر خودبه خودی بودن انتروپی و انتالپی هستن اینکه تابلوه.حالا اگه انتالپی ثابت بمونه تقریبا پس تنها انتروپی میمونه که تعیین کنه فرایندخودبه خودی باشه یا نه -
@mohammad-666 در سوال محلول ها گفته است:
dan-l درمورد دما و گرما اینکه زیاد وابستگی بهم ندارن درسته ولی در مورد اجسام مجزا.نه اینکه مثلا یه لیوان اب اگه دماش بالا بره نتونیم بگیم چه به سر گرماش اومده چون حتما گرماش هم بالا میره.
در مورد انتروپی .دوعامل موثر بر خودبه خودی بودن انتروپی و انتالپی هستن اینکه تابلوه.حالا اگه انتالپی ثابت بمونه تقریبا پس تنها انتروپی میمونه که تعیین کنه فرایندخودبه خودی باشه یا نهthx
-
سلام دو تا سوال داشتم لطفا اگه میدونین جواب بدین.
سوال گفته که انحلال پذیری نیتروژن و هلیم و اکسیژن رو در اب مقایسه کنین.سوال دوم اینه که از کجا باید بدونم که مثلا انحلال اتانول در اب با افزایش بی نظمی همراهه یا مثلا انحلال پتاسیم نیترات در اب با کاهش بی نظمی همراهه؟
و یا اینکه مثلا سدیم کلرید در تولوین حل نمیشه؟ اینا تو کتاب نیستن پس باید از کجا اینارو بدونم؟ اینا سوالای ای کیو بودن ممنون -
در مورد گرماده بودن یا گرماگیر بودن انحلال مواد:
اینا گرماده ان:1.اسید ها
2.باز های قوی
3.کلسیم کلرید و لیتیم سولفات
4.الکل های سبک
5.کلیه ی گاز ها
6.فلز های فعال -اکسید و هیدرید های ان هامنبع شیمی مبتکران
جواب سوالارو پیدا کردم ممنون
-
سلام دوستان اگه ممکنه این سوال رو حل کنید ممنون میشم.(جواب من با کتاب متفاوته. ولی فکر میکنم توی محاسبات اشتباه تایپ شده برای همین پرسیدم)
اگر در دمایی مشخص,مقدار 0.02 مول کلسیم کلرید در 85 گرم محلول سیر شده ی ان حل شده باشد انحلال پذیری کلسیم کلرید در این دما را بدست اوردید
ca=40
cl=35.5
ممنون@دانش-آموزان-نظام-قدیم-آلا @همیار @mohammad-6666 MM.zahed Heroes_Hunter @
-
یعنی فقط من محلول میخونم؟

یه سوال ... این فکر کنید کتابه ولی جواب رو متوجه نمیشم ....
اگه ممکنه اینو توضیح بدید ممنون میشم:
-
dan-l سلام
مساله که یادم رفته اما این داره میگه صابون دو سر داره یه سر قطبی یه سر نا قطبی
وقتی با چربی و اب قاطیش می کنیم این مثل یه پلی بین اب و چربی عمل می کنه
جاسوس دوجانبست هم با اب دوسته هم با چربی و باعث میشه یه ترکیبی که قبلا اصلا با هم نمی ساخت الان پایدار بشه -
dan-l در سوال محلول ها گفته است:
سلام دو تا سوال داشتم لطفا اگه میدونین جواب بدین.
سوال گفته که انحلال پذیری نیتروژن و هلیم و اکسیژن رو در اب مقایسه کنین.سوال دوم اینه که از کجا باید بدونم که مثلا انحلال اتانول در اب با افزایش بی نظمی همراهه یا مثلا انحلال پتاسیم نیترات در اب با کاهش بی نظمی همراهه؟
و یا اینکه مثلا سدیم کلرید در تولوین حل نمیشه؟ اینا تو کتاب نیستن پس باید از کجا اینارو بدونم؟ اینا سوالای ای کیو بودن ممنونمیزان انحلال پذیری گاز ها با جرم و حجم رابطه مستقیم داره هر چی جرم و حجم بیشتر انحلال پذیریشم بیشتر... بنظرم تو این سوال انحلال پذیری اکسیژن بیشتر از نیتروژن و نیتروژنم بیشتر از هلیومه . (قطبی بودن و تشکیل پیوند هیدروژنی یه ترکیب تو آب هم عامل موثریه تو حل شدنش ) گازهای قطبی راحت تر حل میشن مث هیدروژن کلرید.
انحلال گاز در مایع باعث کاهش بینظمی و مایع در مایع و جامد در مایع باعث افزایش بی نظمی میشه...
سدیم کلرید یونه و تولوئن نا قطبی یون در مواد نا قطبی حل نمیشه . -
dan-l در سوال محلول ها گفته است:
سلام دوستان اگه ممکنه این سوال رو حل کنید ممنون میشم.(جواب من با کتاب متفاوته. ولی فکر میکنم توی محاسبات اشتباه تایپ شده برای همین پرسیدم)
اگر در دمایی مشخص,مقدار 0.02 مول کلسیم کلرید در 85 گرم محلول سیر شده ی ان حل شده باشد انحلال پذیری کلسیم کلرید در این دما را بدست اوردید
ca=40
cl=35.5
ممنون@دانش-آموزان-نظام-قدیم-آلا @همیار @mohammad-6666 MM.zahed Heroes_Hunter @
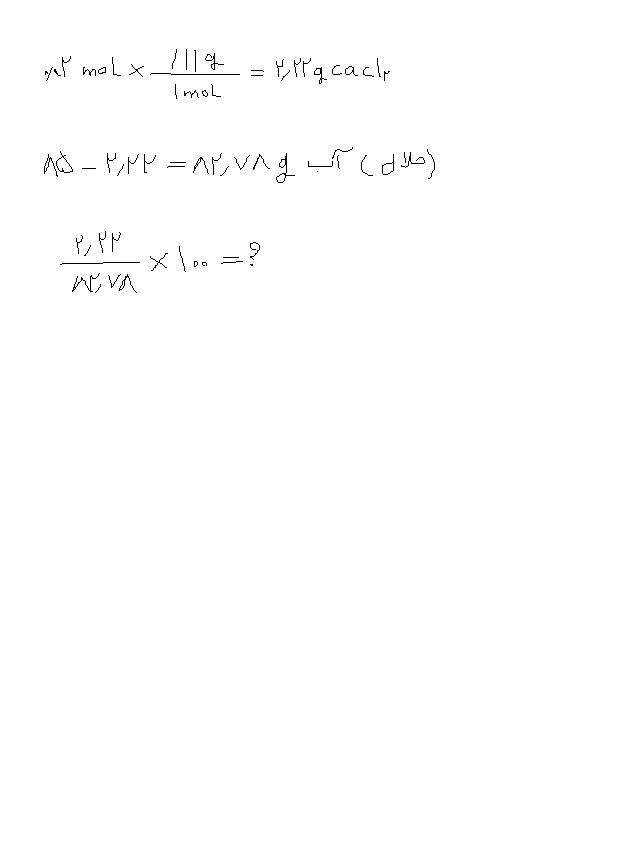
اینم من اینجوری رفتم ... درستی یا نادرستیشو نمیدونم کاش گزینه داشت
کاش گزینه داشت -
dan-l در سوال محلول ها گفته است:
سلام ... یه سوال دیگه... اگه تونستین اینو به روش کتاب درسی حل کنین من نتونستم اینو به روش کتاب درسی حل کنم

من گزینه یک بدست اوردم ... اینجوری که جرم محلول میشه 80 با استفاده از چگالی حجم محلول میشه 1/15 لیتر . مول پتاسیم نیتراتم که میشه 20/101 تقسیم کنیم میرسیم به گزینه ی 1 . روش کتاب درسی چی هست حالا؟!! من کلا با روش خودم میرم :|


