سلام سلاااام🤩
بچه ها تو این تاپیک میخوایم دانشجوها هم مثل کنکوریا ساعت مطالعه شون رو اعلام کنن ✌
هم انگیزه بشه برای فارغ التحصیلای آلاء تا تو محیط دانشگاه هم دست از تلاشِ آلائی برندارن 💪و هم اینکه کنکوریای با درسایی که دانشجوها میخونن یکم آشنا میشن🤗
پس از امشب استارت این تاپیک رو میزنیم و هرشب میایم و میگیم در طول روز چ درسایی رو خوندیم ،چند ساعت و چیکارا کردیم😁
دعوت میکنم از @فارغ-التحصیلان-آلاء که باهامون همراه بشن🤝
خیلی ممنون از z Gheibi و M.ba78 بابت پیشنهاد و همراهیشون❤
راستی از romisa جانم هم دعوت میکنم بهمون سر بزنه و همراهیمون کنه😍
سلام به بچه های عزیز آلا🌻
خب دوستان تو این تاپیک قراره که تجربه هامون رو از دانشجویی بگیم
نحوه درس خوندن، نحوه ارتباطات،خوابگاه و... هر صحبتی که تو ذهن تون هست
که ورودی های امسال مون بتونن استفاده کنن😊
ممکنه حتی یه سری نکات و صحبت ها بگیم که خودمون هم ندونیم و بهمون کمک بشه😅
و اینکه بچه های جدید حتما سوالات شون رو بپرسن
@فارغ-التحصیلان-آلاء @رتبه-های-انجمن-آلاء
@تجربیا @ریاضیا @انسانیا
@بچه-های-تجربی-کنکور-1402
@بچه-های-ریاضی-کنکور-1402
@همیار
سلام.
تا حالا فک کردین به یه سیستم عامل دیگه مهاجرت کنین؟ گاهی اوقات حس نکردین از ویندوز خسته شدین؟
خب من درمانش رو دارم بیاین لینوکس بریزیم، همه!
اصلا لینوکس چیه؟
خب اینه: "لینوکس (Linux) یک سیستم عامل رایگان و متن باز است که بر پایه هسته Linux (کرنل) توسعه داده شده است. هسته لینوکس مسئولیت مدیریت منابع سختافزاری و ارتباط بین نرمافزار و سختافزار در سیستم را بر عهده دارد."
متن بازی (open source ) یعنی چی؟ یعنی کد هاش برای همه آزاد و همه می تونن بیاین لینوکس رو تغییر بدن، (گویی انگولش کنن) اما ویندوز این شکل نیست کدهای توسعه ویندوز، رو فقط خود مایکروسافت داره. (واسه همین ویندوز گرونه 199 دلار ویندوز 11 پرو 😲 )
خلاصه اش اقا اینکه لینوکس یه هسته ی اصلی داره حالا می رسیم به توزیع های لینوکس.
اینم تاریخچه ش :در سال 1991 فردی با نام لینوس توروالدز (Linus Torvalds)، دانشجوی رشته علوم کامپیوتر در دانشگاه هلسینکی فنلاند، تصمیم گرفت یک سیستم عامل جدید بر اساس یونیکس (Unix) طراحی کند. او نیازمند یک سیستم عامل برای استفاده شخصی و توسعه برنامههای خود بود. لینوس کد منبع سیستم عامل خود را در اینترنت منتشر کرد و خواستار کمک و بازخورد از جامعه برنامهنویسی شد. این کد با عنوان “هسته لینوکس” شناخته میشد.
گروهی از برنامهنویسان از سراسر جهان به لینوس پیوستند و شروع به توسعه و بهبود هسته لینوکس کردند. این جامعه برنامهنویسی فعال با همکاری بینالمللی سایر برنامه نویسان باعث شد هسته لینوکس به سرعت رشد کند. در سال 1994، نسخه اولیه رسمی Linux با ورژن 1.0 منتشر شد. این نسخه اولیه شامل امکانات اساسی سیستم عامل شبیه به یونیکس بود و از آن پس، توسعه و بهبودهای بیشتری در هسته لینوکس صورت گرفت.
(اینجاش مهمه)
با گذر زمان، جامعه برنامهنویسی Linux رشد کرد و شرکتها و سازمانها نیز به توسعه و پیشرفت لینوکس کمک کردند. این شرکتها شامل ردهت (RedHat)، اینتل (Intel)، آیبیام (IBM) و بسیاری دیگر بودند. به مرور و با گذشت زمان، Linux به عنوان یک سیستم عامل پرکاربرد، به ویژه در سرورها و دستگاههای همراه، شناخته شد. همچنین، توزیعهای لینوکس محبوبی مانند اوبونتو (Ubuntu)، فدورا (Fedora) و دبیان (Debian) با امکانات و رابط کاربری متنوعی ارائه شدند.
از آن زمان تا به امروز، Linux به یکی از قدرتمندترین و پرطرفدارترین سیستم عاملها تبدیل شده است و در بسیاری از زمینهها از توزیع های مختلف Linux استفاده میشود، از جمله سرورها، دستگاههای هوشمند و رایانههای شخصی.
اگه به میخواین در آینده مهندسی نرم افزار، کامپیوتر، ای تی، شبکه و هزاران چیز دیگه مربوط به علوم کامپیوتر و کامپیوتر بخونین پیشنهاد می کنم همین الان لینوکس رو نصب کنید.
حالا چه توزیعی بریزیم؟
من نزدیک 1.5 ساله از ویندوز مهاجرت کردم به لینوکس و تاحالا سه تا توزیع مختلف روی ماشین مجازی ریختم و تست کردم. عملا انچنان تفاوت خاصی با هم ندارند ولی
برای شروع پیشنهاد می کنم (یعنی خیلی نوبی) : اوبونتو (ubuntu) یا linux mint یا manjaro ، این توزیع های خوبن
من در حال حاضر از manjaro استفاده می کنم که واقعا توزیع مناسبیه، ولی اگه اصلا لینوکس کار نکردین ubuntu یا linux mint بریزین.
حالا چجوری لینوکس بریزیم؟
مثلا برای نصب ubuntu میرم تو گل سرچ می کنیم download ubuntu و وبسایت رسمی ubuntu نسخه اخرین نسخه LTS اوبنتو رو بریزین ( در حال حاضر اخرین نسخه Ubuntu 24.04.1 LTS) هستش
[LTS یعنی چه مخفف long-term support یعنی ما معنی پنج سال به روز رسانی رایگان امنیتی میدیم که یعنی توزیع پایدار و با ثباتی واسه همین برای تازه کارا مناسبه]
یه فایلی به پسوند iso. دانلود میشه.
با نرم افزار refus این فایل رو روی یه فلش یا سی دی بوت می کنیم ( آموزش هاش داخل آقای گوگل هست و می تونین سی دی اوبونتو رو بخرید که بوت شده)
فلش رو وصل می کنیم، سیستم یه ریستارت می زنیم بعد قبل اینکه سیستم بالا بیاد یکی از دکه های f12 یا f10 یا del یا ... ( با توجه به نوع مادربرد، لپتاپ و ... احتمال 99 درصد f12 هستش) از منو بوت فلش رو انتخاب می کنیم و تامام وارد پنجره نصب اوبونتو میشیم که به شدت ساده هستش، داخل اینترنت میلیون ها آموزش نصب اوبنتو و بقیه توزیع ها هستش)
▶️| #معرفی_رشته
بریم برای یه معرفی رشته ی جداب
#مهندسی_پزشکی
☁️رشته ی مهندسی پزشکی چیه؟
ساخت تجهیزات پزشکی یکی از کارهایی هست که بچه های این رشته انجام میدن
این علم تلاش می کنه تا مهندسین پزشکی بتونن از ایده های پزشکی استفاده کنن
🌥کسی که این رشته رو خونده باید چه ویژگی هایی داشته باشه؟
خلاقیت و نو اوری داشته باشه
مسلط به زبان انگلیسی باشه
نرم افزار های تخصصی طراحی رو بلد باشه
قادر به تحلیل نیاز های مشتریان و بیماران باشه
ریاضی، فیزیک، زیست و شیمی اش قوی باشه
⛅️ تهش چی میشه؟
کار در شرکت های تخصصی تجهیزات پزشکی
کار در شرکت های دانش بنیان در حوزه ی مهندسی پزشکی
نمایندگی فروش و خدمات پس از فروش تجهیزات پزشکی وارداتی
طراحی و ساخت دستگاه های تشخیص مشکلات پزشکی و بیماری ها
کار و تحقیق در جنبه های فنی و مهندسی مربوط به سیستم های بیولوژیکی انسان ها و حیوانات
نصب، تنظیم و نگهداری، تعمیر یا پشتیبانی فنی تجهیزات پزشکی با عنوان متخصص تجهیزات پزشکی بیمارستانی
🌤 مسیر تحصیلی اش چیه؟
کارشناسی: مهندسی پزشکی
کارشناسی ارشد: بیوالکتریک، بیومکانیک، بیومتریال
دکتری: مهندسی بافت، رباتیک پزشکی، پردازش سیگنال ها با تصاویر پزشکی، ابزار دقیق پزشکی، مهندسی ورزش، بیوالکتریک، بیومکانیک، بیومتریال
منبع یک کاناله امیدوارم اطلاعات درست باشند. باز هم خودتون بررسی کنید
@ida-shateri
@بچه-های-کنکور-ریاضی-1400
@ریاضیا
سلام
امیدوارم حالتون خوب باشه
یلدای گذشته مبارکتون 🙂❄️🌸
یه سوال داشتم از دانشجو های آلایی
روش خاصی برای جزوه نویسی دارین ؟
اون دسته دروسی که علاوه بر فایل ، صحبتای استاد هم مهمن رو چیکار میکنین ؟
من خودم نکات اضافه ی گفته شده سر کلاس و فایل خود استاد ( در صورتی که استاد فایلشو بده 🙄 ) رو با هم تو جزوه پاک نویس میکنم ولی خب آخر ترم با حجم بالای نکات چرکنویس و فایلای نوشته نشده روبرو میشم😐💔
و از طرفی خوندن و تسلط روی مطالب نسبت به جزوه نویسی مهم تره ، مخصوصا الان که نزدیک به امتحانات ترم هستیم
ممنون میشم تجربیاتتون در این زمینه رو به اشتراک بذارین 🙏🌸
شاید یکی از نقاط عطف زندگیتون در دوران دانشجویی،فارغ از اینک چی میخونید یادگیری زبان برنامه نویسی اندروید،با توانایی ساخت اپلکیشن،میتونید هم به درآمدی برسید هم مشکلات زیادی رو که پیش میاد واستون رفع کنید...پیشنهاد من این از بیسیک فور اندروید شروع کنید(b4a),ساده ،روان ،قوی
کل چیزی که نیاز دارید؛
۱)ی سیستم ساده کامپوتری
۲)ی گوشی
۳) سه ماه وقت گذاشتن و تمرین
هر سوالی هم در این زمینه داشتید میتونید اینجا بپرسید،از مراحل نصب و ساخت تا انتشار در مارکت ها..
سلول های بنیادی راهی به آینده
-
#اخبار_جدید_سلولهای_بنیادی
 درمان ۳ نوع سرطان با سلول های بنیادی نتیجه داد
درمان ۳ نوع سرطان با سلول های بنیادی نتیجه داد محققان کشور موفق به کسب نتایج مثبت از یافتن سلولهای نهفته سرطانی و درمان ۳ نوع سرطان با سلولهای بنیادی بافت جنین شده اند.
محققان کشور موفق به کسب نتایج مثبت از یافتن سلولهای نهفته سرطانی و درمان ۳ نوع سرطان با سلولهای بنیادی بافت جنین شده اند. دکتر حسن نیک نژاد، عضو هیات علمی دانشکده پزشکی دانشگاه علوم پزشکی شهید بهشتی در خصوص آخرین مطالعات تیم تحقیقاتی خود در گروه فارماکولوژی این دانشکده به خبرنگار مهر گفت: اخیرا در حال انجام تحقیقاتی هستیم که بتوانیم به واسطه سلول های بنیادی بعد از سزارین، سرطان را درمان کنیم.
دکتر حسن نیک نژاد، عضو هیات علمی دانشکده پزشکی دانشگاه علوم پزشکی شهید بهشتی در خصوص آخرین مطالعات تیم تحقیقاتی خود در گروه فارماکولوژی این دانشکده به خبرنگار مهر گفت: اخیرا در حال انجام تحقیقاتی هستیم که بتوانیم به واسطه سلول های بنیادی بعد از سزارین، سرطان را درمان کنیم.
وی با تاکید بر اینکه اکنون درمان های جدید سرطان بر پایه سلول های بنیادی در دنیا مورد توجه قرار گرفته است، افزود: خوشبختانه ما هم در کشور به نتایج خوبی در این زمینه دست یافته ایم و دومین یا سومین کشوری هستیم که در زمینه درمان سرطان با سلول بنیادی، خیلی قوی کار کرده ایم.
وی با اشاره به روش های رایج درمان سرطان گفت: در حال حاضر برای درمان سرطان از دارو و برای اینکه سلول های سرطانی از بین بروند از روش شیمی درمانی استفاده می شود. نیک نژاد با اشاره به عوارض شیمی درمانی گفت: از بین رفتن مغز استخوان، ریزش مو، سمی شدن کلیه و... از عوارض شیمی درمانی به شمار می روند.
نیک نژاد با اشاره به عوارض شیمی درمانی گفت: از بین رفتن مغز استخوان، ریزش مو، سمی شدن کلیه و... از عوارض شیمی درمانی به شمار می روند. عضو هیات علمی دانشکده پزشکی دانشگاه علوم پزشکی شهیدبهشتی با تاکید بر اینکه به همین دلیل بر آن شدیم تا بتوانیم سلول های سرطانی را با استفاده از سلول درمانی از بین ببریم، گفت: استفاده از سلول های بنیادی «پرده جفت جنین یا پرده آمنیوتیک» آخرین دستاورد محققان در این دانشکده است که در راستای درمان سرطان به کار گرفته شده است.
عضو هیات علمی دانشکده پزشکی دانشگاه علوم پزشکی شهیدبهشتی با تاکید بر اینکه به همین دلیل بر آن شدیم تا بتوانیم سلول های سرطانی را با استفاده از سلول درمانی از بین ببریم، گفت: استفاده از سلول های بنیادی «پرده جفت جنین یا پرده آمنیوتیک» آخرین دستاورد محققان در این دانشکده است که در راستای درمان سرطان به کار گرفته شده است.
به گفته عضو هیات علمی دانشکده پزشکی دانشگاه علوم پزشکی شهید بهشتی، این نوع سلول های بنیادی بعد از عمل جراحی سزارین از جفت جنین گرفته می شود. نیک نژاد با تاکید بر اینکه استفاده از این پرده جنینی و کاربرد سلول های بنیادی آن مزایای زیادی دارد، اظهار داشت: این سلول ها قادرند باعث کاهش خونرسانی به تومور سرطانی شوند که از این طریق عملا رگ زایی در تومور سرطانی کاهش می یابد.
نیک نژاد با تاکید بر اینکه استفاده از این پرده جنینی و کاربرد سلول های بنیادی آن مزایای زیادی دارد، اظهار داشت: این سلول ها قادرند باعث کاهش خونرسانی به تومور سرطانی شوند که از این طریق عملا رگ زایی در تومور سرطانی کاهش می یابد.
وی افزود: در افرادی که سرطان دارند ممکن است سلول های سرطانی در فاز نهفته قرار گیرند که دارو بر روی آنها اثری ندارد. این موضوع باعث رشد مجدد تومور می شود. سلول های سرطانی در فاز نهفته می روند و معمولا بدن نمی تواند در این فاز این سلول ها را تشخیص دهد و بعد از دو تا پنج سال دوباره عود می کنند. اگر سلولی در فاز نهفته باشد، ما هیچ راهی برای تشخیص نداریم زیرا عملا تکثیر نمی شوند؛ مثلا در جاهایی که بتواند از سیستم ایمنی دور می ماند و تکثیر هم نمی شود ولی چند سال بعد که شیمی درمانی تمام شود دوباره رشد می کند.
عضو هیات علمی دانشکده پزشکی دانشگاه علوم پزشکی شهیدبهشتی ادامه داد: ولی به واسطه سلول های بنیادی می توان سلول های سرطانی نهفته را پیدا و در راستای درمان آنها اقدام کرد.
نیک نژاد با بیان اینکه درمان سرطان به واسطه سلول درمانی با سلول های بنیادی می تواند چندین اقدام را برای از بین بردن سرطان به کار گیرد، گفت: بر اساس آخرین یافته های ما در دانشگاه علوم پزشکی شهید بهشتی، سلول های بنیادی جنینی توانایی از بین بردن سلول های سرطانی را دارند یعنی این سلول ها موادی از خود ترشح می کنند که سلول های سرطانی را از بین می برند و از تکثیر سلول های سرطانی جلوگیری می کنند. همچنین مانع رگ زایی در سلول سرطانی می شوند. وی با تاکید بر اینکه در واقع ما با چند سلاح توسط سلول های بنیادی به جنگ با تومورسرطانی می رویم تا این سلولها بتوانند جایگزین شیمی درمانی شود، خاطر نشان کرد: استفاده از سلول بنیادی برای درمان سرطان هیچگونه عوارضی نخواهد داشت. حتی رد پیوند هم در این روش وجود ندارد؛ مهم تر از همه این است که عوارض شیمی درمانی در این پروسه وجود نخواهد داشت.
وی با تاکید بر اینکه در واقع ما با چند سلاح توسط سلول های بنیادی به جنگ با تومورسرطانی می رویم تا این سلولها بتوانند جایگزین شیمی درمانی شود، خاطر نشان کرد: استفاده از سلول بنیادی برای درمان سرطان هیچگونه عوارضی نخواهد داشت. حتی رد پیوند هم در این روش وجود ندارد؛ مهم تر از همه این است که عوارض شیمی درمانی در این پروسه وجود نخواهد داشت. عضو هیات علمی دانشکده پزشکی دانشگاه علوم پزشکی شهید بهشتی با بیان اینکه تحقیقات ما در این دانشکده روی ۳ نوع سرطان نتیجه داده است، گفت: این تحقیقات روی سرطانهای رحم، سینه و پروستات نتیجه داده است و می توانیم با سلول های بنیادی این نوع سرطان ها را درمان کنیم. اکنون در حال تحقیقات روی سرطان پانکراس هستیم.
عضو هیات علمی دانشکده پزشکی دانشگاه علوم پزشکی شهید بهشتی با بیان اینکه تحقیقات ما در این دانشکده روی ۳ نوع سرطان نتیجه داده است، گفت: این تحقیقات روی سرطانهای رحم، سینه و پروستات نتیجه داده است و می توانیم با سلول های بنیادی این نوع سرطان ها را درمان کنیم. اکنون در حال تحقیقات روی سرطان پانکراس هستیم. خبر گزاری مهر
خبر گزاری مهر
 Reference:mehrnews.com/xTrbt
Reference:mehrnews.com/xTrbt@دانش-آموزان-آلاء
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -

#معرفی_چهرههای_زیست_فناوری
دکتر کوروش شاهپسند دانش آموخته دانشگاه هاروارد عضو هیئت علمی پژوهشگاه رویان و کاشف کانفورماسیون بیماری زای پروتئین تائو(عامل ایجاد آلزایمر) و داروی درمان بیماری آلزایمردکتر کوروش شاهپسند درباره تحقیقات خود بر روی بیماری آلزایمر گفت: در زمانی که در دانشگاه هاروارد تحصیل می کردم عامل اصلی مرگ سلولهای عصبی را شناسایی کردم. در همین راستا در زمانی که به ایران بازگشتم یک آنتیبادی به عنوان واکسن درمانی علیه عامل اصلی مرگ سلولهای عصبی طراحی کردم.
وی افزود: زمانی که این آنتیبادی به عنوان یک دارو به سلول های عصبی کشتداده شده تزریق شد با توقف مرگ سلولهای عصبی روبه رو شدیم؛ در واقع به نوعی درمان آزمایشگاهی آلزایمر را در اختیار داریم.
دکتر شاهپسند با بیان این که عامل اصلی مرگ سلولهای عصبی حالت خاصی از پروتئین تائو است، گفت: این پروتئین در مغز وجود دارد و در شرایط آلزایمر یا بیماریهای مختلف دچار اختلالات ساختاری میشود. ما شکل سمی این پروتئین را شناسایی کردیم و علیه آن یک آنتیبادی ساختیم. این آنتیبادی به پروتئین تائو میچسبد و آن را از بین میبرد.
وی ادامه داد: این دارو در حال گذراندن مراحل ثبت در وزارت بهداشت است تا مجوز کارآزمایی بالینی آن اخذ شود. پس از اخذ مجوز، بر روی بیماران کارآزمایی بالینی انجام میشود. این نخستین داروی درمان آلزایمر است که در ایران در حال آمادهسازی جهت ثبت در وزارت بهداشت است.
این دانشآموخته دانشگاه هاروارد درباره دیگر فعالیتهای تحقیقاتی خود گفت: در حال حاضر ۵۶ طرح تحقیقاتی در حال پیگیری است. پروتئین تائو که در طی بیماریهای عصبی دچار تغییرات ساختاری میشود بر روی ۲۵ بیماری دستگاه عصبی مانند پارکینسون، سندرم داون، دیابت و بیماریهای دیگر نقش دارد. پس از این که مجوز کارآزمایی بالینی داروی آلزایمر را اخذ کردیم با فاصله زمانی و به موازات آن، تحقیقات بر روی بیماریهایی که پروتئین تائو بر آنها نقش دارد را آغاز میکنیم.
بخشی از مصاحبه دکتر کوروش شاهپسند:



https://uupload.ir/view/8jr_vid-20210123-wa0000.mp4/@دانش-آموزان-آلاء @تجربیا @ریاضیا
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
آیا پیوند سلولهای بنیادی خونساز می تواند از بدتر شدن علائم در بیماری ام اس جلوگیری کند؟
محققین کشور ایتالیا به تازگی پژوهشی را طراحی کردند که از سلولهای بنیادی خونساز برای کاهش علائم بیماران مبتلا به ام اس استفاده کردند.محققین کشور ایتالیا به تازگی پژوهشی را طراحی کردند که از سلولهای بنیادی خونساز برای کاهش علائم بیماران مبتلا به ام اس استفاده کردند.
در این مطالعه که در مجله Neurology به چاپ رسیده است، این فرضیه مطرح شده است که از پیوند سلولهای بنیادی خونساز به بیماران مبتلا ام اس (مخصوصا بیمارانی که نسبت به درمانهای رایج مقاومت نشان دادهاند) بتوان علائم ناشی از این بیماری را کاهش داد.
نویسنده این مقاله اذعان داشت که "روش های رایج برای جلوگیری از حملات و اثرات بیماری ام اس چندان در بلند مدت کارامد نمی باشد بطوریکه مطالعات قبلی نشان داده است که نیمی از مبتلایان که داروهای ام اس را استفاده می کردند پس از یک بازه 10 ساله علائم وخیم تری را نشان دادند."
در این مطالعه 210 فرد مبتلا به ام اس (با میانگین سنی 35 سال) که بین سالهای 1997 و 2019 پیوند سلولهای بنیادی خونساز را انجام داده بودند ، وارد مطالعه شدند. از این تعداد ، 122 نفر مبتلا به MS عود کننده-بهبودیافته ، 86 نفر MS با عود مجدد و دو نفر MS بدون سابقه قبلی، بودند. شدت علائم MS هر فرد در 6 ماه ، 5 سال و 10 سال پس از پیوند مورد بررسی قرار گرفته شد.
پس از بررسی پنج ساله، محققین دریافتند که 80٪ از بیماران هیچ گونه علائمی از بیماری ام اس نداشته اند و از این میان پس از 10 سال 66٪ هنوز بدتر شدن علائم و حملات را تجربه نکرده بودند.
مجری این طرح ادامه داد:" نتایج ما بسیارتامل برانگیز است، زیرا نشان میدهد پیوند سلولهای بنیادی خونساز ممکن است مانع از بدتر شدن علائم در طولانی مدت شود. نتایج بهبودی بیماران با توجه به تنوع گروه های مورد مطالعه،متفاوت بود، بطور مثال در گروه عود کننده-بهبودیافته به ترتیب 86 و 71 درصد بعد از 5 سال و 10 سال علائمی حاکی از شدت یافتن بیماری مشاهده نشد."
این گروه تحقیقاتی همچنین گزارش داد که برخی از افراد طی 10 سال پس از درمان در وضعیت خود بهبود یافته اند.
این مطالعه نشان میدهد که سرکوب سیستم ایمنی به دنبال پیوند سلولهای بنیادی خونساز میتواند به عنوان درمانی برای افراد مبتلا به ام اس در نظر گرفته شود ، به ویژه افرادی که به درمان معمولی پاسخ نمی دهند!
با این وجود مجریان این طرح امید داشت تا با انجام مطالعات بیشتر در وسعت بزرگتر بتوان ادعاهای این مطالعه را اثبات کنند.
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
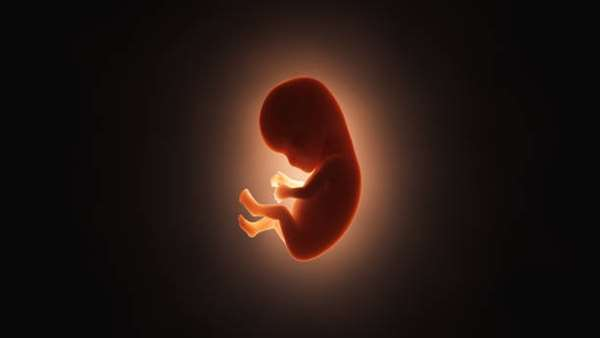
محققان نشان داده اند که پروتئین های کراتین در جنین اولیه و مرحله هشت سلولی جنین، نقش مهمی را در تنوع سلول به سلول بازی می کنند. در مرحله بلاستوسیستی، این ناهمگونی خودش را به صورت شبکه متراکمی از کراتین ها در تروفواکتودرم نشان می دهد و این با عدم بیان کراتین در توده داخلی سلولی(ICM) همراه است.
تصویربرداری زنده با استفاده از mRNA کراتین نشان دار شده به صورت فلورسنت نشان دهنده سازمان دهی شدن فیلامنت های کراتین در ناحیه راسی سلول ها در مرحله اینترفاز است که منجر به توارث غیر متقارن فیلامنت های کراتین به سلول های دختری تبدیل شونده به تروفواکتودرم می شود. این در حالی است که سلول های دختری فاقد کراتین به نوعی درون روی می کنند و به سلول های توده داخلی تبدیل می شوند که در آینده لایه های جنینی و سلول های تخصص یافته جنین را تولید می کنند.
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
بافت های بدن به طور دائم بوسیله سلول های بنیادی بازسازی می شوند. این سلول های بنیادی در مکان های خاصی از بافت های مختلف قرار دارند که آن را اصطلاحا ریز محیط یا نیچ می نامند و در آن جا این سلول های بنیادی با سایر انواع سلول ها برهمکنش می کنند. یافته های این مطالعه جدید نشان می دهد که سلول های بنیادی مغزی به تغییراتی که در خارج از مغز رخ می دهد پاسخ می دهند.در مطالعه ای که روی موش ها صورت گرفته است، ثابت شده است که التهاب تولید بوسیله عفونت های باکتریایی در هر بخشی از بدن می تواند به طور موقت سلول های بنیادی مغزی را فعال کند و آن ها را آماده عملکرد سازد. زمانی که التهاب فروکش می کند، این سلول ها به مرحله خاموشی خود بر می گردند. این مطالعه موجب می شود که محققین درک بهتری از ارتباط بین سلول های بنیادی و محیط سیستمیک (بقیه بدن) داشته باشند. تاکنون این انتظار وجود داشت که سلول های بنیادی با محیط نزدیک شان برهمکنش داشته باشند اما این اولین بار است که مشخص می شود که سلول های بنیادی تحت تاثیر محیط های با فواصل دورتر نیز قرار دارند.
https://www.sciencedirect.com/science/article/abs/pii/S1934590920305105?via%3Dihub
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
اکنون به خوبی مشخص شده است که COVID-19 تنها یک بیماری تنفسی نیست و علاوه بر ریه ها می تواند سیستم قلبی عروقی، گوارشی و عصبی را نیز تحت تاثیر قرار دهد. در این میان بیماران علایم عصبی مانند از دست رفتن یا تغییر در حس بویایی و چشایی، سردرد، خستگی، سرگیجه و تهوع را تجربه می کنند و برخی نیز دچار سکته یا مشکلات شدیدتر می شوند.
اما در پژوهشی جدید محققان به بررسی نحوه ورود ویروس به سیستم عصبی و نحوه پاسخ دهی سیستم ایمنی به ویروس پرداختند. آن ها حضور RNA و پروتئین مربوط به ویروس کرونا را در نواحی از نظر آناتومیکی مجزایی از نازوفارینکس و مغز نشان داده اند. علاوه بر این؛ آن ها تغییر مورفولوژیک مربوط به عفونت مانند انفارکته ترومبئومبولیک ایسکمی را در سیستم عصبی مرکزی نشان داده اند که دال بر گرایش ویروس به سمت سیستم عصبی است. به عقیده آنها ویروس کرونا می تواند با عبور کردن از سطح مواجه عصبی-موکوسی در موکوس بویایی خود را به سیستم عصبی برساند و موکوس بویایی و بافت اندوتلیالی و عصبی که شامل پایانه های عصبی بویایی و حسی است را تحت تاثیر قرار دهد.
https://medicalxpress.com/news/2021-01-insights-covid-brain.html
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
تیمی از محققان از بخشهای مختلف در دانشگاه استنفورد ، اطلس سلولی ریه انسان را ایجاد کرده اند که ده ها نوع سلول را که بخشی از ریه ها را تشکیل می دهد ، نشان می دهد. محققان در مقاله خود در مجله Nature ، کار خود را (که بیشتر شامل توالی RNA تک سلولی است) و برخی از داده هایی که در طی کار در مورد ریه ها به دست آورده اند ، توصیف می کنند.
برای ایجاد اطلس ، محققان نمونه های بافتی از نواحی مختلف ریه ها را به همراه نمونه های خون همراه جمع آوری کردند. هر یک از نمونه ها به اجزای سلولی خود تجزیه شده و سپس بر اساس نوع: ایمنی ، اپیتلیال ، اندوتلیا یا معده طبقه بندی می شوند.
محققان نسخه رونویسی برای تقریباً 75000 سلول را تولید کردند. با استفاده از نشانگرها ، تیم سپس سلول ها را خوشه بندی کرد تا 58 جمعیت سلول را متمایز نشان دهد. با این کار ، آنها قادر به تولید پروفایل بیان برای 91 درصد از انواع ریه بودند - و همچنین 14 نوع سلول ریه را یافتند که قبلاً شناخته نشده بودند. آنها همچنین تقریباً 200 نشانگر پیدا کردند که می تواند برای شناسایی انواع ناشناخته ای که پیدا کردند ، مورد استفاده قرار گیرد.
تیم تحقیق دریافت که آنها قادر به استفاده از اطلس حاصل برای ردیابی اهداف هورمون در ریه ها هستند. با انجام این کار ، آنها دریافتند که برخی گیرنده های هورمونی به طور گسترده در نقاط مختلف ریه ها بیان می شوند ، در حالی که دیگران اینگونه نیستند. به عنوان بخشی از این تلاش ثانویه ، محققان همچنین مناطقی را شناسایی كردند كه 233 ژن در آنها بیان می شود و می تواند توسط دانشمندانی كه در زمینه شناخت و درمان طیف گسترده ای از بیماری های ریوی كار می كنند ، استفاده شود.
محققان همچنین از اطلس خود برای مقایسه ریه های انسان و موش استفاده کردند. آنها دریافتند که موش ها تقریباً 30٪ از انواع سلولهای ریوی انسان و انسانها تقریباً 5٪ از انواع سلولهای ریه موش را ندارند. یافته های آنها نشان می دهد که تنوع در گونه های اولیه پستانداران بیش از آنچه تصور می شد وجود داشته است.
محققان اظهار داشتند که این اطلس می تواند توسط طیف گسترده ای از محققان پزشکی مورد استفاده قرار گیرد و خاطرنشان می کند که بینش جدیدی در زمینه تنظیم ، برهم کنش و عملکرد سلول ها و انواع ریه فراهم می کند.
محققان اظهار داشتند که این اطلس می تواند توسط طیف گسترده ای از محققان پزشکی مورد استفاده قرار گیرد و خاطرنشان می کند که بینش جدیدی در زمینه تنظیم ، برهم کنش و عملکرد سلول ها و انواع ریه فراهم می کند.
https://medicalxpress.com/news/2020-11-stanford-team-cellular-atlas-human.html
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
در سال های اخیر جایگزینی میکروگلیاها با سلول های غیر میکروگلیایی(مانند سلول های بنیادی و ...) برای درمان اختلالات مربوط به این سلول ها پیشنهاد شده است. با این حال، اغلب این تلاش ها مانند استفاده از رویکرد متداول پیوند مغز استخوان، به دلیل کارایی پایین جایگزینی این سلول ها با شکست مواجه شده است.
در مطالعه صورت گرفته در دانشگاه فودان چین، محققین استراتژی های موثری را برای جایگزینی میکروگلیاها پیشنهاد کرده اند که شامل جایگزینی میکروگلیاها بوسیله پیوند مغز استخوان(mrBMT)، جایگزینی میکروگلیاها بوسیله خون محیطی(mrPB) و جایگزینی میکروگلیاها بوسیله پیوند میکروگلیاها(mrMT) است. نتایج نشان داده است که جایگزینی میکروگلیاها با مغز استخوان و خون محیطی به سلول های شبه میکروگلیا اجازه می دهد که میکروگلیاهای موجود در سیستم عصبی مرکزی را به طور موثری جایگزین کنند. از طرف دیگر استفاده از پیوند میکروگلیا موجب جایگزینی این سلول ها در نواحی مغزی مد نظر می شود.
Reference:https://medicalxpress.com/news/2020-08-scientists-malfunctioning-vacuum-cleaner-cells.html
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
آتروفی اپتیک غالب(DOA) با تخریب اعصاب چشمی مشخص می شود و در ابتدای بلوغ موجب بروز علایمی در بیماران می شود که از جمله آن ها می توان به از بین رفتن تدریجی بینایی و نقص در تشخیص رنگ و ... اشاره کرد که می تواند در نهایت منجر به نابینایی شود و متاسفانه درمان موثری برای این مشکل وجود ندارد.
در این میان ژنی به نام OPA1 دستورالعمل هایی را برای تولید پروتئین ایجاد می کند که در سلول ها و بافت های سراسر بدن یافت می شود و برای حفظ عملکرد مناسب میتوکندری ها حیاتی است. بدون وجود OPA1، عملکرد میتوکندریایی به طور مناسبی صورت نمی گیرد و روی ارتباطات سلولی اثرات منفی می گذارد. در مورد بیماران مبتلا به آتروفی اپتیک غالب، جهش در ژن OPA1 و عملکرد نامناسب میتوکندریایی موجب شروع بیماری و پیشرفت در آن می شود. در مطالعه ای جدید در دوبلین، محققین ژن درمانی جدیدی را ارائه کرده اند که با اصلاح موتاسیون OPA1 می تواند عملکرد میتوکندریایی را بهبود بخشیده و با تقویت توانایی تولید انرژی از آسیب سلول های عصب بینایی جلوگیری کند. به عقیده آن ها این رویکرد درمانی می تواند با گذشت زمان و برطرف کردن چالش ها برای درمان آتروفی اپتیک غالب و سایر بیماری های چشمی موثر باشد.
Reference:https://www.tcd.ie/news_events/articles/scientists-develop-new-gene-therapy-for-eye-disease/
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
کم خونی سلول داسی شکل و بتا تالاسمی از اختلالات اصلی ژنتیکی خون است که در اثر جهش در ژن تولید کننده بتاگلوبین، یک جز هموگلوبین ایجاد می شود. افراد مبتلا به هر دو بیماری از کم خونی ، حملات درد ، خستگی و خطر آسیب به اعضای بدن رنج می برند که همه اینها بر کیفیت زندگی آنها تأثیر می گذارد. انتقال خون مکرر برای تسکین علائم یا پیوند مغز استخوان به عنوان یک راه حل طولانی مدت تنها گزینه های درمانی تاکنون بوده است.
انقلاب اخیر مهندسی ژنوم سبب جلب توجه محققان برای درمان این بیماری ها با استفاده از ژن درمانی شده است. از آنجا که سلول های بنیادی خونساز برای ویرایش ازمایشگاهی نسبتاً در دسترس هستند ، کم خونی سلول داسی شکل و بتا تالاسمی کاندیداهای اصلی مطالعات ژن درمانی شده اند. یک راه حل اصلی نحوه استفاده از CRISPR در تحقیق و درمان کم خونی سلول داسی شکل و بتا تالاسمی است.
در اینجا به طور خاص موفقیت درمان CTX001 ، یک داروی تحقیقاتی مبتنی بر CRISPR را گزارش می دهیم که در آزمایش های بالینی برای درمان بیماری سلول داسی شکل و بتا تالاسمی آزمایش می شود. گزارش های اخیر نشان می دهد که CTX001 ، که توسط Vertex Pharmaceuticals و CRISPR Therapyics تهیه شده است ، بیش از یک سال است که در بازگرداندن سطح هموگلوبین و کاهش علائم در بیماران موثر است. این داده ها در همایش انجمن هماتولوژی 2020 آمریکا ارائه شده است و جزئیات داده های دو بیمار در مجله پزشکی New England منتشر شده است.
@دانش-آموزان-آلاء @تجربیا @دوازدهم
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
محققان دانشگاه فناوری و طراحی سنگاپور (SUTD) اقدام به طراحی چاپگر سه بعدی در مقیاس میکرو نمودند تا با تمایز سلول های بنیادی، سلول های قلبی را حاصل نمایند. این مطالعه که در مجله Bioprinting به چاپ رسید، ثابت نمود که ابزارهای مکانیکی همچون چاپگرهای سه بعدی میتوانند برخی شرایط موثر در تمایز سلول های بنیادی اعم از میزان تکثیر، اندازه سلول ها و شکل آن ها را کنترل نماید.
این فناوری و رویکرد می تواند با کنار هم قرار دادن سلول های متفاوت، افق جدیدی برای تولید و بازسازی اندام ها باشد.
محقق اصلی مطالعه ، اظهار داشت: "زمینه تولید مواد و جوهرهای زیستی با سرعت بی نظیری در حال پیشرفت است. ما شاهد آن هستیم که زیست چاپگرهای امروزی دقت و سرعت بالا و در عین حال هزینه ی کمتری را دارند که این امر در چند سال گذشته غیرقابل تصور بود. آنچه ما نشان داده ایم این است كه چاپ سه بعدی در حال حاضر به نقطه ای از دقت مهندسی رسیده است كه می تواند نتیجه تمایز سلول های بنیادی را كنترل كند. این امر خود نوید بخش پیشرفت های فراوانی در حوزه طراحی و توسعه دارو ها می تواند باشد.
Link:https://www.regmednet.com/3d-printed-device-developed-for-directed-stem-cell-differentiation/
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
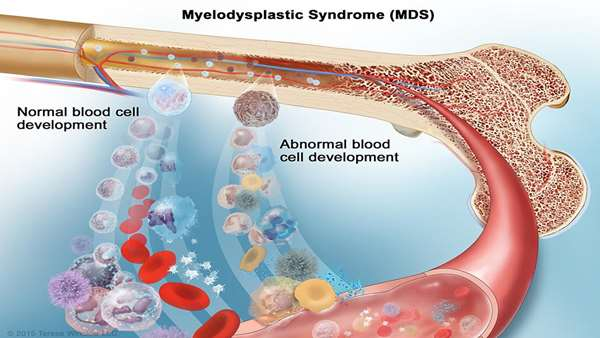
محققان یک کارآزمایی بالینی را روی افراد پیر بین 50 تا 75 سال و مبتلا به سندرم میلودیسپلازی پر خطر انجام دادند تا موثر بودن پیوند سلول های بنیادی خون ساز آلوژن روی آن ها را ارزیابی کنند. در این مطالعه که روی 384 بیمار صورت گرفت نتایج داد که نرخ بقای کلی و سه ساله در بیمارانی که متحمل سلول درمانی آلوژن شدند در مقایسه با گروه کنترل، 48 درصد در برابر 26 درصد بود.
این در حالی بود که هیچ عارضه جانبی مربوط به استفاده از سلول های بنیادی در آن ها مشاهده نشد. در این افراد میزان بقای بدون نشان دادن علایم بیماری نیز بیشتر از گروه کنترل بود. به عقیده ناکامورا، این رویکرد درمانی می تواند در صورت تقویت شدن با فاکتورهای مختلف به رویکرد درمانی امیدوار کننده برای بیماران مبتلا به سندرم میلودیسپلازی تبدیل شود.
Reference:https://medicalxpress.com/news/2020-12-stem-cell-transplant-benefits-older.html
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
تولید تیموس دارای عملکرد در آزمایشگاه
سال هاست که توجه زیادی به فرایندهای دخیل در تولید تیموس شده است و محققین بسیاری سعی در دستکاری این فرایندها در بالین داشته اند زیرا تغییرات در تکوین یا عملکرد تیموس می تواند منجر به نقص ایمنی و یا بیماری های خود ایمن شود.
در مطالعه ای جدید در انستیتو فرانسیس کریک، محققین سلول های هیبرید اپی تلیال-مزانشیم را شناسایی کرده اند که قادرند در شرایط آزمایشگاهی به صورت طولانی مدت تکثیر شوند و می توان از آن ها برای بازسازی و تولید یک فنوکپی آناتومیک از تیموس طبیعی استفاده کرد و البته برای این کار به سلول های بینابینی تیموسی و ماتریکس خارج سلولی سلول زدایی شده تیموس نیاز است. این تیموس مهندسی شده از نظر عملکردی فعال بوده و این قابلیت را دارد که از بلوغ سلول های T در شرایط درون تنی(بعد از پیوند به موش ناقص از نظر ایمنی) حمایت کند.
یافته های این مطالعه نشان دهنده ارتباط سلولی و مولکولی بین استروما، ماتریکس خارج سلولی و تیموسیت ها است و چشم اندازهای کاربردی را برای درمان بیماری های ایمونولوژیک اکتسابی و مادرزادی ارائه می دهد.
Reference:https://imms.kz/?q=en/news/869
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -

محققان دانشگاه موناش از ترکیب امواج صوتی و دینامیکی سیال، یک رویکرد جدید به منظور جداسازی اسپرم های با کیفیت بالا در تولید مثل ایجاد کرده اند و روزنه های امید جدیدی را برای تشکیل خانواده در زوج های نابارور فراهم نموده اند.
این فرآیند سریع و خودکار که توسط تیمی از گروه مهندسی مکانیک و هوافضا دانشگاه موناش ایجاد شده است ، می تواند اسپرم را با مورفولوژی طبیعی سر و DNA خالص از نمونه های خام منی جدا کند.
این دستگاه می تواند تقریباً 140 اسپرم در ثانیه پردازش کرده و بیش از 60،000 اسپرم با کیفیت بالا در کمتر از 50 دقیقه انتخاب کند.
این مطالعه در مجله پیشرو میکروسیالات Lab on a Chip منتشر شده است. نظارت بر این کار توسط دکتر رضا نصرتی و پروفسور آدریان نیلد - متخصصان ریز سیالات از گروه مهندسی مکانیک و هوا فضا انجام شده است.
نتایج این مطالعه نشان می دهد که جمعیت اسپرم انتخاب شده نسبت به نمونه خام اولیه (52 درصد) و زیرمجموعه دور ریخته شده اسپرم (36 درصد)، درصد قابل توجهی بالاتر از اسپرم های متحرک به تدریج (83 درصد) را نشان می دهند"
دکتر نصرتی می گوید میزان موفقیت به پارامترهای مختلفی بستگی دارد ، اما در نهایت به کیفیت اسپرم و تخمک بستگی دارد.
دکتر نصرتی گفت: "روند ما با هدف انتخاب اسپرم بهتر در یک بازه زمانی سریعتر انجام می شود، بنابراین امیدوارم این امر به بهبود نتایج در تولید مثل کمک کند. هنگامی که به طور کامل آزمایش و اجرا شود ، این روش می تواند پنجره ها و فرصت های جدیدی را برای زوج های نابارور برای داشتن یک کودک باز کند.
ما امیدواریم که با آزمایش بیشتر ، فرآیند انتخاب اسپرم ما بتواند فرصت های جدیدی فراهم کند و برای صنعت کمک به تولید مثل مفید باشد و به از بین بردن ترس ، اضطراب و کلیشه های منفی مرتبط با ناباروری کمک کند.
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
محققین در مطالعه ای جدید بر بازبرنامه ریزی سلولی متکی بوده اند تا مدل از نظر ژنتیکی مشابهی از سلول های پیر و جوان ارائه دهند. آن نها سلول های بنیادی مزانشیمی را از مایع سینوویال جداسازی کرده و آن ها را به سلول های بنیادی پرتوان القایی(iPSCs) بازبرنامه ریزی کردند.
در ادامه آن ها این سلول های iPS را مجددا به به سلول های بنیادی مزانشیمی القا کردند تا به نوعی موجب جوان سازی سلول های بنیادی مزانشیمی اولیه شوند. در ادامه این سلول های بنیادی مزانشیمی بازبرنامه ریزی و جوان شده با سلول های بنیادی مزانشیمی اولیه مقایسه شدند. آنالیزها نشان داد که بیان GATA6 به عنوان یک پروتئین مهم در تکوین سیستم گوارشی، قلب و ریه در سلول های بازبرنامه ریزی شده سرکوب شده بود.
این سرکوب GATA6 منجر به افزایش فعالیت پروتئین های ضروری برای تکوین جنینی موسوم به SHH و هم چنین افزایش بیان FOXP1 شد که برای تکوین مناسب قلب، ریه و مغز ضروری است. این مطالعه نشان می دهد که مسیر GATA6/SHH/FOXP1 یک مسیر کلیدی است که پیری و جوان سازی سلول های بنیادی مزانشیمی را تنظیم می کند و این یافته ها می تواند درک ما را در مورد پیری سلول های بنیادی مزانشیمی که فاکتوری تاثیرگذار در پزشکی بازساختی است افزایش دهد.
Reference:https://medicalxpress.com/news/2020-11-gene-responsible-cellular-aging.html
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -

فناوری چاپگرهای سهبعدی که با زیستمواد میتوانند بافتهای مبتنی بر سلولهای زنده را تولید کنند، توسط یک شرکت فناور داخلی بومی سازی شده است.
مجموعه فناور ایده کاران سهبعدی شریف با نقش آفرینی فعالان حوزههای مهندسی مکانیک، الکترونیک، نرمافزار، زیستمواد، سلولی و مولکولی بر روی ساخت چاپگرهای سهبعدی زیستی فعالیت میکند و زمینه را برای تولید چاپگرهای زیستی آغاز کرده است.
در این مجموعه فناور برای نخستین بار چاپگر سهبعدی زیستی بر پایه نیوماتیک با قابلیت چاپ سلولهای زنده در محیط تمیز طراحی و توسعه داده شد که به کمک آن میتوان بافتهای مصنوعی را با دقت و سرعت بالا تولید کرد.
هم اکنون نمونههای تجاری این دستگاه در حال فعالیت در مراکز پژوهشی و ارائه خدمت به استادان و دانشجویان حوزه مهندسی بافت و پزشکی بازساختی است. با ارائه این محصول به محققان و فعالان فناور، زمینه تولید فرآوردههای پرکاربرد در حوزه زیستی و سلامت فراهم میشود.
برخورداری از قابلیتهای نمونه خارجی
مدلهای مختلف این دستگاه با استفاده از قطعهها و قابلیتهای مختلف، از قابلیت چاپ انواع هیدروژل حاوی سلول، بایومتریالهای کامپوزیت حاوی پلیمرهای زیستتخریبپذیر و ترکیبی از هردو عنصر را دارد. با بهرهگیری از این دستگاه بافتهای مصنوعی مورد نظر خود را با اهداف گوناگون ایجاد کرده و مورد تست و بررسی قرار دهند.
این دستگاه با قابلیت کنترل دما از صفر تا 175 درجه سانتیگراد این امکان را میدهد که طیف وسیعی از مواد را به چاپ برساند. قابلیتهای لینک کردن با استفاده از نور فرابنفش این چاپگر با استفاده از دو منبع نور، قدرت بالا را در محدوده طول موج 365 و 405 نانومتر ارائه میکند. دستگاه به گونهای ساخته شده که جابهجایی آن آسان است و میتوان آن را به مکانهای خاص انتقال داد.
فعالان فناور این شرکت، قابلیت و جابهجایی بستر دستگاه را به گونهای طراحی کردهاند که بتواند با دقت 5 میکرون در هر جهت حرکت کند. چاپگر زیستی با قابلیت چاپ پلیمرها و هیدروژلها در محیطی بدون آلودگی و ذرات معلق، میتواند راه را برای چاپ سلول هموار کند.
این شرکت با حمایت ستاد توسعه علوم و فناوریهای سلولهای بنیادی معاونت علمی و فناوری محصول خود را توسعه داده است.
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
به نظر می رسد که مهار آنزیمی به نام کیناز زیپر لوسین دو گانه (DLK) قویا از نورون ها در برابر طیف وسیعی از بیماری های مخرب عصبی حمایت می کند اما این آنزیم بازسازی آکسون ها را نیز مهار می کند. تاکنون روش موثری برای تعدیل ژن ها به منظور بهبود بقای طولانی مدت نورون ها و هم چنین پیشبرد بازسازی آکسون ها ارائه نشده است.
در مطالعه ای جدید، تیمی از محققین در دانشگاه کالیفرنیا خانواده ای از آنزیم ها موسوم به کیناز های GCK-IV را شناسایی کرده اند که مهار آن ها قویا از نورون ها حفاظت می کند و این در حالی است که اجازه بازسازی آکسون ها را نیز می دهد و همین امر آن را به یک رویکرد درمانی جذاب برای درمان برخی از بیماری های مخرب عصبی تبدیل می کند.
در این مطالعه محققین ابتدا سلول های گانگلیونی شبکیه(RGCs) را از سلول های بنیادی تولید کردند و در ادامه مجموعه ای از غربالگری ها را روی آن ها انجام دادند. این سلول های گانگلیونی شبکیه، نوعی نورون هستند که در نزدیک سطح داخلی شبکیه چشم قرار گرفته اند. آن ها اطلاعات بینایی را از گیرنده های نوری دریافت می کنند و با تجمیع آن ها به انتقال شان به مغز کمک می کنند. نتیجه غربالگری مواد شیمیایی مختلف، شناسایی مهار کننده خانواده آنزیمی GCK-IVبود که هم از سلول های گانگلیونی شبکیه حفاظت می کند و هم اجازه بازسازی آکسون ها را می دهد.
https://www.pnas.org/content/117/52/33597
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
محققان در مطالعه ای جدید سعی داشته اند که شبکه های ژنی و پروتئینی که در بیماری های قلبی مادرزادی دچار مشکل می شوند را شناسایی کرده اند. شماری از جهش های ژنتیکی در این بیماری های قلبی مادرزادی دخیل هستند که اولین مورد آن ها که شناسایی شد مربوط به ژنی به نام Tbx5 بود. پروتئین TBX5، فاکتور رونویسی است که بیان چندین ژن مختلف را در پایین دست خود کنترل می کند. بیشتر مطالعاتی که روی اثر جهش های Tbx5 بر قلب صورت گرفته است بر مطالعات جانوری(موشی) متمرکز بوده است.
در پژوهشی جدید، دکتر برانیو و همکارانش این اثر را در سلول های انسانی مورد مطالعه قرار دادند. آن ها از سلول های بنیادی پرتوان القایی(iPSCs) استفاده کردند و با استفاده از فناوری ویرایش ژنومی CRISPR/Cas9 جهش Tbx5 را در این سلول ها ایجاد کرده و سپس آن ها را برای تبدیل شدن به سلول های قلبی القا کردند. در حین تمایز قلبی این سلول ها، محققین آن ها را مورد توالی یابی RNA در سطح تک سلولی قرار دادند تا ژن هایی که تحت تاثیر جهش Tbx5 قرار می گیرند را شناسایی کنند.
ارزیابی ها نشان داد که ژن های بی شماری تحت تاثیر Tbx5 جهش یافته در سطوح بالاتر یا پایین تر بیان می شوند، هر چند همه سلول ها پاسخ یکسانی به جهش Tbx5 ندارند. این تنوع در جهش و پاسخ دهی به جهش را محققین دلیل نشان دادن علایم مختلف بوسیله بیماران می دانند.
https://medicalxpress.com/news/2020-12-reveals-networks-genes-involved-congenital.html
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
در جدید ترین مطالعه صورت گرفته در دانشگاه سانگکیونکوان، پروژه ای به منظور بررسی اثر اگزوزوم مشتق شده از سلول بنیادی مزانشیمی بر روی کنترل خون ریزی مغزی آغاز گردید. این مطالعه با اشاره به اثر مثبت فراورده سلولی بر روی مهار خونریزی مغز،نتایج خود را در مجله STEM CELLS Translational Medicine. به چاپ رسانید.
به دنبال خونریزی شدید در مغز و افزایش فشار مایعات در این ناحیه، احتمال تشنج، فلج مغزی، عقب ماندگی رشد و مرگ و میر افزایش می یابد. لذا اهمیت این جستار میتواند روزنه امیدی را برای درمان به موقع بیماران، خصوصا کودکان (از بالاترین جامعه آماری در این نوع عارضه محسوب میشود) به حساب آید.
سلولهای بنیادی مزانشیمی قادر هستند تا با تولید مولکولهای زیستی فعال، اثر بسیار خوبی در ترمیم از خود نشان دهند.
این سلولها اگرچه امروزه به عنوان کاندیدهای مناسب در علوم پزشکی بازساختی به حساب میآید، اما عوارضی همچون قابلیت تومورزایی و انسداد عروق را میتواند به دنبال داشته باشد.
در این پژوهش با استفاده از اگزوزومهای دریافت شده از محیط کشت سلولهای بنیادی مزانشیمی، اثر آن را بر روی مدل موشی، دارای خونریزی مغزی مورد پژوهش قرار گرفته شد. نتایج نشان داد که اگزوزومهای منتقل شده حاوی فاکتور mRNA کد کننده پروتئین BDNFهستند. تحقیقات پیشین نقش این پروتئین را به عنوان یک عامل محافظتی برای سلولهای عصبی گزارش کرده است. این مطالعه در دو فاز آزمایشگاهی و پیش بالینی انجام گرفت و در تمامی گروهای دریافت کننده، اگزوزومها باعث بیان گیرندههای ترومبین در سطح سلولهای عصبی شد.
از این رو Park اظهار داشت که: " تاثیر استفاده از اگزوزومها برای مهار خونریزی بیشتر از استفاده از سلولهای بنیادی به صورت مستقیم میباشد. همچنین با توجه به مطالعات بعدی برای مشخص نمودن زمان مناسب تزریق و دوز بهینه، اظهار امیدواری از یک گام موثر برای مقابله با آثار ناشی از افزایش فشار مایعات مغزی در زمان خونریزی نمود.
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
طی تکوین مغز، دوره جنینی در تولید نورون ها از سلول های بنیادی عصبی و تبدیل آن ها به به مغز بالغ دارای عملکرد حیاتی است. هر گونه اختلالی در برنامه تکوینی می تواند منجر به نواقص شدید مغزی شود. سندرم X شکننده یک اختلال ژنتیکی است که بوسیله ناتوانی ذهنی و علایم اوتیسم مشخص می شود.
کودکان مبتلا به سندرم X شکننده عموما از تاخیر در فرایندهای تکوینی و مشکلات اجتماعی و رفتاری رنج می برند. سندرم X شکننده دچار نقص در ژن FMR1 هستند که ژن کد کننده پروتئین FNRP به عنوان یک فاکتور کلیدی در تکوین طبیعی مغز است. در این مطالعه دکتر اوسامی و همکارانش با استفاده از توالی یابی های نسل جدید صدها مولکول مرتبط با مغز جنین موشی را شناسایی کرده اند که نه تنها با فرایند نورون زایی بلکه ناتوانی های اوتیسمی و ذهنی همراه هستند.
یافته های این مطالعه نشان داده است که گروهی از مولکول های خاص در مسیرهای پیام رسانی بین سلولی مانند Ras/MAPK، Wnt/β-catenin و mTOR دخیل هستند. فعالیت mTOR در مغز جنینی موش های ناقص از نظر FMR1 بارز است و به نظر می رسد که فعالیت افزایش یافته mTOR می تواند منجر به تکثیر غیر طبیعی و تمایز سلول های بنیادی به مغز جنینی شود. در نهایت، این مکانیسم های مولکولی می توانند مسئول تکوین مغز طی دوره جنینی و مشارکت آن ها در بروز سندرم X شکننده باشند. محققین امیدوارند این اطلاعات جدید بتواند راهگشای درمان اختلالت تکوینی عصبی در آینده باشند.
https://molecularbrain.biomedcentral.com/articles/10.1186/s13041-020-00706-1
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470




