اسید و باز
-
Znbs فورمیک اسید قوی تر از استیک اسیده(گرچه هردو اسید ضعیفند)
این یعنی +H بیشتری در فورمیک اسید میتونیم داشته باشیم. پس نسبت +H محلول اول به +H محلول دوم بزرگتر از یک خواهد بود. اما این موضوع کمکی به ما نمیکنه چون به طور عددی از ما خواستهتوی پرانتز به ما یه کمکی کرده. گفته نسبت ثابت یونش دو اسید 10 هست:
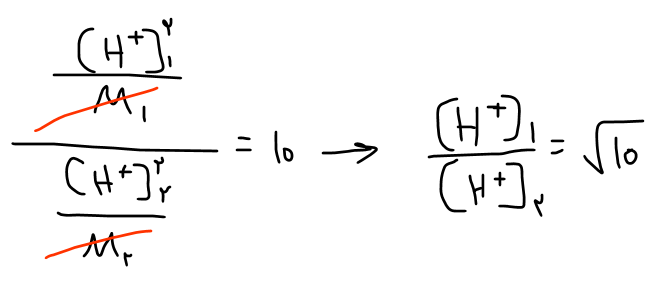
پس به نظرم چون +H محلول اول بیشتر از +H محلول دوم بود باید از رادیکال 10 بزرگتر بشه
خود پاسخنامه چی گفته؟
-
Znbs هم من اشتباه کردم هم پاسخنامه
در واقع پاسخنامه یه محاسباتی نوشته ولی با کلمات فارسیش همخوانی نداره. منم اشتباهم توی محاسباته(عین محاسبات پاسخنامه) اما استدلالم براساس اشتباهی ک کرده بودم درست بودبه هرحال راه درست اینه ک باااااااید [H]-M رو درنظر بگیریم. دلیلش اینه که نگفته ثابت تعادلمون کمتر از 10 به توان منفی 4 هستش یا درجه یونش کمتر از 0.05 هست(در صورتی که اینارو بگه میشه از [H]-M صرف نظرکرد)
راه درستش:







