سلول های بنیادی راهی به آینده
-
بسم الله الذی خلقنا من نطفه واحده
قطعا به علت پیشرفت های خیلی زیاد نتنها کشور خودموم بلکه همه دنیا در ضیمنه سلول های بنیادی و پزشکی بازساختی همه شما اسم این سلول ها رو حداقل شنیدین!
دنیای زیست شناسی سلول و مولکولی واقعا دنیای حیرت آوریه و وقتی وارد دنیای سلول های بنیادی می شیم عجیب تر هم میشه!
من تصمیم گرفتم که توی این تایپک مطالب جذاب درباره سلول های بنیادی و مسائل مربوط به اون رو با شما به اشتراک بذارم،مطالبی که برای همه بچه ها مفید خواهد بود ،حالا چه تجربی باشن، چه ریاضی و چه انسانی!
ما اینجا از خود سلول های بنیادی شروع میکنیم و به مرورو پیشرفته ش میکنیم،درباره آخرین یافته های علمی حرف میزنیم،دانشمندای بنام این رشته رو میشناسیم و قراره کلی عکس و فیلم جذاب ببینیم!
یه تایپک دیگه هم با عنوان "گفت و گو با سلول های بنیادی" ایجاد میشه که هر حرف و حدیثی بود اونجا گفته بشه!
پس دعوت میکنم از همه که همراه ما باشن تا شیرینی زیست شناسی رو بچشن!
تجربیا
انسانیا
ریاضیا
دانش-آموزان-آلاء
دهم
یازدهم
دوازدهم
فارغ-التحصیلان-آلاء -
آیا می دونید سلول بنیادی چیه؟
:small_orange_diamond:سلول بنیادی مادر تمام سلولها است و توانایی تبدیل به تمام سلولهای بدن را دارد. این سلولها توانایی خود نوسازی و تمایز به انواع سلولها را دارند. هم چنین در بازسازی و ترمیم بافتهای آسیب دیده بدن موثر بوده و میتوانند به درون بافتهاپیوند زده شوند و جایگزین سلولهای آسیب دیده شده و به ترمیم و رفع نقص در آن بافت بپردازند.
:small_orange_diamond:به دلیل توانایی منحصر به فرد سلولهای بنیادی، این سلولها امروزه از مباحث جذاب در زیست شناسی پزشکی🧫 و علوم درمانی🧬 است. هم چنین تحقیقات:mag: در این زمینه دانش ما را درباره چگونگی رشد و تکوین یک اندام از یک سلول منفرد افزایش داده و مهم تر آنکه به فهم مکانیزم جایگزینی سلولهای سالم با سلولهای آسیب دیده کمک کرده است.
خلاصه یه جورایی آینده علوم وفناوری سلول بنیادی ساخت بافت ها واندام های یدکی برای انسانه! -
#تقسیم، #تکثیر یا #خودنوزایی؟
:pushpin:در رابطه با سلولهای بنیادی شما بارها و بارها با واژگان #تکثیر، #تقسیم یا #خودنوزایی روبرو خواهید شده . درباره تفاوت آنها با هم بیشتر بدانید:
✍ #تقسیم_سلولی (cell devision)، فرآیندی است که طی آن، یک سلول (معمولا پس از رشد و بزرگ شدن)، دو نیم شده و دو سلول را به وجود می آورد.
✍ #تکثیر_سلولی (cell proliferation)، یعنی کثرت و افزایش تعداد، که به این معنی است که در اثر تقسیمات پی در پی سلول، سلول های زیادی ایجاد می شوند؛ پس تکثیر به معنی افزایش تعداد سلول ها در اثر تقسیم است.
✍ #خودنوزایی (self-renewal)، تقسیم و تکثیر خاصِ سلولهای بنیادی است! خودنوزایی به این معنی است که یک سلول بنیادی به طور پی در پی و طولانی مدت، بدون اینکه بزودی پیر شود (برخلاف سایر سلولها که در اثر تقسیم بزودی پیر خواهند شد)، تقسیم و تکثیر شود و بتواند قابلیت تکثیر خود را برای مدتهای طولانی و برای برخی از انواع سلولهای بنیادی (موسوم به سلولهای بنیادی پرتوان) برای همیشه حفظ کند (لااقل از لحاظ تئوری). نکته دیگر درباره خودنوزایی، آن است که خودنوزایی همزمان با حفظ یک پتانسیل تکوینی و تمایزی روی میدهد. یعنی سلولهای بنیادی به طور معمول میتوانند با هر بار تقسیم، علاوه بر خود، لااقل یک سلول تمایزیافته را نیز به وجود آورند. منتها محققان در آزمایشگاه راههایی را پیدا کردهاند که میتوانند سلولهای بنیادی را وادار کنند که در حالت تمایزنیافته باقی بمانند و طی هر تقسیم سلولی، دو سلول بنیادی همانند خود ایجاد کنند. اما معمولاً در بدن به طور طبیعی، سلولهای بنیادی دارای تقسیم سلولی نامتقارن هستند که طی آن، یک سلول بنیادی و یک سلول تمایزیافته بوجود میآید.
-

شهید دکتر سعید کاظمی آشتیانی،دانشمند بزرگ ایران اسلامی ، رئیس پژوهشکده رویان – مرکز علمی پیشتاز تحقیقات #سلولهای_بنیادی و شبیه سازی در ایران و از بزرگترین مراکز درمانی تحقیقاتی پزشکی تولید مثل در کشور می باشد .:small_orange_diamond: از جمله افراد تاثیر گذاری که پس از انقلاب اسلامی در بخش پزشکی پدیدار گشت، شهید دکتر سعید کاظمی آشتیانی را می توان نام برد، کسی که نامش در ایران و حتی جهان با عنوان پژوهشکده رویان و درمان ناباروری و تولید #سلولهای_بنیادی و اقدامات موثر این پژوهشکده در ارائه هر چه بهتر خدمات درمان ناباروری و دستاوردهای بزرگ ملی آن نظیر تولید، تکثیر و انجماد نخستین رده #سلولهای_بنیادی جنینی تحقیقات گسترده در زمینه سلول درمانی بیماری های مختلف از قبیل ضایعه قرنیه و عوارض سکته قلبی، راه اندازی نخستین بانک خون بند ناف و پیگیری طرح تولید نخستین جانوران شبیه سازی شده خاورمیانه گره خورده است.
دانشمندی که صدور علم و دانش ایران به جای نفت از مهمترین آرزوهایش بود .
:high_brightness: یادش گرامی باد -
-
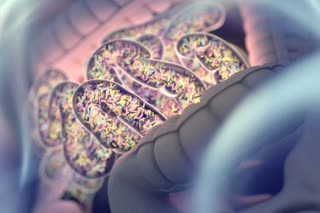
#اخبار_جدید_سلولهای_بنیادی
:beginner: تولید سیستم عصبی گوارشی دارای عملکرد به کمک #سلولهای_بنیادی:small_orange_diamond:اخیرا محققان توانسته اند با موففیت سیستم عصبی گوارشی کاملا دارای عملکردی را با استفاده از سلول های بنیادی و در مدل پیش بالینی تولید کنند. هر چند این مدل هنوز از نظر بالینی در دسترس نیست اما می تواند محققین، پزشکان و جراحان را گامی دیگر به درمان کودکان مبتلا به بیماری Hirschsprung’s نزدیک کند. در کودکان مبتلا به بیماری Hirschsprung’s، این سیستم یا ناقص است یا این که کلا شکل نمی گیرد.
:small_orange_diamond: این سیستم عصبی موسوم به سیستم عصبی انتریک را مغز دوم بدن انسان نیز می نامند زیرا به طور شگفت آوری از سایر بخش های عصبی تفکیک شده است و متفاوت است. این سیستم عصبی انتریک حرکات عضلات روده ای، آزادسازی هورمون و حفظ #سلولهای_بنیادی روده ای که برای حفظ پوشش روده حیاتی هستند را هماهنگ می کند.
:small_orange_diamond: تولید یک مدل پیش بالینی سیستم عصبی انتریک با استفاده از سلول های بنیادی می تواند اطلاعات زیادی را در زمینه این بیماری ارائه دهد و منجر به راهکارهای درمانی شود.:globe_with_meridians: Reference:https://journals.sagepub.com/doi/10.1177/2041731420905701
-
#سؤال
:beginner: آیا سلول های بنیادی بالغین و جنینی دارای توانایی برابر برای ایجاد بافتی به منظور جایگزینی يا پيوند هستند؟:small_orange_diamond: سلول های بنیادی دارای توانایی متفاوت در تخصصی شدن بسمت سلول ها و بافت های خاص هستند .شواهد حاکی از این است که ظرفیت سلول های بنیادی بالغ در ایجاد بافت های متفاوت محدودتر از سلول های بنیادی جنینی است.
:small_orange_diamond: یک سلول بنیادی جنینی سلول های تخصص یافته ای که دارای سه لایه جنینی هستند را میتواند تولید کند و این در حالی است که تا کنون ثابت نشده است که سلول بنیادی بالغ نیز میتواند بافتی را ایجاد کند که شامل هر سه لایه باشد ، بنابراین توانایی ظرفیت تولید بافت و پرتوانی در سلول های بنیادی جنینی و بالغ برابر نیست. -

سلول های بنیادی مشتق از چربی-١:small_orange_diamond: تحقیقات در زمینه سلول های بنیادی چربی در سال های اخیر علی رغم وجود موانع بسیار در اثبات کارائی و سلامت این سلول ها، ویژگی های منحصر به فرد این سلول ها را در جراحی های زیبائی و ترمیمی اثبات کرده است.
:small_blue_diamond:این سلول ها با داشتن جمعیت بزرگی از سلول های مزانشیمی چندتوان در کارآزمائی های بالینی متعدد و با اهداف درمانی متفاوت مورد استفاده قرار گرفته اند.
:small_orange_diamond: تا سال 2012 بیشترین تعداد کارآزمائی بالینی در استفاده از سلول های استرومال مشتق از چربی در قاره ی اروپا و متعلق به کشورهای ایتالیا، انگلیس،استرالیا،آلمان و دانمارک و پس از آن مربوط به آسیا و کشور کره بوده است.
:globe_with_meridians: :round_pushpin:Reference:
Arthur A, Zannettino A, Gronthos S. The therapeutic applications of multipotential mesenchymal/stromal stem cells in skeletal tissue repair. Journal of Cell Physiol, 2012; 218:237-45. -
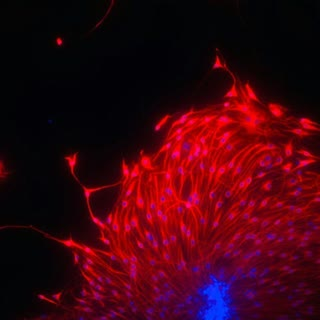
سلول هاي بنيادي مشتق از چربي-۲ :x:شواهد نشان می دهد: :point_down::point_down::point_down::small_blue_diamond:استفاده از سلولهای بنیادی مشتق از چربی در درمان بیماریها، ترمیم و بهبودی بافتها با موفقیت همراه بوده است و استفاده از این سلول ها در زمینه های مختلفی از قبیل ترمیم تاندونها و مفاصل ، بیماریهای قلبی ، بیماریهای عروقی و ضایعات پوستی در حال مطالعه و بهره برداری می باشد.
:small_orange_diamond: در میان ضایعات پوستی یکی از شکایات شایع چین و چروک بوده که از علایم اصلی افت کیفیت پوست و کهولت سن می باشد و از همین رو تقاضای بسیار بالایی برای دریافت درمانهای جدید ، کم عارضه ، سازگار با بدن انسان و ماندگار تر نسبت به درمان های متداول وجود دارد.
:small_blue_diamond:سلول های بنیادی مشتق از چربی از جمله سلول های پرکاربرد در فازهای مختلف کارآزمایی بالینی برای رفع چین وچروک ضایعات پوستی است. -
https://www.aparat.com/v/nfxZm
رویانتان،رویان باد!
دانش-آموزان-آلاء -
https://www.aparat.com/v/HwTSk
چی بودیم،چی شدیم! -
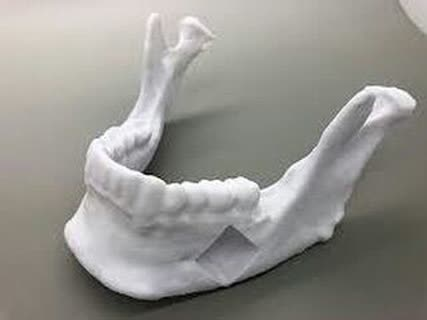
استفاده از فناوری پرینت سه بعدی برای تولید بافت استخوانی
:small_orange_diamond:پرینت زیستی یک رویکرد نوظهور در تولید زیست موادی مانند هیدروژل است که آن ها را سلول و فاکتورهای رشد ترکیب می کند و از این مخلوط برای تولید ساختارهای شبه بافتی که بافت های طبیعی را تقلید می کنند، استفاده می کند. یکی از کاربردهای این فناوری می تواند طراحی و تولید گرافت های استخوانی با توجه به نیاز فرد باشد، به طوری که بتواند ناحیه آسیب دیده را به خوبی پوشش دهد. پرینت زیستی نیازمند زیست موادی است که بتوانند حامل یا ناقل سلول ها باشد، به خوبی قابل پرینت کردن باشند و بتوانند یک ریز محیط مناسب را برای سلول ها فراهم آورند. اما متاسفانه جوهرهای زیستی موجود از زیست سازگاری، قابلیت پرینت، ثبات ساختاری و عملکردهای مناسب بافتی لازم برخوردار نیستند و به همین دلیل استفاده از آن ها در پیش بالین و بالین با مشکل مواجه است. در پژوهشی جدید، محققان یک جوهر زیستی موسوم به جوهر زیستی در هم تنیدگی یونی-کووالانی مهندسی شده جدید (Nanoengineered Ionic-Covalent Entanglement (NICE)) را تولید کرده اند.
:small_orange_diamond:جوهر زیستی NICE ترکیبی از دو فناوری است که به همراه هم موجب تقویت موثرتر این جوهر و تولید ساختارهای قوی تری می شوند. این جوهر زیستی اجازه تولید داربست های قوی می دهد که می توانند در مقیاس مورد نظر و با یک ساختار قابل تحمل برای سلول ها تولید شوند. بارگیری #سلولهای_بنیادی درون این جوهر زیستی برای تولید بافت استخوانی منجر به تولید بافت استخوانی سه بعدی شد که ساختار بافت اسفنجی موجود در استخوان مهره ها را تداعی می کنند. محققین بر این باورند که استفاده از این جوهر زیستی در تولید داربست های استخوانی و بافت های استخوانی می تواند یک رویکرد درمانی موثر برای مشکلات ارتوپدی در آینده ای نزدیک باشد.
:globe_with_meridians: Reference:https://pubs.acs.org/doi/10.1021/acsami.9b19037
-

ساخت نوعی زخم پوش نانوفیبری با قابلیت ترمیمی و آنتی باکتریال
:small_orange_diamond: برخی از مطالعات نشان میدهند که نوعی عسل میتواند به افزایش تولید گلبولهای سفید خون که وظیفه مبارزه با عفونتها و التیام زخمها را بر عهده دارند کمک کند. این عسل در درمان زخمها و ترمیم بافتهای مرده پوست کارایی زیادی دارد بهطوریکه در بعضی از بیمارستانها و مراکز درمانی تا حد زیادی جایگزین آنتی بیوتیکها شدهاست؛ و جهت درمان زخم و مداوای زخم بستر و سوختگیهای عمیق، همچنین جوانسازی سلولهای پوست از این عسل استفاده میشود.
:small_orange_diamond: عسل مانوکا حاوی ترکیبات زیست فعال زیادی از جمله پراکسید هیدروژن، متیل گلیوکسال(MGO)، پلی فنول ها، سوکروز و مالتوز است که به فرایند بهبودی کمک می کنند. همه انواع عسل ها حاوی پراکسید هستند که در تماس با باکتری آن را می کشند و در این میان به سلول های انسانی نیز آسیب می رسانند. آن چه پراکسید هیدروژن را در نمونه عسل خاص می سازد، این است که به آهستگی تولید می شود و به آهستگی رشد باکتری را در متوقف می کند و این در حالی است که اثر ملایمی روی سلول های انسانی دارد. در این میان عسل مانوکا دارای MGO نیز می باشد که رشد باکتریایی را از طریق محدود کردن قابلیت تحرک سوش های باکتریایی مهار می کند. حتی قند موجود در این عسل یعنی سوکروز و مالتوز نیز می توانند منبع مستقیمی برای تامین انرژی سلول ها روی سطح زخم باشد. در پژوهشی جدید، محققین توانسته اند زخم پوش جدیدی را تولید کنند که در آن از عسل مانوکا نیز برای تولید نانوفیبرهای سلولز استات الکتروریسی شده استفاده شده است.
:small_orange_diamond: سلولز استات یک پلیمر آبدوست و زیست تخریب پذیر با قدرت کشسانی بالا است که می توان از آن برای زخم پوش استفاده کرد. استفاده از این نانوفیبرهای حاوی عسل مانوکا به عنوان شبکه های نانوفیبری برای پوشش زخم، فعالیت آنتی میکروبی بالایی را علیه باکتری های گرم مثبت و منفی نشان داد. این زخم پوش ها قابلیت تنفس مناسبی دارند و موجب افزایش بهبودی زخم می شوند.
Reference:https://www.sciencedirect.com/science/article/pii/S0141813020328245?via=ihub
-
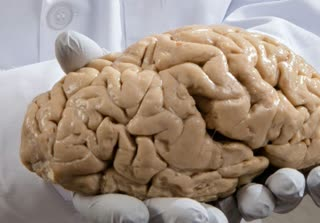
ساخت مدلی سه بعدی از مغز انسان
:small_orange_diamond: درک درست فرآیندهای درگیر در تکوین ، سازماندهی و اختلال در عملکرد مغز انسان دشوار بوده است زیرا ما نمی توانیم مستقیماً عملکرد یا عملکرد سلولهای مغزی انسان را بررسی و یا دستکاری کنیم. برای فائق آمدن بر این چالش، محققان راهی برای ایجاد ساختارهای بافتی سه بعدی خود سازمان یابنده از #سلولهای_بنیادی پرتوان مشتق از بیماران ایجاد کرده اند.
:small_blue_diamond: محققان نشان داده اند که این اسفروئیدهای اختصاصی مناطق مغزی می توانند سال ها حفظ شوند و همین امر اجازه مطالعه مراحل پیشرفته بلوغ و عملکرد مغز را می دهند. این اسفروئیدها می توانند تکوین جنینی مناطق مختلفی از مغز مانند قشر مغز را به خوبی شبیه سازی کنند. در این مطالعه محققین نشان داده اند که اسفروئیدهای مختص هر منطقه از مغز می توانند در کنار یکدیگر قرار گرفته با یکدیگر ادغام شوند و ساختارهای مغزی موسوم به brain assembloids را تولید کنند.
:small_orange_diamond: این ساختارها می توانند برای بررسی فرایندهای تکوین مغزی که پیش از این مطالعه آن ها سخت بود مانند مهاجرت سلولی، ارتباطات سلولی طولانی مدت و تشکیل مدارهای عصبی مورد استفاده قرار گیرند. از این brain assembloids می تواند برای مطالعه بیماری های عصبی روانی مانند اوتیسم، سندرم تیموتی و ... که مکانیسم های مولکولی و سلولی آن ها به خوبی شناخته نشده است استفاده کرد.
:globe_with_meridians: Reference:https://medicalxpress.com/news/2020-04-d-tissue-unprecedented-insight-human.html
-
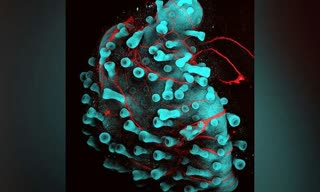
تولید ارگانوئیدهای پوستی حاوی مو به کمک سلول های بنیادی
:small_orange_diamond:ارگانوئیدهای، گروه های سلولی کوچک رشد یافته و سازمان یافته در آزمایشگاه هستند که برای مدل سازی اندام های واقعی طراحی می شوند و در مطالعه ای جدید محققین سعی در ایجاد ارگانوئیدهای پوست داشته اند. آن ها توانسته اند برای اولین بار ارگانوئیدهای پوست انسانی را از سلول های بنیادی پرتوان تولید کنند و این در حالی است که این پوست ها حتی ویژگی مانند داشتن مو را نیز دارا بودند.
:small_orange_diamond: در این پژوهش محققان توانسته اند با شبیه سازی مراحل تکوینی اولیه پوست انسان، ارگانوئیدهای پوستی را تولید کنند که دارای ضمائم پوستی از جمله فولیکول های مو هستند. دسترسی به این ارگانوئیدهای پوستی می تواند زمینه را برای درک بهتر تکوین پوست و مو هموار کنند و در مطالعات مربوط به ریزش مو کمک کننده باشد.
:globe_with_meridians: Reference:https://www.nature.com/articles/s41586-020-2352-3
-

بیماری ALS و سلول درمانی :point_down:
:red_circle: بیماری ALS یا اسکلروز جانبی آمیوتروفیک ، Amyotrophic lateral sclerosis یا بیماری لوگهریگ یک بیماری نورونهای حرکتی یا MND یا Motor Neuron Disease است که موجب تخریب پیشرونده و غیرقابل ترمیم در دستگاه عصبی مرکزی (مغز و نخاع) و دستگاه عصبی محیطی میشود.
:small_orange_diamond:اسکلروز جانبی آمیوتروفیک شایعترین بیماری نورونهای حرکتی (MND) میباشد که در حقیقت در ALS نشانههای فلج مرکزی و محیطی تواماً ایجاد میشود.
:small_blue_diamond: بروز بیماری دونفر در هر صد هزار نفر میباشد و اغلب افراد بین چهل تا شصت سال را درگیر میسازد. بیماری ماهیت پیشرونده دارد و اغلب بیماران بعد از دو تا پنج سال فوت میکنند ولی گاه دورههای توقف بیماری وجود دارد؛ که باعث میشود ۱۰ درصد از بیماران تا ۱۰ سال زنده بمانند. از آنجایی که این بیماری تنها به اعصاب حرکتی آسیب میرساند، بنابراین هیچ اختلالی در بینایی، بساوایی، شنوایی، چشایی و بویایی فرد به وجود نخواهد آمد و جالب این که اعصاب حرکتی مؤثر در حرکت چشمها و مثانه برای مدتهای طولانی از حمله عامل بیماری مصون خواهند
ماند.
:small_orange_diamond:Riluzole
تنها داروی مورد تائید سازمان غذا و داروی آمریکا برای کنترل و بهبود شرایط بیماران مبتلا به این بیماری است.:small_blue_diamond: درمان های رایج و مورد بررسی برای بیماری اسکلروز جانبی آمیوتروفیک:
:white_check_mark: درمان با استفاده از آنتاگونیست های گلوتامات که موفق ترین راهکار درمانی در کارآزمائی های بالینی
:white_check_mark: آنتی اکسیدان تراپی
:white_check_mark: راهکارهای ایمنوتراپي
:white_check_mark: استفاده از سلول های بنیادی مزانشیمی مشتق از مغز استخوان
:white_check_mark: استفاده از سلول های بنیادی جنینی و پرتوان القائی:small_orange_diamond: ۳۷ کارآزمائی بالینی از درمان این بیماری با استفاده از سلول های بنیادی مختلف در پایگاه های جستجو کارآزمائی بالینی ثبت شده است که از این میان استفاده از سلول های بنیادی مزانشیمی مشتق از مغز استخوان در فاز 1 و 2 کارآزمائی بالینی در 70 درصد از بیماران بهبود شرایط زندگی و کاهش اثرات پیش رونده را نشان داده است.
:globe_with_meridians: Reference:
Serhiy Forostyak, et al., Neuroprotective Potential of Cell-Based Therapies in ALS: From Bench to Bedside. Front Neurosci. 2017; 11: 591. -

استفاده از فناوری پرینت سه بعدی برای تولید بافت استخوانی
:small_orange_diamond:پرینت زیستی یک رویکرد نوظهور در تولید زیست موادی مانند هیدروژل است که آن ها را سلول و فاکتورهای رشد ترکیب می کند و از این مخلوط برای تولید ساختارهای شبه بافتی که بافت های طبیعی را تقلید می کنند، استفاده می کند. یکی از کاربردهای این فناوری می تواند طراحی و تولید گرافت های استخوانی با توجه به نیاز فرد باشد، به طوری که بتواند ناحیه آسیب دیده را به خوبی پوشش دهد. پرینت زیستی نیازمند زیست موادی است که بتوانند حامل یا ناقل سلول ها باشد، به خوبی قابل پرینت کردن باشند و بتوانند یک ریز محیط مناسب را برای سلول ها فراهم آورند. اما متاسفانه جوهرهای زیستی موجود از زیست سازگاری، قابلیت پرینت، ثبات ساختاری و عملکردهای مناسب بافتی لازم برخوردار نیستند و به همین دلیل استفاده از آن ها در پیش بالین و بالین با مشکل مواجه است. در پژوهشی جدید، محققان یک جوهر زیستی موسوم به جوهر زیستی در هم تنیدگی یونی-کووالانی مهندسی شده جدید (Nanoengineered Ionic-Covalent Entanglement (NICE)) را تولید کرده اند.
:small_orange_diamond:جوهر زیستی NICE ترکیبی از دو فناوری است که به همراه هم موجب تقویت موثرتر این جوهر و تولید ساختارهای قوی تری می شوند. این جوهر زیستی اجازه تولید داربست های قوی می دهد که می توانند در مقیاس مورد نظر و با یک ساختار قابل تحمل برای سلول ها تولید شوند. بارگیری #سلولهای_بنیادی درون این جوهر زیستی برای تولید بافت استخوانی منجر به تولید بافت استخوانی سه بعدی شد که ساختار بافت اسفنجی موجود در استخوان مهره ها را تداعی می کنند. محققین بر این باورند که استفاده از این جوهر زیستی در تولید داربست های استخوانی و بافت های استخوانی می تواند یک رویکرد درمانی موثر برای مشکلات ارتوپدی در آینده ای نزدیک باشد.
:globe_with_meridians: Reference:https://pubs.acs.org/doi/10.1021/acsami.9b19037
Bio یکی از سایت های معتبر و پرطرفدار پزشکی که بروزترین مطالب رو داره سایت medicalpress هستش..
واقعا سایت خیلی خوبیه..!:growing_heart:
پیشنهاد میکنم حتما از مطالبش بچها استفاده کنن نه تنها تجربیا بلکه تمام دانش-آموزان-آلاء
میتونین از گوگل ترنسلیت هم برای ترجمه متون استفاده کنین..! -
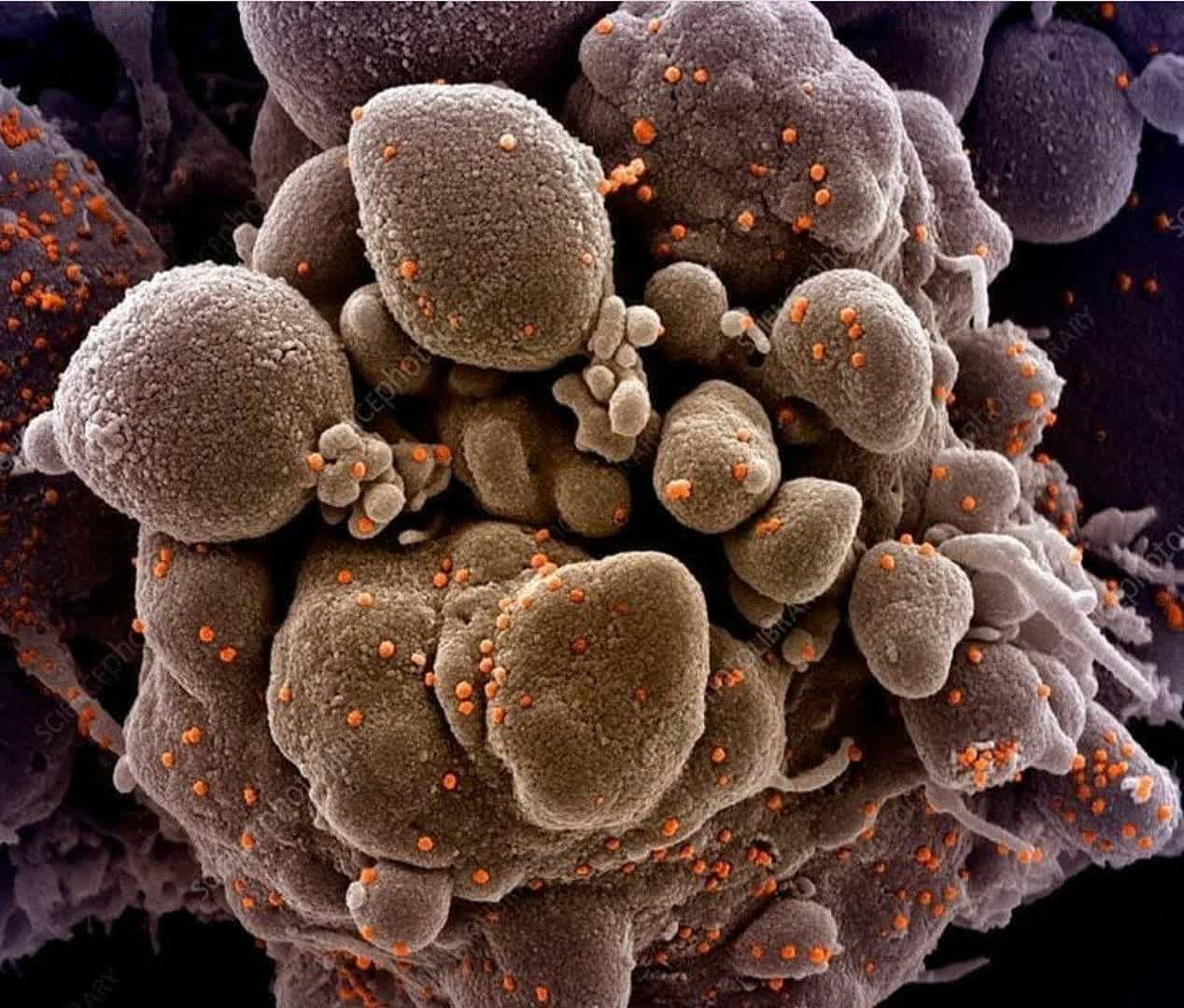
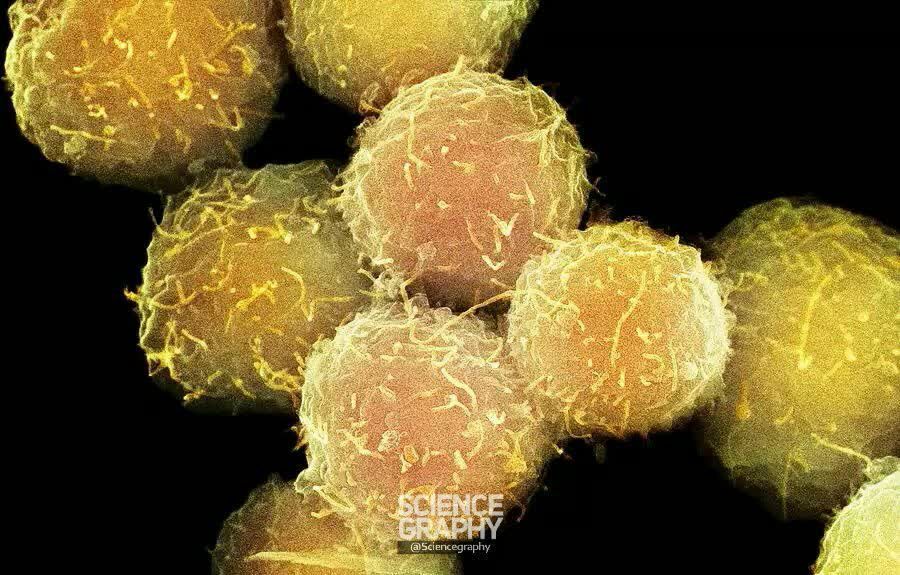
#تصاویر_میکروسکوپی
:beginner:سلول های آلوده به #کرونا
کوچیکا خود ویروس هستن!
دانش-آموزان-آلاء -
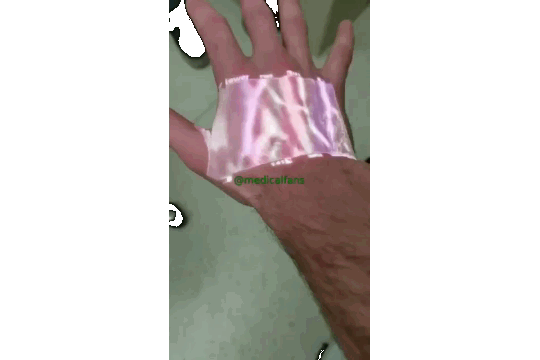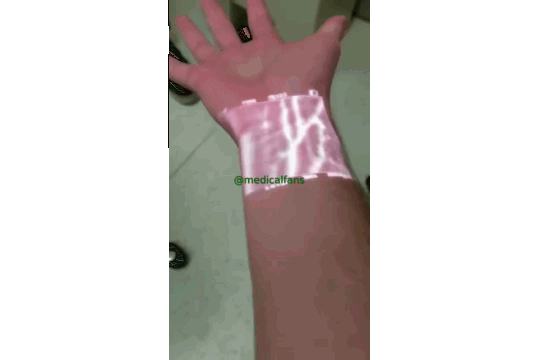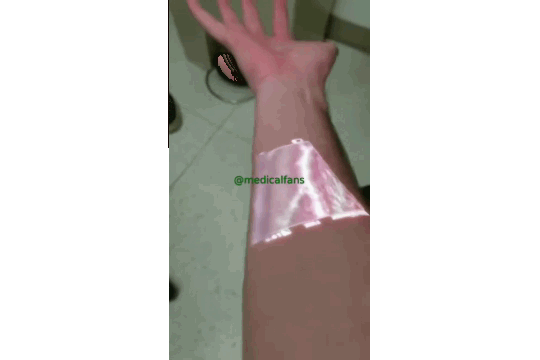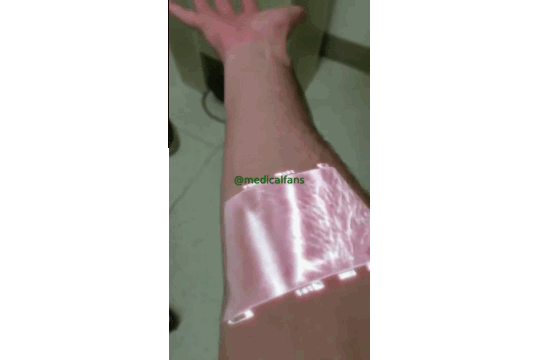
تصویری که فناوری نوین تصویربرداری از رگ را نشان می دهد.
:pushpin:این فناوری از نور مادون قرمز استفاده می کند ، که توسط خون جذب می شود اما از بافت های اطراف منعکس می شود تا رگ ها تا عمق 15 میلی متر پیدا می کند، و سپس نتایج را بر روی پوست نمایش می دهد.
-
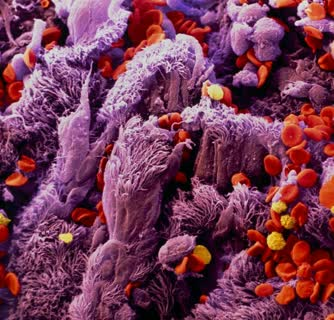
#تصاویر_میکروسکوپی
#سرطان
#ریه:microscope: در تصویر بالا عکس میکروسکوپ الکترونی اپیتلیوم نایژه ریه انسانی که از سرطان رنج می برد ، مشاهده می شود.
:blue_book: این شایع ترین شکل سرطان ریه است که ناشی از استعمال سیگار است. اپیتلیوم یک غشای مخاطی ایجاد می کند که مجاری هوایی ریه را می پوشاند. این شامل توده هایی از مژه های مو مانند (که در اینجا دیده می شود) و سلول های جامی که ترشح مخاط را دارند.
:closed_book: به علت سرطان ، رشد سلول های بی نظم باعث شده این سطح ناهموار شود. سلول های خونی (قرمز) نیز به دلیل خونریزی بیرون آمده اند. رشد سرطانی و سطح ناهموار بدان معنی است که مژه ها ، که بطور معمول برای از بین بردن ذرات به دام افتاده در مخاط ضرب میزنند ، کمتر موثر هستند و راه های هوایی مسدود می شوند.