سلول های بنیادی راهی به آینده
-
#اخبار_جدید_سلولهای_بنیادی
 پیشرفت در مهندسی بافت: پرینت مستقیم بافت های سه بعدی در بدن(2)
پیشرفت در مهندسی بافت: پرینت مستقیم بافت های سه بعدی در بدن(2) این فرمولاسیون به صورت سه بعدی قابل پرینت شدن در دمای فیزیولوژیک است و می تواند به طور بی خطری با استفاده از نور مرئی که بی خطر است کراس لینک شود. به منطور ساخت بافت در بدن، آن ها از یک پرینتر رباتیک سه بعدی استفاده کردند که از طریق یک نازل جوهر زیستی را به صورت برنامه ریزی شده و بسیار دقیق در درون بدن می افشاند. برای چسبندگی بهتر بافت پرینت شده با بافت نرم از پیش موجود، نوک نازل به درون بافت بدن وارد می شود و مواد را تزریق می کند و بدین ترتیب نوعی لنگر برای چسبیدن و متصل ماندن بافت جدید ارائه می کند. چنین توانمندی در مهندسی بافت اجازه انجام رویکردهای کمتر خطرناک و کمتر تهاجمی را برای ترمیم نواقص بافتی یا اندامی می دهد. با استفاده از پرینت های سه بعدی، تولید بافت های سفارشی(با توجه به نیاز بیمار) و کاملا شخصی(با استفاده از حتی سلول های خود فرد) امکان پذیر خواهد بود.
این فرمولاسیون به صورت سه بعدی قابل پرینت شدن در دمای فیزیولوژیک است و می تواند به طور بی خطری با استفاده از نور مرئی که بی خطر است کراس لینک شود. به منطور ساخت بافت در بدن، آن ها از یک پرینتر رباتیک سه بعدی استفاده کردند که از طریق یک نازل جوهر زیستی را به صورت برنامه ریزی شده و بسیار دقیق در درون بدن می افشاند. برای چسبندگی بهتر بافت پرینت شده با بافت نرم از پیش موجود، نوک نازل به درون بافت بدن وارد می شود و مواد را تزریق می کند و بدین ترتیب نوعی لنگر برای چسبیدن و متصل ماندن بافت جدید ارائه می کند. چنین توانمندی در مهندسی بافت اجازه انجام رویکردهای کمتر خطرناک و کمتر تهاجمی را برای ترمیم نواقص بافتی یا اندامی می دهد. با استفاده از پرینت های سه بعدی، تولید بافت های سفارشی(با توجه به نیاز بیمار) و کاملا شخصی(با استفاده از حتی سلول های خود فرد) امکان پذیر خواهد بود. Reference:https://medicalxpress.com/news/2020-06-d-tissues-body.html
Reference:https://medicalxpress.com/news/2020-06-d-tissues-body.html -

#اخبار_جدید_سلولهای_بنیادی
 استفاده از خاصیت ترمیمی بندناف برای کاهش اسکار ناشی از جراحی بیماری spina bifida(1)
استفاده از خاصیت ترمیمی بندناف برای کاهش اسکار ناشی از جراحی بیماری spina bifida(1) بیماری spina bifida، شرایطی است که به موجب آن پوشش مغز، نخاع یا مننژ به طور کامل تکوین نمی یابد. این نقص می تواند منجر به ناتوانی یا فلجی، عملکرد نامناسب سیستم ادراری و روده و اختلالات ذهنی شود. محققین از یک پچ یا تکه بافتی متشکل از لایه خارجی بند ناف نوزادان سالم برای درمان spina bifida استفاده کرده اند.
بیماری spina bifida، شرایطی است که به موجب آن پوشش مغز، نخاع یا مننژ به طور کامل تکوین نمی یابد. این نقص می تواند منجر به ناتوانی یا فلجی، عملکرد نامناسب سیستم ادراری و روده و اختلالات ذهنی شود. محققین از یک پچ یا تکه بافتی متشکل از لایه خارجی بند ناف نوزادان سالم برای درمان spina bifida استفاده کرده اند. -

#اخبار_جدید_سلولهای_بنیادی
 استفاده از خاصیت ترمیمی بندناف برای کاهش اسکار ناشی از جراحی بیماری spina bifida(2)
استفاده از خاصیت ترمیمی بندناف برای کاهش اسکار ناشی از جراحی بیماری spina bifida(2) مشخصه اصلی این تکه های مشتق از بند ناف این است که بند ناف حاوی مواد طبیعی خاصی است که دارای ویژگی های بازسازی کنندگی هستند. این پچ ها یا تکه های مشتق از بند ناف اجازه می دهند که بافت موضعی ناحیه تحت تاثیر spina bifida به جای این که بوسیله تشکیل اسکار به صورت نامطلوب ترمیم شود، به نحو مطلوب تری بهبود یابد و فرد نیازمند جراحی بیشتر برای برداشتن بافت اسکار در ناحیه آسیب نشود.
مشخصه اصلی این تکه های مشتق از بند ناف این است که بند ناف حاوی مواد طبیعی خاصی است که دارای ویژگی های بازسازی کنندگی هستند. این پچ ها یا تکه های مشتق از بند ناف اجازه می دهند که بافت موضعی ناحیه تحت تاثیر spina bifida به جای این که بوسیله تشکیل اسکار به صورت نامطلوب ترمیم شود، به نحو مطلوب تری بهبود یابد و فرد نیازمند جراحی بیشتر برای برداشتن بافت اسکار در ناحیه آسیب نشود. -

ثبت نام در:https://www.royan-edu.ir/the-wonders-of-the-giant-squid/
Zaraa @دختر-بهار ZDM Bad Fighter Mono
@jahad-20 @Dr-Rashidi @mahta-kamali HADAF MAN @Z-H-Z zzz r
mj323 @m-hmt @Miss-Joker
Mbf
دانش-آموزان-آلاء -
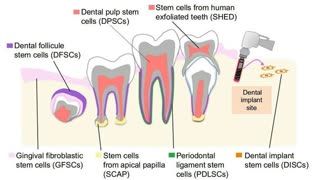
 انواع سلول های بنیادی قابل استخراج از بافت دندان و بافت های اطراف آن و منابع آن ها
انواع سلول های بنیادی قابل استخراج از بافت دندان و بافت های اطراف آن و منابع آن ها سلول های بنیادی مزانشیمی قابل استخراج از بخش داخلی پالپ دندان های مولار(رنگ قرمز
سلول های بنیادی مزانشیمی قابل استخراج از بخش داخلی پالپ دندان های مولار(رنگ قرمز
 ) تحت نام DPSCs ،
) تحت نام DPSCs ، از پالپ دندان های شیری (رنگ قرمز
از پالپ دندان های شیری (رنگ قرمز
 ) تحت نام SHED که نخستین بار در سال 2003 توسط پرفسورSongtao Shi کشف شد ،
) تحت نام SHED که نخستین بار در سال 2003 توسط پرفسورSongtao Shi کشف شد ، از بخش آپیکال پاپیلای دندان (رنگ زرد
از بخش آپیکال پاپیلای دندان (رنگ زرد
 ) تحت نام SCAP
) تحت نام SCAP از بخش بافت های حمایت کننده دنان و لثه ی اطراف دندان ها که شامل سلول های بنیادی مزانشیمی مستخرج از فولیکول دندان تحت نام DFSCs (رنگ بنفش
از بخش بافت های حمایت کننده دنان و لثه ی اطراف دندان ها که شامل سلول های بنیادی مزانشیمی مستخرج از فولیکول دندان تحت نام DFSCs (رنگ بنفش
 )،
)، سلول های بنیادی مزانشیمی مستخرج از لیگامنت های اطراف دندان تحت نام PDLSCs (رنگ سبز
سلول های بنیادی مزانشیمی مستخرج از لیگامنت های اطراف دندان تحت نام PDLSCs (رنگ سبز
 )
) رنگ صورتی و نارنجی
رنگ صورتی و نارنجی 
 که نشان دهنده سلول های استخراج شده از بافت لثه و سلول های مستخرج از بافت های خارج شده به منظور انجام ایمپلنت های دندانی است.
که نشان دهنده سلول های استخراج شده از بافت لثه و سلول های مستخرج از بافت های خارج شده به منظور انجام ایمپلنت های دندانی است. -
ساخت مدلی سه بعدی از مغز انسان درک درست فرآیندهای درگیر در تکوین ، سازماندهی و اختلال در عملکرد مغز انسان دشوار بوده است زیرا ما نمی توانیم مستقیماً عملکرد یا عملکرد سلولهای مغزی انسان را بررسی و یا دستکاری کنیم. برای فائق آمدن بر این چالش، محققان راهی برای ایجاد ساختارهای بافتی سه بعدی خود سازمان یابنده از #سلولهای_بنیادی پرتوان مشتق از بیماران ایجاد کرده اند.
درک درست فرآیندهای درگیر در تکوین ، سازماندهی و اختلال در عملکرد مغز انسان دشوار بوده است زیرا ما نمی توانیم مستقیماً عملکرد یا عملکرد سلولهای مغزی انسان را بررسی و یا دستکاری کنیم. برای فائق آمدن بر این چالش، محققان راهی برای ایجاد ساختارهای بافتی سه بعدی خود سازمان یابنده از #سلولهای_بنیادی پرتوان مشتق از بیماران ایجاد کرده اند. محققان نشان داده اند که این اسفروئیدهای اختصاصی مناطق مغزی می توانند سال ها حفظ شوند و همین امر اجازه مطالعه مراحل پیشرفته بلوغ و عملکرد مغز را می دهند. این اسفروئیدها می توانند تکوین جنینی مناطق مختلفی از مغز مانند قشر مغز را به خوبی شبیه سازی کنند. در این مطالعه محققین نشان داده اند که اسفروئیدهای مختص هر منطقه از مغز می توانند در کنار یکدیگر قرار گرفته با یکدیگر ادغام شوند و ساختارهای مغزی موسوم به brain assembloids را تولید کنند.
محققان نشان داده اند که این اسفروئیدهای اختصاصی مناطق مغزی می توانند سال ها حفظ شوند و همین امر اجازه مطالعه مراحل پیشرفته بلوغ و عملکرد مغز را می دهند. این اسفروئیدها می توانند تکوین جنینی مناطق مختلفی از مغز مانند قشر مغز را به خوبی شبیه سازی کنند. در این مطالعه محققین نشان داده اند که اسفروئیدهای مختص هر منطقه از مغز می توانند در کنار یکدیگر قرار گرفته با یکدیگر ادغام شوند و ساختارهای مغزی موسوم به brain assembloids را تولید کنند. این ساختارها می توانند برای بررسی فرایندهای تکوین مغزی که پیش از این مطالعه آن ها سخت بود مانند مهاجرت سلولی، ارتباطات سلولی طولانی مدت و تشکیل مدارهای عصبی مورد استفاده قرار گیرند. از این brain assembloids می تواند برای مطالعه بیماری های عصبی روانی مانند اوتیسم، سندرم تیموتی و ... که مکانیسم های مولکولی و سلولی آن ها به خوبی شناخته نشده است استفاده کرد.
این ساختارها می توانند برای بررسی فرایندهای تکوین مغزی که پیش از این مطالعه آن ها سخت بود مانند مهاجرت سلولی، ارتباطات سلولی طولانی مدت و تشکیل مدارهای عصبی مورد استفاده قرار گیرند. از این brain assembloids می تواند برای مطالعه بیماری های عصبی روانی مانند اوتیسم، سندرم تیموتی و ... که مکانیسم های مولکولی و سلولی آن ها به خوبی شناخته نشده است استفاده کرد. Reference:https://medicalxpress.com/news/2020-04-d-tissue-unprecedented-insight-human.html
Reference:https://medicalxpress.com/news/2020-04-d-tissue-unprecedented-insight-human.html -
#اخبار_جدید_سلولهای_بنیادی
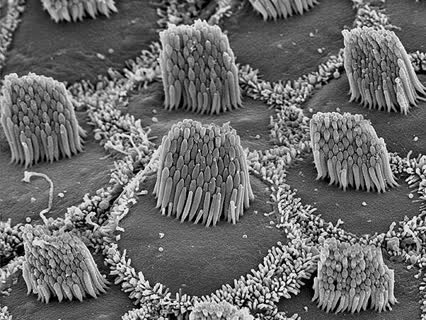
 تولید سلول های مرتبط با شنوایی به کمک سلول های بنیادی القایی(1)
تولید سلول های مرتبط با شنوایی به کمک سلول های بنیادی القایی(1) در مطالعه جدید، محققین از رویکرد بازبرنامه ریزی مستقیم برای تولید سلول های حسی موسوم به سلول های مویی گوش داخلی استفاده کرده اند. در این رویکرد محققین با موفقیت سه نوع مختلف از سلول های موش را به سلول های مویی حسی(iHCs) بازبرنامه ریزی کردند. دو نوع سلول اول مورد استفاده در این رویکرد، ورژن های جنینی و بالغ سلول های بافت پیوندی موسوم به فیبروبلاست و نوع سوم سلول، نوعی از سلول های گوش داخلی به نام سلول پشتیبان بوده است.
در مطالعه جدید، محققین از رویکرد بازبرنامه ریزی مستقیم برای تولید سلول های حسی موسوم به سلول های مویی گوش داخلی استفاده کرده اند. در این رویکرد محققین با موفقیت سه نوع مختلف از سلول های موش را به سلول های مویی حسی(iHCs) بازبرنامه ریزی کردند. دو نوع سلول اول مورد استفاده در این رویکرد، ورژن های جنینی و بالغ سلول های بافت پیوندی موسوم به فیبروبلاست و نوع سوم سلول، نوعی از سلول های گوش داخلی به نام سلول پشتیبان بوده است. -
#اخبار_جدید_سلولهای_بنیادی
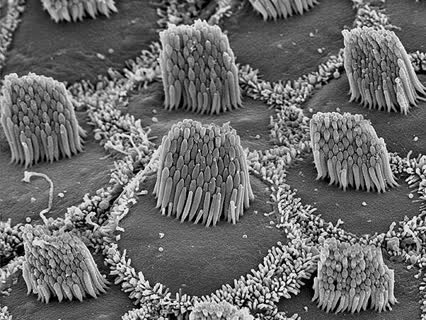
 تولید سلول های مرتبط با شنوایی به کمک سلول های بنیادی القایی(2)
تولید سلول های مرتبط با شنوایی به کمک سلول های بنیادی القایی(2) برای بازبرنامه ریزی این سلول ها، محققان فیبروبلاست ها و سلول های پشتیبان را در معرض کوکتیلی از چهار فاکتور رونویسی قرار دادند. این چهار فاکتور رونویسی حاصل غربالگری ترکیب 16 فاکتور رونویسی دخیل در تکوین سلول های مویی شنوایی موش بود. بدنبال بازبرنامه ریزی، سلول های iHC تولید شد که از نظر ساختار، الکتروفیزیولوژی و فعالیت ژنتیکی شبیه سلول های حسی مویی طبیعی بودند. این سلول ها دارای ویژگی های دیگری مانند آسیب پذیری به آنتی بیوتیک های شناخته شده عامل ناشنوایی نیز بودند. به عقیده محققین این سلول های حسی مویی یا iHC پتانسیل تسریع تحقیقات روی ناشنوایی را دارا هستند و می توان از آن ها در مطالعات تکوینی، غربالگری های دارویی و تست های سمیت شناسی روی سلول های گوش استفاده کرد.
برای بازبرنامه ریزی این سلول ها، محققان فیبروبلاست ها و سلول های پشتیبان را در معرض کوکتیلی از چهار فاکتور رونویسی قرار دادند. این چهار فاکتور رونویسی حاصل غربالگری ترکیب 16 فاکتور رونویسی دخیل در تکوین سلول های مویی شنوایی موش بود. بدنبال بازبرنامه ریزی، سلول های iHC تولید شد که از نظر ساختار، الکتروفیزیولوژی و فعالیت ژنتیکی شبیه سلول های حسی مویی طبیعی بودند. این سلول ها دارای ویژگی های دیگری مانند آسیب پذیری به آنتی بیوتیک های شناخته شده عامل ناشنوایی نیز بودند. به عقیده محققین این سلول های حسی مویی یا iHC پتانسیل تسریع تحقیقات روی ناشنوایی را دارا هستند و می توان از آن ها در مطالعات تکوینی، غربالگری های دارویی و تست های سمیت شناسی روی سلول های گوش استفاده کرد. Reference: https://elifesciences.org/articles/55249
Reference: https://elifesciences.org/articles/55249 -
-
#اخبار_جدید_سلولهای_بنیادی
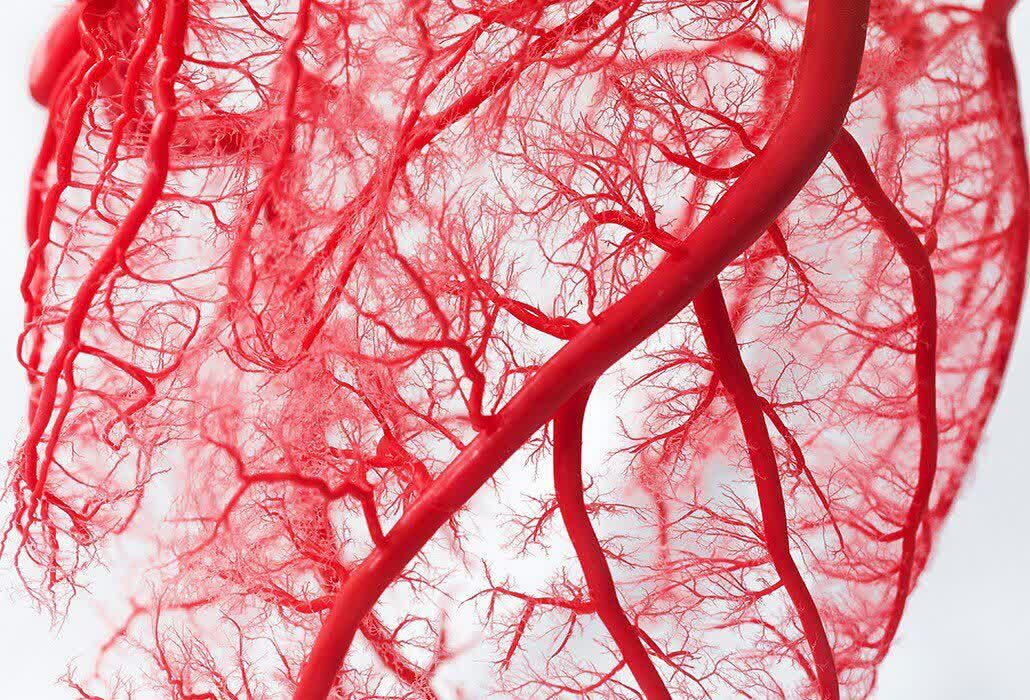
 کشف محققان در رزمینه ارتباط بین سلول های عروق خونی و سلول های عصبی
کشف محققان در رزمینه ارتباط بین سلول های عروق خونی و سلول های عصبی پژوهشگران با استفاده از ویدئوهای لحظه ای و زنده (real-time video) کشف کرده اند که هر دوی نورون ها و سلول های عروق خونی، زوائد دینامیکی را به سوی یکدیگر می فرستند و به موجب آن ها با یکدیگر ارتباطات برقرار می کنند.این زوائد موسوم به فیلوپودیای پیام رسان یا cytonemes هستند و دارای گیرنده یا لیگاندهایی در رأس شان هستند که به آن ها اجازه فرستادن پیام را می دهد. اما این مطالعه جدید نشان داد که این امر نیازمند یک مکانیسم پیام رسان دقیق از نظر فضایی و زمانی است.
پژوهشگران با استفاده از ویدئوهای لحظه ای و زنده (real-time video) کشف کرده اند که هر دوی نورون ها و سلول های عروق خونی، زوائد دینامیکی را به سوی یکدیگر می فرستند و به موجب آن ها با یکدیگر ارتباطات برقرار می کنند.این زوائد موسوم به فیلوپودیای پیام رسان یا cytonemes هستند و دارای گیرنده یا لیگاندهایی در رأس شان هستند که به آن ها اجازه فرستادن پیام را می دهد. اما این مطالعه جدید نشان داد که این امر نیازمند یک مکانیسم پیام رسان دقیق از نظر فضایی و زمانی است. این ارتباط بین نورون و عروق خونی اجازه می دهد که برخی از پیش سازهای نورون ها به صورت خفته یا خاموش باقی بمانند و یا برعکس منبع سلول های بنیادی عصبی، فعال شوند. پیش سازهای عصبی در ابتدا در یک محیط هیپوکسی یا کم اکسیژن قرار دارند که موجب می شود آن ها به صورت تکثیر شونده باقی بمانند.
این ارتباط بین نورون و عروق خونی اجازه می دهد که برخی از پیش سازهای نورون ها به صورت خفته یا خاموش باقی بمانند و یا برعکس منبع سلول های بنیادی عصبی، فعال شوند. پیش سازهای عصبی در ابتدا در یک محیط هیپوکسی یا کم اکسیژن قرار دارند که موجب می شود آن ها به صورت تکثیر شونده باقی بمانند. زمانی که در حین تکوین عروقی خونی با آن ها ارتباط برقرار می کند، اکسیژن بوسیله عروق خونی به محیط اضافه می شود و به عنوان یک سیگنال برای تمایز پیش سازهای عصبی به نورون ها می شود. این مطالعه نشان می دهد که طی تکوین سیستم عصبی محیطی، تشکیل نورون های جدید و حفظ سلول های بنیادی بسیار به سیگنال های دریافتی عروق خونی بستگی دارد. این یافته می تواند به درک ارتباط بین ناشنوایی و بیماری های قلبی عروقی و هم چنین بهبود پروتکل ها برای تمایز آزمایشگاهی نورون ها برای درمان های بازسازی کننده کمک می کند.
زمانی که در حین تکوین عروقی خونی با آن ها ارتباط برقرار می کند، اکسیژن بوسیله عروق خونی به محیط اضافه می شود و به عنوان یک سیگنال برای تمایز پیش سازهای عصبی به نورون ها می شود. این مطالعه نشان می دهد که طی تکوین سیستم عصبی محیطی، تشکیل نورون های جدید و حفظ سلول های بنیادی بسیار به سیگنال های دریافتی عروق خونی بستگی دارد. این یافته می تواند به درک ارتباط بین ناشنوایی و بیماری های قلبی عروقی و هم چنین بهبود پروتکل ها برای تمایز آزمایشگاهی نورون ها برای درمان های بازسازی کننده کمک می کند. -
#اخبار_جدید_سلولهای_بنیادی
 استفاده از فناوری ارگانوئید در غربالگری داروهای مغزی
استفاده از فناوری ارگانوئید در غربالگری داروهای مغزی در حال حاضر بیشتر مطالعات سمیت شناسی(سمیت عصبی، قلبی و ...) روی مدل های جانوری صورت می گیرد که فرایندی گران و زمان بر است و لزوما پاتوفیزیولوژی انسانی را شبیه سازی نمی کند. ایجاد مدل های برون تنی متناسب انسانی می تواند وقایع کلیدی تکوین مغز انسان را پوشش دهد و بسیاری از این چالش ها را برطرف سازد.در مطالعه ای ، محققین به ارزیابی اثرات داروی ضد افسردگی پاروگزتین روی مدل های مغزی مشتق از سلول های بنیادی پرتوان القایی(brain Spheres) پرداختند. پیش از این استفاده از این دارو به عنوان یکی از SSRIs، اثرات ضد و نقیضی را روی تکوین مغز در جانوران نشان داده بود.
در حال حاضر بیشتر مطالعات سمیت شناسی(سمیت عصبی، قلبی و ...) روی مدل های جانوری صورت می گیرد که فرایندی گران و زمان بر است و لزوما پاتوفیزیولوژی انسانی را شبیه سازی نمی کند. ایجاد مدل های برون تنی متناسب انسانی می تواند وقایع کلیدی تکوین مغز انسان را پوشش دهد و بسیاری از این چالش ها را برطرف سازد.در مطالعه ای ، محققین به ارزیابی اثرات داروی ضد افسردگی پاروگزتین روی مدل های مغزی مشتق از سلول های بنیادی پرتوان القایی(brain Spheres) پرداختند. پیش از این استفاده از این دارو به عنوان یکی از SSRIs، اثرات ضد و نقیضی را روی تکوین مغز در جانوران نشان داده بود. این مطالعه نشان داد که غلظت های درمانی پاروگزتین موجود در خون(20 تا 60 نانوگرم/میلی لیتر) منجر به کاهش 80 درصد بیان مارکرهای سیناپسی، کاهش 60 درصدی فرا رشد نوریتی و کاهش 40 تا 75 درصدی بقای کلی جمعیت های سلولی اولیگودندروسیتی می شود. محققین این مطالعه بر این باورند که قطعا استفاده از داروی پاروگزتین می تواند عوارض جانبی روی تکوین مغز داشته باشد و منجر به ناهنجاری های مغزی شود.
این مطالعه نشان داد که غلظت های درمانی پاروگزتین موجود در خون(20 تا 60 نانوگرم/میلی لیتر) منجر به کاهش 80 درصد بیان مارکرهای سیناپسی، کاهش 60 درصدی فرا رشد نوریتی و کاهش 40 تا 75 درصدی بقای کلی جمعیت های سلولی اولیگودندروسیتی می شود. محققین این مطالعه بر این باورند که قطعا استفاده از داروی پاروگزتین می تواند عوارض جانبی روی تکوین مغز داشته باشد و منجر به ناهنجاری های مغزی شود. Reference:https://www.frontiersin.org/articles/10.3389/fncel.2020.00025/full
Reference:https://www.frontiersin.org/articles/10.3389/fncel.2020.00025/full -

#اخبار_جدید_سلولهای_بنیادی
 یافته محققان در زمینه تغییر بیان ژن سلول های کشت شده در فضا (1)
یافته محققان در زمینه تغییر بیان ژن سلول های کشت شده در فضا (1) در پژوهشی جدید محققین نشان داده اند که کشت سلول های قلبی در فضا موجب تغییر در بیان ژن های آن ها می شود، اما تنها 10 روز بعد از برگرداندن این سلول ها به شرایط کشت روی کره زمین، این سلول های قلبی به شرایط طبیعی باز می گردند. در این پژوهش جدید، محققین در دانشگاه کالیفرنیا از سلول های بنیادی پرتوان القایی انسانی برای مطالعه اثر سفر فضایی یا شرایط عدم جاذبه روی عملکرد قلب انسانی استفاده کردند. بی وزنی، عدم جاذبه یا اصطلاحا microgravity، محیطی است که از منظر اثر آن روی بدن انسان به میزان بسیار زیادی ناشناخته باقی مانده است و مطالعاتی از این دست می تواند اطلاعات جدیدی را در این زمینه ارائه دهد.
در پژوهشی جدید محققین نشان داده اند که کشت سلول های قلبی در فضا موجب تغییر در بیان ژن های آن ها می شود، اما تنها 10 روز بعد از برگرداندن این سلول ها به شرایط کشت روی کره زمین، این سلول های قلبی به شرایط طبیعی باز می گردند. در این پژوهش جدید، محققین در دانشگاه کالیفرنیا از سلول های بنیادی پرتوان القایی انسانی برای مطالعه اثر سفر فضایی یا شرایط عدم جاذبه روی عملکرد قلب انسانی استفاده کردند. بی وزنی، عدم جاذبه یا اصطلاحا microgravity، محیطی است که از منظر اثر آن روی بدن انسان به میزان بسیار زیادی ناشناخته باقی مانده است و مطالعاتی از این دست می تواند اطلاعات جدیدی را در این زمینه ارائه دهد. -

#اخبار_جدید_سلولهای_بنیادی
 یافته محققان در زمینه تغییر بیان ژن سلول های کشت شده در فضا (2)
یافته محققان در زمینه تغییر بیان ژن سلول های کشت شده در فضا (2) مطالعات گذشته نشان داده اند که سفرهای فضایی منجر به شروع تغییراتی در عملکرد قلبی از جمله تغییر در ضربان قلب، فشار شریانی پایین تر و برون ده قلبی بالاتر می شود اما در مورد اثر بی وزنی روی عملکرد قلب انسان در سطح سلولی اطلاعات کمی موجود است. این مطالعه با نشان دادن تغییر بیان ژن ها در این شرایط، دیدگاه هایی را در مورد مکانیسم های سلولی ارائه داده است که درک هر چه بهتر و بیشتر آن ها می توان به سلامت فضانوردان در سفرهای طولانی مدت کمک کند و یا دیدگاه های جدیدی را در زمینه بهبود سلامت قلب روی زمین ارائه دهد. محققین برنامه دارند که درمان های مختلفی را روی سلول های قلبی انسانی در شرایط بی وزنی تست کنند تا شاید بتوانند راهی برای جلوگیری از این تغییرات بیابند.
مطالعات گذشته نشان داده اند که سفرهای فضایی منجر به شروع تغییراتی در عملکرد قلبی از جمله تغییر در ضربان قلب، فشار شریانی پایین تر و برون ده قلبی بالاتر می شود اما در مورد اثر بی وزنی روی عملکرد قلب انسان در سطح سلولی اطلاعات کمی موجود است. این مطالعه با نشان دادن تغییر بیان ژن ها در این شرایط، دیدگاه هایی را در مورد مکانیسم های سلولی ارائه داده است که درک هر چه بهتر و بیشتر آن ها می توان به سلامت فضانوردان در سفرهای طولانی مدت کمک کند و یا دیدگاه های جدیدی را در زمینه بهبود سلامت قلب روی زمین ارائه دهد. محققین برنامه دارند که درمان های مختلفی را روی سلول های قلبی انسانی در شرایط بی وزنی تست کنند تا شاید بتوانند راهی برای جلوگیری از این تغییرات بیابند. -
#اخبار_جدید_سلولهای_بنیادی
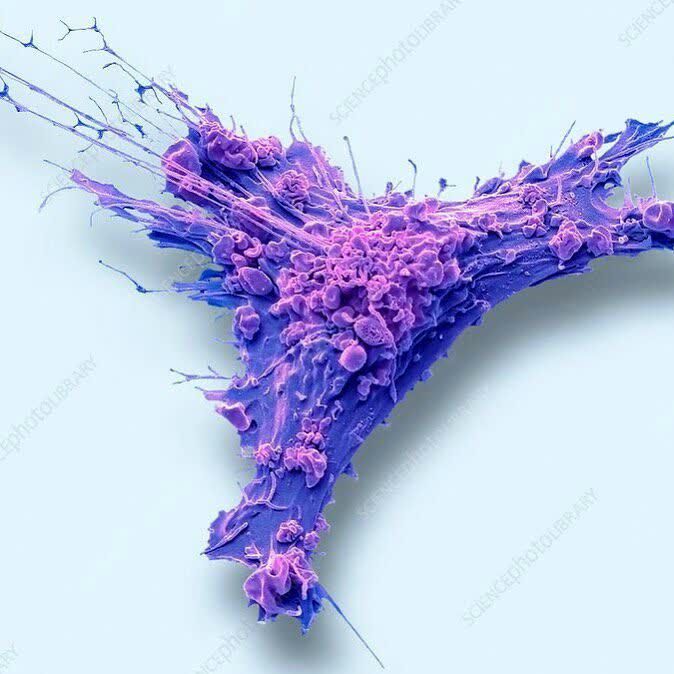
 یافته دانشمند ایرانی در مورد فرایند ترمیم زخم(1)
یافته دانشمند ایرانی در مورد فرایند ترمیم زخم(1) هنگامی که زخمی روی پوست ایجاد میشود، سلولهای بدن به سرعت فرآیند ترمیم پوست را آغاز میکنند. اگرچه نحوه ترمیم زخم توسط سلولها و شکلگیری زخمها مشخص است اما پژوهشگران "دانشگاه واشنگتن در سنت لوییس" (WUSTL) به سرپرستی "دلارام شکیبا" (Delaram Shakiba)، دانشمند ایرانی این دانشگاه، برای نخستین بار توانستند چگونگی آغاز این فرآیند را نشان دهند و بینشهای جدیدی را در مورد ترمیم زخم، فیبروز و متاستاز سرطان فراهم کنند.
هنگامی که زخمی روی پوست ایجاد میشود، سلولهای بدن به سرعت فرآیند ترمیم پوست را آغاز میکنند. اگرچه نحوه ترمیم زخم توسط سلولها و شکلگیری زخمها مشخص است اما پژوهشگران "دانشگاه واشنگتن در سنت لوییس" (WUSTL) به سرپرستی "دلارام شکیبا" (Delaram Shakiba)، دانشمند ایرانی این دانشگاه، برای نخستین بار توانستند چگونگی آغاز این فرآیند را نشان دهند و بینشهای جدیدی را در مورد ترمیم زخم، فیبروز و متاستاز سرطان فراهم کنند. شکیبا و همکارانش، روشی را کشف کردند که فیبروبلاستها به وسیله آن با ماتریس خارج سلولی در تعامل قرار میگیرند. آنها نوعی فرآیند بازگشتی را کشف کردند که بین سلولها و محیط اطراف آنها وجود دارد و در ساختار سلولهایی که پیشتر ناشناخته بودهاند نیز دیده میشود.
شکیبا و همکارانش، روشی را کشف کردند که فیبروبلاستها به وسیله آن با ماتریس خارج سلولی در تعامل قرار میگیرند. آنها نوعی فرآیند بازگشتی را کشف کردند که بین سلولها و محیط اطراف آنها وجود دارد و در ساختار سلولهایی که پیشتر ناشناخته بودهاند نیز دیده میشود. -
#اخبار_جدید_سلولهای_بنیادی
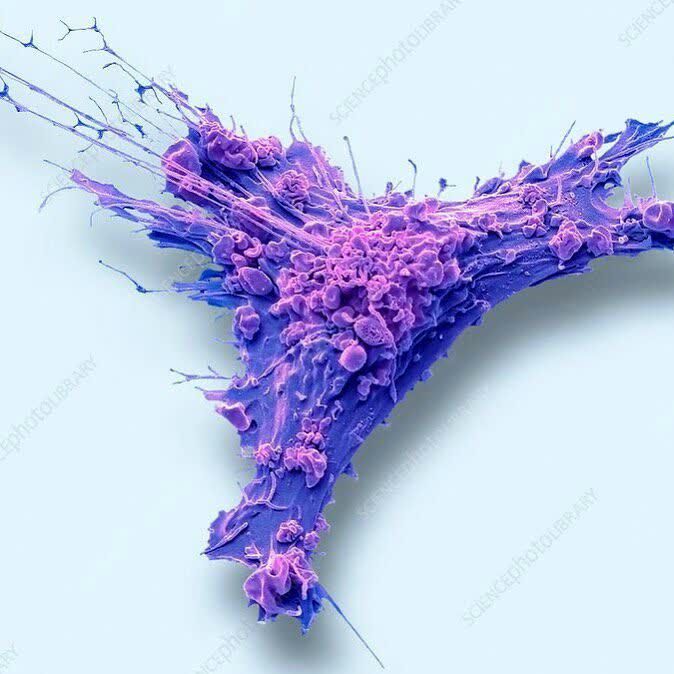
 یافته دانشمند ایرانی در مورد فرایند ترمیم زخم(2)
یافته دانشمند ایرانی در مورد فرایند ترمیم زخم(2)شکیبا گفت: تلاشهای بالینی برای جلوگیری از پیشرفت مشکلاتی مانند زخم و فیبروز، چندان موفقیتآمیز نبودهاند. ما در پژوهش خود دریافتیم که فیبروبلاستها در مراحل نخست این فرآیند، از مکانیسمهای متفاوتی استفاده میکنند و واکنش آنها به داروها در این مراحل میتواند با واکنش آنها در مراحل بعدی متفاوت باشد.
"گای جنین" (Guy Genin)، از پژوهشگران این پروژه گفت: ما در این پژوهش توانستیم برخی مدلهای ریاضی را به کار ببریم تا به فرآیند ترمیم زخم پی ببریم. ما اکنون میتوانیم محرکهای خاصی را طراحی کنیم تا رفتار سلول را هنگام ترمیم بافت آسیب دیده نشان دهیم.
پژوهشگران در این پروژه، از یک روش نقشهبرداری سهبعدی و یک مدل محاسباتی استفاده کردند تا رفتار سلول را مورد بررسی قرار دهند.
جنین افزود: ترمیم زخم، نمونه بارزی از فرآیندهای مهم فیزیولوژیکی است که در بدن صورت میگیرند. ما با بررسی این فرآیندها خواهیم توانست تا بینشهای جدیدی را برای آموزش سلولها در مورد ترمیم زخم ارائه دهیم.Reference:https://www.sciencedaily.com/releases/2020/07/200729124355.htm
-
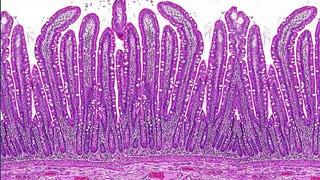
 نقش سلول های بنیادی در ترمیم بافت روده
نقش سلول های بنیادی در ترمیم بافت روده یک پوشش سلولی قوی برای روده سالم حیاتی است و به صورت سدی برای میلیاردها میکروب و سمت مضری عمل می کند در مجرای روده ای وجود دارد. این سد اغلب به دلیل عفونت و التهاب آسیب می بیند که همین امر منجر به علایم دردناک متعددی می شود. در مطالعه صورت گرفته در دانشگاه موناش، محققین محیطی را بررسی کردند که پیرامون سلول های بنیادی را احاطه می کند و از روش تولید ارگانوئیدهای روده ای مشتق از سلول های بنیادی در ظروف آزمایشگاهی برای این امر استفاده کردند. ارزیابی های صورت گرفته با استفاده از این ارگانوئیدهای روده ای نشان داد که تولید یک بیو مولکول موسوم به نوروگولین-1 اثری مستقیم روی سلول های بنیادی دارد و موجب وارد شدن آن ها به فرایند ترمیم می شود. به عقیده محققین استفاده از مکمل های دارای نوروگولین-1 موجب تسریع فرایند ترمیم پوشش روده از طریق فعال کردن مسیرهای رشد کلیدی می شود.
یک پوشش سلولی قوی برای روده سالم حیاتی است و به صورت سدی برای میلیاردها میکروب و سمت مضری عمل می کند در مجرای روده ای وجود دارد. این سد اغلب به دلیل عفونت و التهاب آسیب می بیند که همین امر منجر به علایم دردناک متعددی می شود. در مطالعه صورت گرفته در دانشگاه موناش، محققین محیطی را بررسی کردند که پیرامون سلول های بنیادی را احاطه می کند و از روش تولید ارگانوئیدهای روده ای مشتق از سلول های بنیادی در ظروف آزمایشگاهی برای این امر استفاده کردند. ارزیابی های صورت گرفته با استفاده از این ارگانوئیدهای روده ای نشان داد که تولید یک بیو مولکول موسوم به نوروگولین-1 اثری مستقیم روی سلول های بنیادی دارد و موجب وارد شدن آن ها به فرایند ترمیم می شود. به عقیده محققین استفاده از مکمل های دارای نوروگولین-1 موجب تسریع فرایند ترمیم پوشش روده از طریق فعال کردن مسیرهای رشد کلیدی می شود.
 Reference: https://www.sciencedirect.com/science/article/abs/pii/S1934590920302885?via=ihub
Reference: https://www.sciencedirect.com/science/article/abs/pii/S1934590920302885?via=ihub -
#اخبار_جدید_سلولهای_بنیادی
 یافته محققان در زمینه سلول های بنیادی مزانشیمی و عملکرد آن ها در حضور هورمون آدیپونکتین(1)
یافته محققان در زمینه سلول های بنیادی مزانشیمی و عملکرد آن ها در حضور هورمون آدیپونکتین(1)
محققان به بررسی دلایل احتمالی نتایج متغیر سلول درمانی پرداخته اند و نشان داده اند که تنها فاکتورهای میزبان در این امر دخیل نیستند و خود سلول های بنیادی مزانشیمی نیز می توانند در این امر دخیل باشند. آن ها اخیرا نشان داده اند که آدیپونکتین، یک هورمون سودمند ترشح شده بوسیله سلول های چربی نقش مهمی را بازسازی عضلانی بازی می کند و به پروتئین گیرنده T-کادهرین روی سطح سلول ها متصل می شود. با توجه به این که T-کادهرین روی سطح سلول های بنیادی مزانشیمی به وفور وجود دارد، این محققین به بررسی این امر پرداختند که آیا آدیپونکتین در فعالیت بازسازی کنندگی سلول های بنیادی مزانشیمی در مدل نارسایی قلبی دخیل است یا خیر. آدیپونکتین در غلظت های بالا در خون وجود دارد و تولید اگزوزوم های مترشحه از سلول های بنیادی را تحریک می کند؛ این در حالی است که این اگزوزوم ها نقش میانجی کننده بین سلولی را برای فرایندهای ترمیمی بازی می کنند. -
#اخبار_جدید_سلولهای_بنیادی
 یافته محققان در زمینه سلول های بنیادی مزانشیمی و عملکرد آن ها در حضور هورمون آدیپونکتین(2)
یافته محققان در زمینه سلول های بنیادی مزانشیمی و عملکرد آن ها در حضور هورمون آدیپونکتین(2)
در این مطالعه با اندازه گیری اولیه تولید اگزوزومن ها در سیستم های کشت سلولی، محققین ثابت کردند که افزایش مقدار آدیپونکتین منجر به افزایش میزان اگزوزوم های مشتق از سلول های بنیادی مزانشیمی می شود که خود به بیان T-کادهرین روی سطح آن ها بستگی دارد. تزریق سلول های بنیادی مزانشیمی به مدل موشی نارسایی قلبی منجر به بهبودی قابل توجه عملکرد بطن چپ قلب شد که با میزان افزایش یافته اگزوزوم ها در جریان خون ارتباط مستقیمی داشت. این در حالی بود که با افزایش سطح آدیپونکتین در خون، اثر درمانی سلول های بنیادی مزانشیمی روی عملکرد قلبی به میزان قابل توجهی بهبود یافت. در مجموع این مطالعه نشان داد که سلول های بنیادی مزانشیمی اثرات درمانی شان روی عملکرد قلبی را از طریق تولید اگزوزوم ها بر جای می گذارند که این امر خود تحت تاثیر سطح آدیپونکتین پلاسمای میزان و بیان T-کادهرین روی سطح سلول های بنیادی مزانشیمی قرار دارد. با توجه به این امر استفاده از داروهایی مانند آگونیست های PPARγ می تواند موجب افزایش تولید آدیپونکتین شود و در نتیجه به صورت ترکیب با سلول درمانی برای تقویت نتایج سلول درمانی استفاده شود. -

#اخبار_جدید_سلولهای_بنیادی
 غیرفعال کردن یک ژن می تواند منجر به درمان سندروم داون شود.
غیرفعال کردن یک ژن می تواند منجر به درمان سندروم داون شود.
 بر اساس پژوهشی که در دانشگاه راتگرز (Rutgers) آمریکا صورت گرفته، هدف قرار دادن یک ژن کلیدی پیش از تولد می تواند منجر به درمان سندروم داون، معکوس کردن رشد غیرطبیعی مغز و بهبود عملکرد شناختی پس از تولد شود.
بر اساس پژوهشی که در دانشگاه راتگرز (Rutgers) آمریکا صورت گرفته، هدف قرار دادن یک ژن کلیدی پیش از تولد می تواند منجر به درمان سندروم داون، معکوس کردن رشد غیرطبیعی مغز و بهبود عملکرد شناختی پس از تولد شود. در این مطالعه که نتایج آن در مجله Cell Stem Cell چاپ شده است دانشمندان دو مدل آزمایشگاهی (یک مدل ارگانویید ۳بعدی از مغز و یک مدل مغز موش با سلولهای انسانی) به وسیله سلولهای بنیادی برگرفته از افراد مبتلا به سندروم داون ساخته و دریافتند که ژن OLIG2 نقش بسیار مهمی در علایم ایجاد شده در مغز بیماران ایفا می کند.
در این مطالعه که نتایج آن در مجله Cell Stem Cell چاپ شده است دانشمندان دو مدل آزمایشگاهی (یک مدل ارگانویید ۳بعدی از مغز و یک مدل مغز موش با سلولهای انسانی) به وسیله سلولهای بنیادی برگرفته از افراد مبتلا به سندروم داون ساخته و دریافتند که ژن OLIG2 نقش بسیار مهمی در علایم ایجاد شده در مغز بیماران ایفا می کند. این کشف می تواند راهکاری بسیار کلیدی در درمان بیماران مبتلا به سندروم داون پیش از تولد با هدفگیری ژن OLIG2 داشته باشد. از طرف دیگر ترکیب دو مدل آزمایشگاهی استفاده شده در این مطالعه، قابلیت کاربرد در سایر اختلالات ادراکی همچون آلزایمر و اوتیسم را نیز داراست.
این کشف می تواند راهکاری بسیار کلیدی در درمان بیماران مبتلا به سندروم داون پیش از تولد با هدفگیری ژن OLIG2 داشته باشد. از طرف دیگر ترکیب دو مدل آزمایشگاهی استفاده شده در این مطالعه، قابلیت کاربرد در سایر اختلالات ادراکی همچون آلزایمر و اوتیسم را نیز داراست.
دانش-آموزان-آلاء -

حسین بهاروند، استاد ممتاز، موسس و رئیس پژوهشکده زیست شناسی و فناوری سلول های بنیادی پژوهشگاه رویان است. وی از سال 1385 تاکنون ریاست گروه زیست شناسی تکوینی دانشگاه علم و فرهنگ را نیز بر عهده دارد. او در سال 1382 برای اولین بار سلول های بنیادی جنینی انسانی و موشی را در ایران تولید کرد و در سال 1387 به همراه همکارانش موفق به تولید سلول های بنیادی پرتوان القائی انسانی و موشی شد. این فعالیت ها او و همکارانش را قادر ساخت تا شاخه های مختلف پزشکی بازساختی را در ایران پایه گذاری و پیگیری کنند. زمینه های پژوهشی او پیرامون ارتقاء تحقیقات ترجمانی و پزشکی بازساختی از دیدگاه سلول های بنیادی، زیست شناسی تکوینی و مهندسی با الهام از طبیعت است. وی روی دگرتمایزی و تمایز سلول های بنیادی پرتوان به سلول های قلبی، عصبی، کبدی و بتای پانکراس تحقیق می کند و درباره ساز و کار های پرتوانی و زیست شناسی سلول های زایا مطالعه می نماید. ایشان در کارآزمایی های بالینی متعدد و پیوند سلول های بنیادی بافتی مشارکت داشته است و در زمینه توسعه تولید صنعتی سلول فعالیت می کند. او به عنوان سخنران مدعو در بسیاری از کنفرانس های علمی ملی و بین المللی حضور داشته است. از وی 4 کتاب به زبان انگلیسی توسط انتشارات Springer و John Wiley به ترتیب در سال های 1389، 1391و 1394 چاپ شده است. تاکنون 297 مقاله بین المللی، 102 مقاله داوری شده داخلی به همراه 7 فصل در کتب بین المللی از دکتر بهاروند به چاپ رسیده است. 7 کتاب تألیفی به زبان فارسی و 8 کتاب ترجمه شده از دیگر آثار وی هستند. با استناد به Google Scholar تا ماه سپتامبر 2017 بیش از 6950 بار به مطالعات ایشان ارجاع شده و دارای h-index 43 است. حسین بهاروند عضو هیئت تحریریه هشت مجله علمی بین المللی از جمله Journal of Biological Chemistry و Scientific reports (زیرمجموعه انتشارات Nature) بوده و دارای 2 اختراع ثبت شده در آمریکاست. وی 29 جایزه ملی و بین المللی دریافت کرده است. در دهمین، دوازدهمین و هفدهمین جشنواره رازی (سال های 1383، 1385 و 1391) موفق به کسب جایزه تحقیقات در زمینه علم پزشکی از وزارت بهداشت، درمان و آموزش پزشکی و در بیست و ششمین جشنواره بین المللی خوارزمی (سال 1391) موفق به دریافت جایزه تحقیقات در حوزه علوم پایه از وزارت علوم، تحقیقات و فناوری شده است. در سال 1389 در بیست و هفتمین دوره کتاب سال جمهوری اسلامی ایران، کتاب سلول های بنیادی به تألیف وی به عنوان کتاب برگزیده شناخته شد. ایشان در سال 1389 موفق به دریافت جایزه محقق برتر جهان اسلام در حوزه فناوری و علوم از ISESCO (سازمان اسلامی آموزشی، فرهنگی و علمی) گردید. او در سال های 1388 و 1392 جایزه دکتر هادوی را از جشنواره علمی فرهنگستان علوم پزشکی دریافت کرد و در سال 1394 به عنوان استاد برجسته حیطه علوم پزشکی از سوی بنیاد بین المللی آکادمیک پروفسور یلدا و همچنین چهره تاثیرگذار بیوتکنولوژی کشور معرفی شد. در سال 1395 وی به عنوان محقق برتر حوزه سلول های بنیادی از سوی انجمن ژنتیک ایران برگزیده شد. نامبرده در سال 1393 جایزه علامه طباطبایی را کسب کرد و به عنوان استاد ممتاز از سوی بنیاد ملی نخبگان و معاونت علمی و فناوری ریاست جمهوری شناخته شد. همچنین ایشان در سال 1393 جایزه بین المللی یونسکو-گینه استوایی در حوزه علوم زیستی را دریافت کرد. این جایزه به علت تحقیق بر سلول های بنیادی و کاربرد آن در پزشکی بازساختی در راستای بهبود کیفیت زندگی انسان ها به ایشان اعطا شد.
سوابق اجراییریاست پژوهشکده سلول های بنیادی پژوهشگاه رویان (1385 تا کنون) عضو هیات علمی پژوهشگاه رویان (1375 تا کنون) مدیر گروه زیست شناسی تکوینی، دانشگاه علم و فرهنگ (1386 تا کنون)تحصیلات
دکتری ، 1383 ، زیست شناسی تکوینی ، دانشگاه خوارزمی کارشناسی ارشد ، 1375 ، زیست شناسی تکوینی ، دانشگاه شهید بهشتی کارشناسی ، 1373 ، زیست شناسی تکوینی ، دانشگاه شیرازدانش-آموزان-آلاء
تجربیا ریاضیا انسانیا
دهم یازدهم دوازدهم
دریا دریایی ZDM @Dr-Rashidi









 🧫
🧫