نکات فصل دوم شیمی ۱۱
-
 سامانه = بخشی از جهان که برای مطالعه ترموشیمی انتخاب میشه
سامانه = بخشی از جهان که برای مطالعه ترموشیمی انتخاب میشه محیط = بقیه جهان پیرامون سامانه مورد نطر
محیط = بقیه جهان پیرامون سامانه مورد نطر دما = معیاری قراردادی که میانگین تندی دره های سازنده یک ماده را نشان میدهد
دما = معیاری قراردادی که میانگین تندی دره های سازنده یک ماده را نشان میدهد گرما = به مقدار انرزی گرمایی گفته میشود که به دلیل اختلاف دما بین ۲ ماده جاری میشود
گرما = به مقدار انرزی گرمایی گفته میشود که به دلیل اختلاف دما بین ۲ ماده جاری میشود طرفیت گرمایی = گرمای مورد نیاز برای افزایش دمای یک نمونع ماده به اندازه یک درجه سلسیوس
طرفیت گرمایی = گرمای مورد نیاز برای افزایش دمای یک نمونع ماده به اندازه یک درجه سلسیوس طرفیت گرمایی ویزه = مقدار گرمایی که به یک گرم از یک ماده مورد نیاز داده میشود تا دمای ان به اندازه یک درجه سلسیوس تغییر کند
طرفیت گرمایی ویزه = مقدار گرمایی که به یک گرم از یک ماده مورد نیاز داده میشود تا دمای ان به اندازه یک درجه سلسیوس تغییر کند اگزی گرمایی = به مجموع انرزی جنبشی ذره های سازنده یک ماده
اگزی گرمایی = به مجموع انرزی جنبشی ذره های سازنده یک ماده -
 واکنش گرماده = گرما از سامانه به محیط وارد میشه _و نماد qدر سمت راست معادله نوشته میشه
واکنش گرماده = گرما از سامانه به محیط وارد میشه _و نماد qدر سمت راست معادله نوشته میشه واکنش گرماگیر = گرما از محیط وارد سامانه میشه و نماد qدر سمت چپ و کنار واکنش دهنده ها نوشته میشه
واکنش گرماگیر = گرما از محیط وارد سامانه میشه و نماد qدر سمت چپ و کنار واکنش دهنده ها نوشته میشه انرژی پتانسیل = به مجموع انرزی های ذخیره شده دریک ماده که به نیروی نگهدارنده ذره های سازندش بستگی دارد
انرژی پتانسیل = به مجموع انرزی های ذخیره شده دریک ماده که به نیروی نگهدارنده ذره های سازندش بستگی دارد توصیف یک ماده = بیان مقدار ان برحسب گرم یا مول در دما و فشار معین
توصیف یک ماده = بیان مقدار ان برحسب گرم یا مول در دما و فشار معین -


-
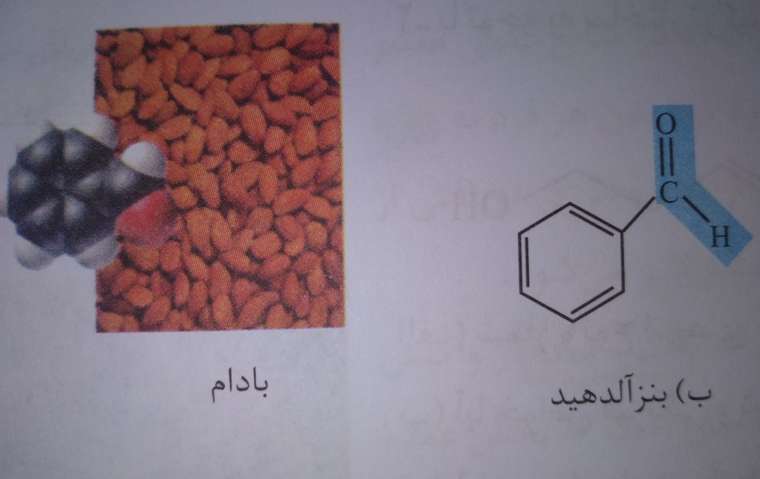
فرمول مولکولی = C6H6O
گروه عاملی = الدهیدیبه دلیل وجود گروه عاملی الدهیدی دارای پیوند قطبی میباشد
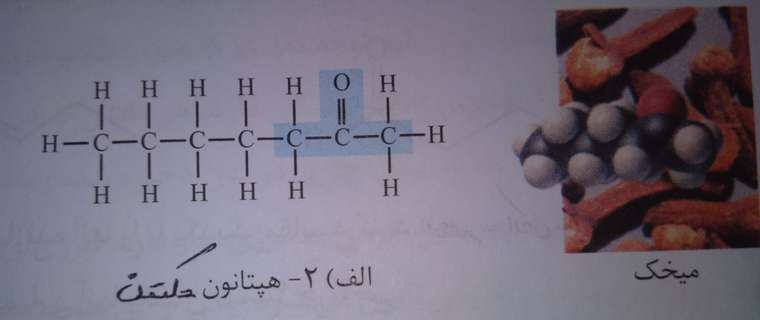
فرمول مولکولی = C7H14O
فاقد پیوند هیدروژنی
۵ اتم کربن هرکدام به ۲ اتم کربن دیگر متصل اند -
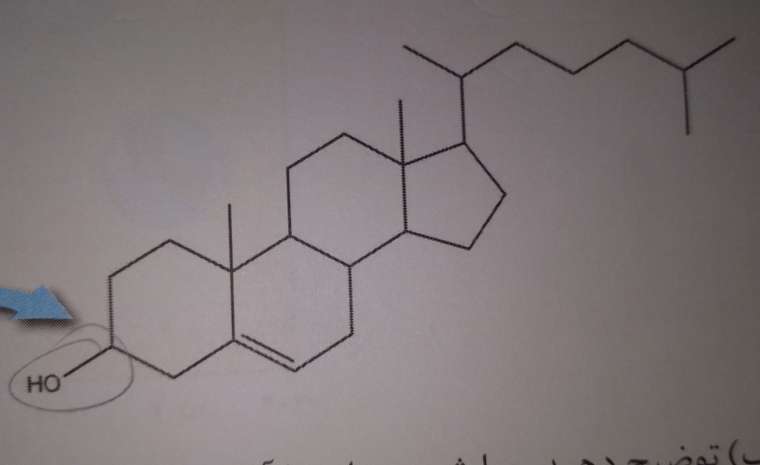
 کلسترول
کلسترول
فرمول مولکولی = C27H46O
گروه عاملی = ههیدروکسیل ( الکلی )
 یک الکل سیر نشده غیر اروماتیک
یک الکل سیر نشده غیر اروماتیک
 هیدردکربن محسوب نمیشود
هیدردکربن محسوب نمیشود
 بخش ناقطبی خیلی بزرگتر از بخش قطبی
بخش ناقطبی خیلی بزرگتر از بخش قطبی
 در اب محلول نیست
در اب محلول نیست
 یکی از مواد الی موجود در مواد غذاهای جانوری که مقدار اضافی ان در دیواره رگ رسوب میکند
یکی از مواد الی موجود در مواد غذاهای جانوری که مقدار اضافی ان در دیواره رگ رسوب میکند -
 نکاتی درمورد گرماسنج لیوانی
نکاتی درمورد گرماسنج لیوانی🧊دستگاهی ساده برای اندازه گیری تجربی انتالپی واکنش
🧊برای تعیین انتالپی فرایندهای انحلال وواکنش هایی که در حالت محلول انجام میشود مناسب است
🧊برای تعیین انتالپی واکنش های سوختن مناسب نیست
🧊از ان برای اندازه گیری گرمای یک واکنش در فشار ثابت استفاده میشود
-
 نکاتی در مورد هیدروژن پر اکسید
نکاتی در مورد هیدروژن پر اکسید ماده ای است که بانام تجاری اب اکسیژنه به فروش میرود
ماده ای است که بانام تجاری اب اکسیژنه به فروش میرود محلول رقیق ان خاصیت ضدعفونی کننده و رنگبری و لکه بری دارد
محلول رقیق ان خاصیت ضدعفونی کننده و رنگبری و لکه بری دارد یک مولکول قطبی محسوب میشود
یک مولکول قطبی محسوب میشود پایداری ان نسبت به اب کمتر است زیرا در ساختار خود O_Oدارد که پیوندی ناقطبی و سست است
پایداری ان نسبت به اب کمتر است زیرا در ساختار خود O_Oدارد که پیوندی ناقطبی و سست است برای اندازه گیری ان از قانون هس استفاده میشود
برای اندازه گیری ان از قانون هس استفاده میشودااگ براتون مفید بود لطفا رای بدین


-
 قانون هس
قانون هس به قانون جمع پذیری گرمای واکنش ها معروف است
به قانون جمع پذیری گرمای واکنش ها معروف است برای واونش هایی قابل اجرا هست که شرایط تشکیل انها یکسان باشد = در دما وفشار یکسان
برای واونش هایی قابل اجرا هست که شرایط تشکیل انها یکسان باشد = در دما وفشار یکسان براساس ان گرمای یک واکنش معین ره راهی که برای انجام ان در پیش گرفته وابسته نیست
براساس ان گرمای یک واکنش معین ره راهی که برای انجام ان در پیش گرفته وابسته نیست چنانچه معادله را به صورت وارون بنویسیم تعییرات امتالپی در منفی یک ضرب میشود
چنانچه معادله را به صورت وارون بنویسیم تعییرات امتالپی در منفی یک ضرب میشود معادله واکنش در هر عددی صرب یا تقسیم شود تعییرات انتالپی هم همان روند را دارد
معادله واکنش در هر عددی صرب یا تقسیم شود تعییرات انتالپی هم همان روند را دارد -
 گاز متان
گاز متان 
 ساده ترین ونخستین عضو الکان ها
ساده ترین ونخستین عضو الکان ها بخش عمده گاز شهری رو تشکیل میده
بخش عمده گاز شهری رو تشکیل میده از تجزیه گیاهان به وسیاه باکتری های بی هوازی زیر اب تولید میشه
از تجزیه گیاهان به وسیاه باکتری های بی هوازی زیر اب تولید میشه نخستین بار از سطح مرداب جمع اوری شد وبه این نام مشهور شد
نخستین بار از سطح مرداب جمع اوری شد وبه این نام مشهور شد -
 با اینکه همه واکنش های سوختن گرماده هستن اما ارزش سوختی مواد بدون علامت منفی گزارش میشه
با اینکه همه واکنش های سوختن گرماده هستن اما ارزش سوختی مواد بدون علامت منفی گزارش میشه اب حاصل از سوختن مواد الی در لحطه سوختن به صورت گاز است ولی بعد از مدتی در دمای اتاق به حالت مایع درمیاید
اب حاصل از سوختن مواد الی در لحطه سوختن به صورت گاز است ولی بعد از مدتی در دمای اتاق به حالت مایع درمیاید الکل ها سوخت سبز به شمار میروند زیرا در ساختار خود Cو H اکسیژن هم دارند
الکل ها سوخت سبز به شمار میروند زیرا در ساختار خود Cو H اکسیژن هم دارند درمیان کربوهیدرات ها چربی ها وپروتیین ها فقط کربوهیدرات ها هستند که گلوکز حاصل از انها درخون حل شده و اکسایش ان در یاخته ها صورت میگیرد
درمیان کربوهیدرات ها چربی ها وپروتیین ها فقط کربوهیدرات ها هستند که گلوکز حاصل از انها درخون حل شده و اکسایش ان در یاخته ها صورت میگیرد در میان هیدرو کربن های مطرح شده در کتاب متان بیشترین و متانول کمترین ارزش سوختی را دارد
در میان هیدرو کربن های مطرح شده در کتاب متان بیشترین و متانول کمترین ارزش سوختی را دارد


