شیمی دهم فصل دو
-
 Z Z.ns marked this topic as a question on
Z Z.ns marked this topic as a question on
-
سلام. اگر رشتتون ریاضی باشه که فصل پنج فیزیک دهم میخونید به صورت کامل. ولی خب این توضیحات رو میدم: اول رابطه pv = nRT رو در نظر بگیرید. خب اگر T ثابت باشه(nR هم که ثابته دیگه) باید pv همیشه برابر با یه مقدار ثابتی باشه، پس اگر بر حسب p نمودار رو بکشیم، میشه p = d/V(دی یک عدد ثابت و V متغیره)، پس با این توضیحات نمودار هموگرافیکی میشه، یعنی چیزی شبیه به 1 به روی x. اصلا هم مهم نیست بدونید نمودار هموگرافیک چیه، فقط کافیه بدونید شکلش مثل شکل زیره(توجه کنید در نمودار PV شکلش مثل شکل زیر هست، اگر بخوایم فرآیند هم دما رو با نمودار pt یا vt رسم کنیم کار سختی نیست(یه خط موازی محور y میشه):
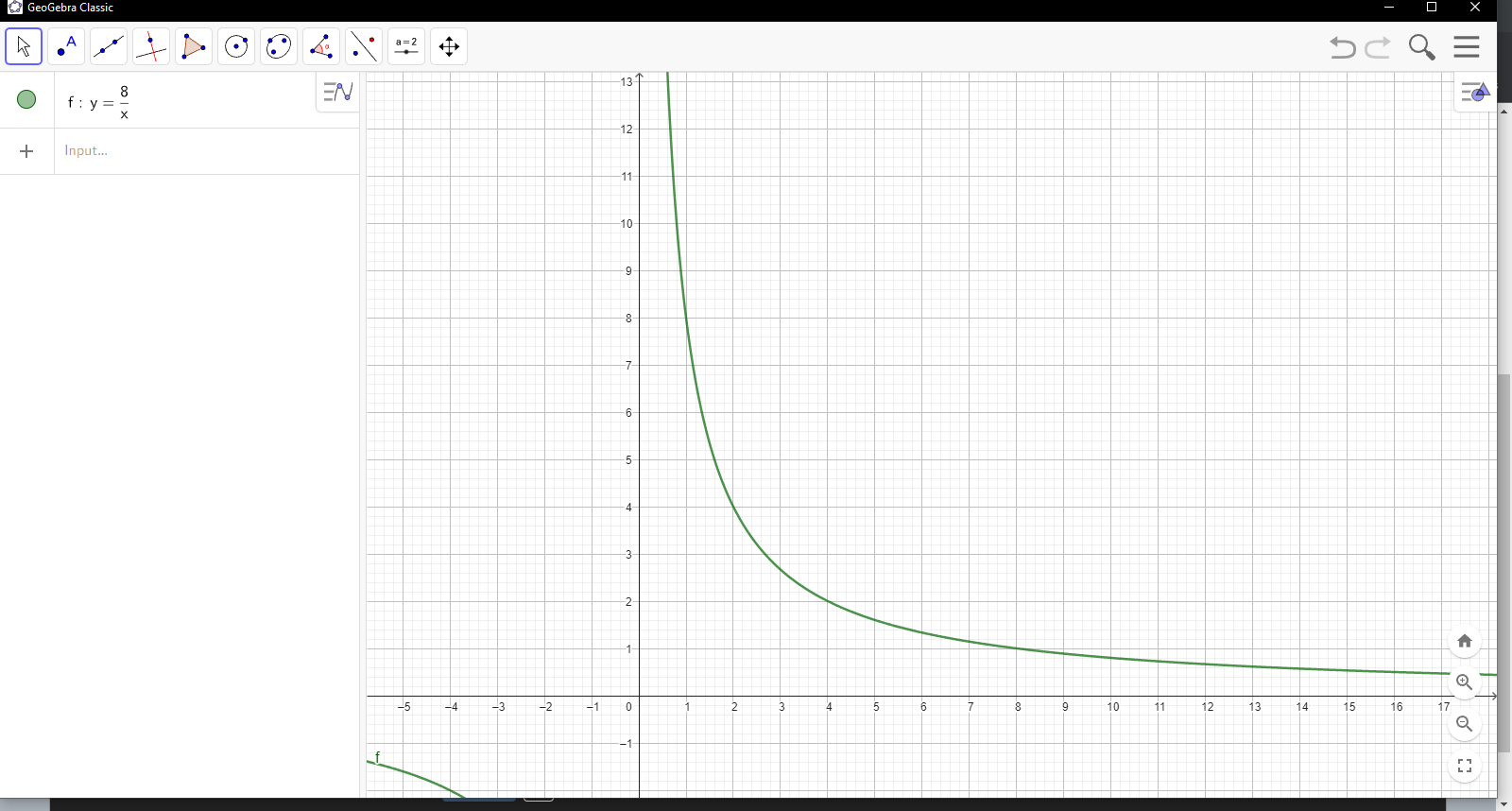
راستی، گفتید سهمی، این نمودار همونطور که گفتم هموگرافیکه و فکر کنم توی ریاضی تجربی ها هم هست(توی حسابان هست، ولی تجربی هارو یکم شک دارم. البته شکلش برای شیمی مهمه، خودش مهم نیست)
خب درباره فرآیند هم فشار توی نمودار pt و pv نکته خاصی نیست، در هر دو یه معادله خط موازی محور x ها تشکلی میشه، چون فشار برابره حین انجام واکنش. اما نکته اصلی نمودار vt هست. نمیخوام خیلی ریز بشم چون این اگر خیلی توضیح بدم از بحث شیمی خارج میشه و وارد بحث ترمودینامیک میشیم. پس در همین حد بدونید که نمودارش معادله خط هست و اگر خط رو امتداد بدیم باید از مبدا بگذره. حالا چون دلیلش سخت نیست میگم، من خودم میتونم با دو راه اثبات کنم، فکر کنم راه های بیشتری هم داشته باشه ولی من بلد نیستم، ولی به هر حال طبق رابطه pv = nRT اگر فرایند هم فشار باشه توی نمودار VT ما میتونیم بگیم: V/T = nR/p، پس: V=dT(اینجا V و T متغیر و دی هم ثابته(همون ان آر به روی پی) پس معادله خط هست و عرض از مبدا نداره، پس باید این خط از مبدا بگذره(توجه کن گفتم خط، نه خود واکنش، یعنی پاره خط واکنش رو اگر امتداد بدی و خطش رو تشکیل بدی از مبدا میگذره)فرآیند هم حجم هم مثل فرآیند هم فشار هست تقریبا، نمودار PV و VT که یه خط به ترتیب موازی با محور y و موازی با محور x. نمودار PT یه معادله خط که از مبدا مختصات میگذره.
پس به طور خلاصه:
هم دما PV هموگرافیک، VT , PT خطی موازی با محور y.
هم حجم PV و VT به ترتیب خط موازی محور y و x و PTخطی گذرنده از مبدا.
هم فشار PT و PV خطی موازی محور x ها و VT خطی گذرنده از مبدا مختصات.اگر مشکل یا توضیح اضافی خواستی بگو.
-
سلام. اگر رشتتون ریاضی باشه که فصل پنج فیزیک دهم میخونید به صورت کامل. ولی خب این توضیحات رو میدم: اول رابطه pv = nRT رو در نظر بگیرید. خب اگر T ثابت باشه(nR هم که ثابته دیگه) باید pv همیشه برابر با یه مقدار ثابتی باشه، پس اگر بر حسب p نمودار رو بکشیم، میشه p = d/V(دی یک عدد ثابت و V متغیره)، پس با این توضیحات نمودار هموگرافیکی میشه، یعنی چیزی شبیه به 1 به روی x. اصلا هم مهم نیست بدونید نمودار هموگرافیک چیه، فقط کافیه بدونید شکلش مثل شکل زیره(توجه کنید در نمودار PV شکلش مثل شکل زیر هست، اگر بخوایم فرآیند هم دما رو با نمودار pt یا vt رسم کنیم کار سختی نیست(یه خط موازی محور y میشه):

راستی، گفتید سهمی، این نمودار همونطور که گفتم هموگرافیکه و فکر کنم توی ریاضی تجربی ها هم هست(توی حسابان هست، ولی تجربی هارو یکم شک دارم. البته شکلش برای شیمی مهمه، خودش مهم نیست)
خب درباره فرآیند هم فشار توی نمودار pt و pv نکته خاصی نیست، در هر دو یه معادله خط موازی محور x ها تشکلی میشه، چون فشار برابره حین انجام واکنش. اما نکته اصلی نمودار vt هست. نمیخوام خیلی ریز بشم چون این اگر خیلی توضیح بدم از بحث شیمی خارج میشه و وارد بحث ترمودینامیک میشیم. پس در همین حد بدونید که نمودارش معادله خط هست و اگر خط رو امتداد بدیم باید از مبدا بگذره. حالا چون دلیلش سخت نیست میگم، من خودم میتونم با دو راه اثبات کنم، فکر کنم راه های بیشتری هم داشته باشه ولی من بلد نیستم، ولی به هر حال طبق رابطه pv = nRT اگر فرایند هم فشار باشه توی نمودار VT ما میتونیم بگیم: V/T = nR/p، پس: V=dT(اینجا V و T متغیر و دی هم ثابته(همون ان آر به روی پی) پس معادله خط هست و عرض از مبدا نداره، پس باید این خط از مبدا بگذره(توجه کن گفتم خط، نه خود واکنش، یعنی پاره خط واکنش رو اگر امتداد بدی و خطش رو تشکیل بدی از مبدا میگذره)فرآیند هم حجم هم مثل فرآیند هم فشار هست تقریبا، نمودار PV و VT که یه خط به ترتیب موازی با محور y و موازی با محور x. نمودار PT یه معادله خط که از مبدا مختصات میگذره.
پس به طور خلاصه:
هم دما PV هموگرافیک، VT , PT خطی موازی با محور y.
هم حجم PV و VT به ترتیب خط موازی محور y و x و PTخطی گذرنده از مبدا.
هم فشار PT و PV خطی موازی محور x ها و VT خطی گذرنده از مبدا مختصات.اگر مشکل یا توضیح اضافی خواستی بگو.
-
 Z Z.ns has marked this topic as solved on
Z Z.ns has marked this topic as solved on


