سلول های بنیادی راهی به آینده
-
https://www.aparat.com/v/nfxZm
رویانتان،رویان باد!
@دانش-آموزان-آلاء -
https://www.aparat.com/v/HwTSk
چی بودیم،چی شدیم! -
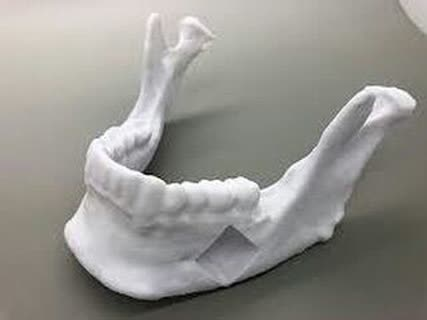
استفاده از فناوری پرینت سه بعدی برای تولید بافت استخوانی
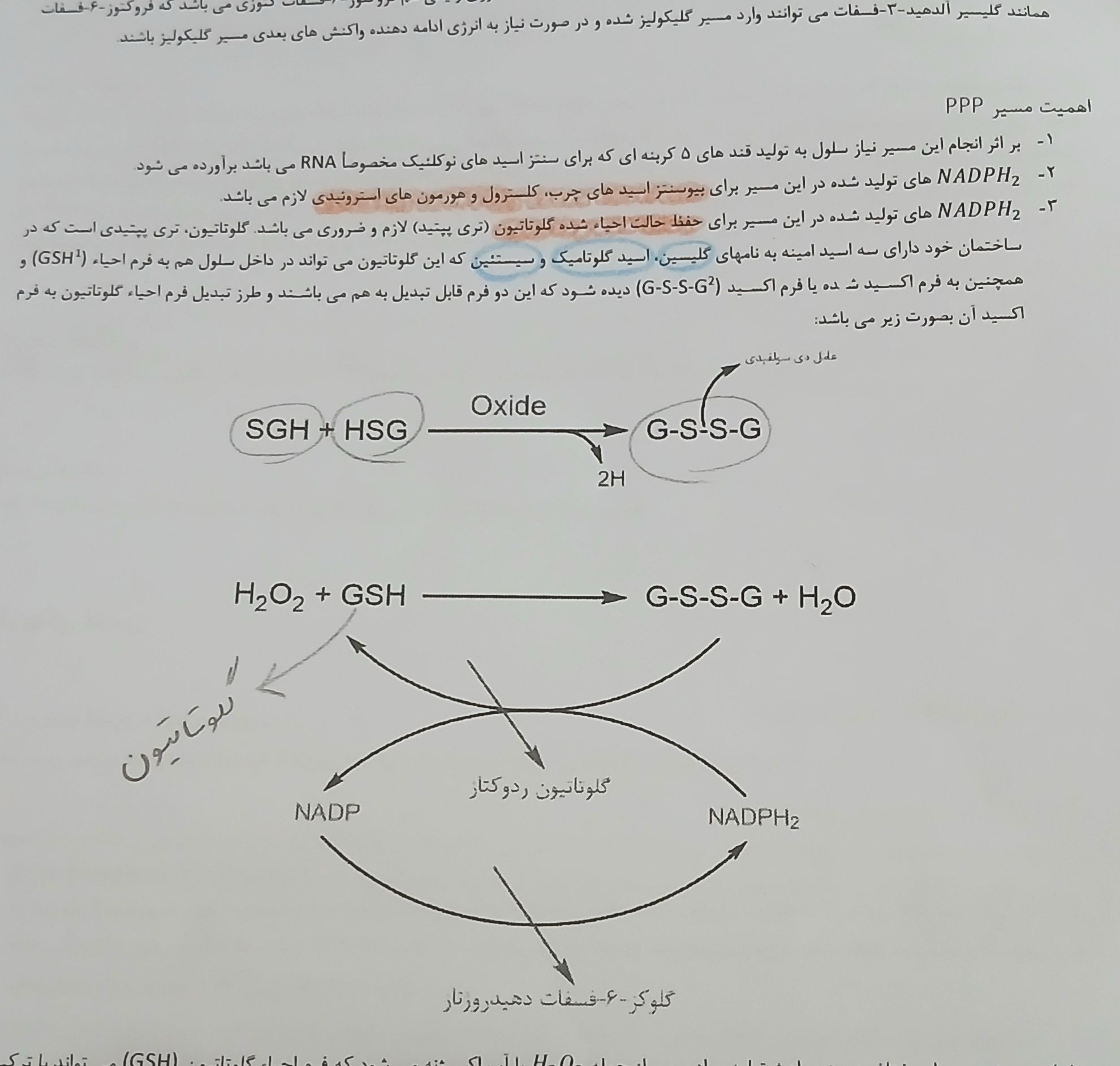
 پرینت زیستی یک رویکرد نوظهور در تولید زیست موادی مانند هیدروژل است که آن ها را سلول و فاکتورهای رشد ترکیب می کند و از این مخلوط برای تولید ساختارهای شبه بافتی که بافت های طبیعی را تقلید می کنند، استفاده می کند. یکی از کاربردهای این فناوری می تواند طراحی و تولید گرافت های استخوانی با توجه به نیاز فرد باشد، به طوری که بتواند ناحیه آسیب دیده را به خوبی پوشش دهد. پرینت زیستی نیازمند زیست موادی است که بتوانند حامل یا ناقل سلول ها باشد، به خوبی قابل پرینت کردن باشند و بتوانند یک ریز محیط مناسب را برای سلول ها فراهم آورند. اما متاسفانه جوهرهای زیستی موجود از زیست سازگاری، قابلیت پرینت، ثبات ساختاری و عملکردهای مناسب بافتی لازم برخوردار نیستند و به همین دلیل استفاده از آن ها در پیش بالین و بالین با مشکل مواجه است. در پژوهشی جدید، محققان یک جوهر زیستی موسوم به جوهر زیستی در هم تنیدگی یونی-کووالانی مهندسی شده جدید (Nanoengineered Ionic-Covalent Entanglement (NICE)) را تولید کرده اند.
پرینت زیستی یک رویکرد نوظهور در تولید زیست موادی مانند هیدروژل است که آن ها را سلول و فاکتورهای رشد ترکیب می کند و از این مخلوط برای تولید ساختارهای شبه بافتی که بافت های طبیعی را تقلید می کنند، استفاده می کند. یکی از کاربردهای این فناوری می تواند طراحی و تولید گرافت های استخوانی با توجه به نیاز فرد باشد، به طوری که بتواند ناحیه آسیب دیده را به خوبی پوشش دهد. پرینت زیستی نیازمند زیست موادی است که بتوانند حامل یا ناقل سلول ها باشد، به خوبی قابل پرینت کردن باشند و بتوانند یک ریز محیط مناسب را برای سلول ها فراهم آورند. اما متاسفانه جوهرهای زیستی موجود از زیست سازگاری، قابلیت پرینت، ثبات ساختاری و عملکردهای مناسب بافتی لازم برخوردار نیستند و به همین دلیل استفاده از آن ها در پیش بالین و بالین با مشکل مواجه است. در پژوهشی جدید، محققان یک جوهر زیستی موسوم به جوهر زیستی در هم تنیدگی یونی-کووالانی مهندسی شده جدید (Nanoengineered Ionic-Covalent Entanglement (NICE)) را تولید کرده اند. جوهر زیستی NICE ترکیبی از دو فناوری است که به همراه هم موجب تقویت موثرتر این جوهر و تولید ساختارهای قوی تری می شوند. این جوهر زیستی اجازه تولید داربست های قوی می دهد که می توانند در مقیاس مورد نظر و با یک ساختار قابل تحمل برای سلول ها تولید شوند. بارگیری #سلولهای_بنیادی درون این جوهر زیستی برای تولید بافت استخوانی منجر به تولید بافت استخوانی سه بعدی شد که ساختار بافت اسفنجی موجود در استخوان مهره ها را تداعی می کنند. محققین بر این باورند که استفاده از این جوهر زیستی در تولید داربست های استخوانی و بافت های استخوانی می تواند یک رویکرد درمانی موثر برای مشکلات ارتوپدی در آینده ای نزدیک باشد.
جوهر زیستی NICE ترکیبی از دو فناوری است که به همراه هم موجب تقویت موثرتر این جوهر و تولید ساختارهای قوی تری می شوند. این جوهر زیستی اجازه تولید داربست های قوی می دهد که می توانند در مقیاس مورد نظر و با یک ساختار قابل تحمل برای سلول ها تولید شوند. بارگیری #سلولهای_بنیادی درون این جوهر زیستی برای تولید بافت استخوانی منجر به تولید بافت استخوانی سه بعدی شد که ساختار بافت اسفنجی موجود در استخوان مهره ها را تداعی می کنند. محققین بر این باورند که استفاده از این جوهر زیستی در تولید داربست های استخوانی و بافت های استخوانی می تواند یک رویکرد درمانی موثر برای مشکلات ارتوپدی در آینده ای نزدیک باشد. -

ساخت نوعی زخم پوش نانوفیبری با قابلیت ترمیمی و آنتی باکتریال
 برخی از مطالعات نشان میدهند که نوعی عسل میتواند به افزایش تولید گلبولهای سفید خون که وظیفه مبارزه با عفونتها و التیام زخمها را بر عهده دارند کمک کند. این عسل در درمان زخمها و ترمیم بافتهای مرده پوست کارایی زیادی دارد بهطوریکه در بعضی از بیمارستانها و مراکز درمانی تا حد زیادی جایگزین آنتی بیوتیکها شدهاست؛ و جهت درمان زخم و مداوای زخم بستر و سوختگیهای عمیق، همچنین جوانسازی سلولهای پوست از این عسل استفاده میشود.
برخی از مطالعات نشان میدهند که نوعی عسل میتواند به افزایش تولید گلبولهای سفید خون که وظیفه مبارزه با عفونتها و التیام زخمها را بر عهده دارند کمک کند. این عسل در درمان زخمها و ترمیم بافتهای مرده پوست کارایی زیادی دارد بهطوریکه در بعضی از بیمارستانها و مراکز درمانی تا حد زیادی جایگزین آنتی بیوتیکها شدهاست؛ و جهت درمان زخم و مداوای زخم بستر و سوختگیهای عمیق، همچنین جوانسازی سلولهای پوست از این عسل استفاده میشود. عسل مانوکا حاوی ترکیبات زیست فعال زیادی از جمله پراکسید هیدروژن، متیل گلیوکسال(MGO)، پلی فنول ها، سوکروز و مالتوز است که به فرایند بهبودی کمک می کنند. همه انواع عسل ها حاوی پراکسید هستند که در تماس با باکتری آن را می کشند و در این میان به سلول های انسانی نیز آسیب می رسانند. آن چه پراکسید هیدروژن را در نمونه عسل خاص می سازد، این است که به آهستگی تولید می شود و به آهستگی رشد باکتری را در متوقف می کند و این در حالی است که اثر ملایمی روی سلول های انسانی دارد. در این میان عسل مانوکا دارای MGO نیز می باشد که رشد باکتریایی را از طریق محدود کردن قابلیت تحرک سوش های باکتریایی مهار می کند. حتی قند موجود در این عسل یعنی سوکروز و مالتوز نیز می توانند منبع مستقیمی برای تامین انرژی سلول ها روی سطح زخم باشد. در پژوهشی جدید، محققین توانسته اند زخم پوش جدیدی را تولید کنند که در آن از عسل مانوکا نیز برای تولید نانوفیبرهای سلولز استات الکتروریسی شده استفاده شده است.
عسل مانوکا حاوی ترکیبات زیست فعال زیادی از جمله پراکسید هیدروژن، متیل گلیوکسال(MGO)، پلی فنول ها، سوکروز و مالتوز است که به فرایند بهبودی کمک می کنند. همه انواع عسل ها حاوی پراکسید هستند که در تماس با باکتری آن را می کشند و در این میان به سلول های انسانی نیز آسیب می رسانند. آن چه پراکسید هیدروژن را در نمونه عسل خاص می سازد، این است که به آهستگی تولید می شود و به آهستگی رشد باکتری را در متوقف می کند و این در حالی است که اثر ملایمی روی سلول های انسانی دارد. در این میان عسل مانوکا دارای MGO نیز می باشد که رشد باکتریایی را از طریق محدود کردن قابلیت تحرک سوش های باکتریایی مهار می کند. حتی قند موجود در این عسل یعنی سوکروز و مالتوز نیز می توانند منبع مستقیمی برای تامین انرژی سلول ها روی سطح زخم باشد. در پژوهشی جدید، محققین توانسته اند زخم پوش جدیدی را تولید کنند که در آن از عسل مانوکا نیز برای تولید نانوفیبرهای سلولز استات الکتروریسی شده استفاده شده است. سلولز استات یک پلیمر آبدوست و زیست تخریب پذیر با قدرت کشسانی بالا است که می توان از آن برای زخم پوش استفاده کرد. استفاده از این نانوفیبرهای حاوی عسل مانوکا به عنوان شبکه های نانوفیبری برای پوشش زخم، فعالیت آنتی میکروبی بالایی را علیه باکتری های گرم مثبت و منفی نشان داد. این زخم پوش ها قابلیت تنفس مناسبی دارند و موجب افزایش بهبودی زخم می شوند.
سلولز استات یک پلیمر آبدوست و زیست تخریب پذیر با قدرت کشسانی بالا است که می توان از آن برای زخم پوش استفاده کرد. استفاده از این نانوفیبرهای حاوی عسل مانوکا به عنوان شبکه های نانوفیبری برای پوشش زخم، فعالیت آنتی میکروبی بالایی را علیه باکتری های گرم مثبت و منفی نشان داد. این زخم پوش ها قابلیت تنفس مناسبی دارند و موجب افزایش بهبودی زخم می شوند.Reference:https://www.sciencedirect.com/science/article/pii/S0141813020328245?via=ihub
-
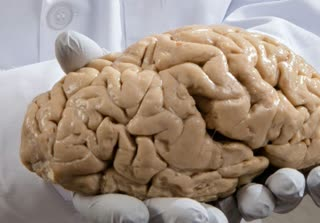
ساخت مدلی سه بعدی از مغز انسان
 درک درست فرآیندهای درگیر در تکوین ، سازماندهی و اختلال در عملکرد مغز انسان دشوار بوده است زیرا ما نمی توانیم مستقیماً عملکرد یا عملکرد سلولهای مغزی انسان را بررسی و یا دستکاری کنیم. برای فائق آمدن بر این چالش، محققان راهی برای ایجاد ساختارهای بافتی سه بعدی خود سازمان یابنده از #سلولهای_بنیادی پرتوان مشتق از بیماران ایجاد کرده اند.
درک درست فرآیندهای درگیر در تکوین ، سازماندهی و اختلال در عملکرد مغز انسان دشوار بوده است زیرا ما نمی توانیم مستقیماً عملکرد یا عملکرد سلولهای مغزی انسان را بررسی و یا دستکاری کنیم. برای فائق آمدن بر این چالش، محققان راهی برای ایجاد ساختارهای بافتی سه بعدی خود سازمان یابنده از #سلولهای_بنیادی پرتوان مشتق از بیماران ایجاد کرده اند. محققان نشان داده اند که این اسفروئیدهای اختصاصی مناطق مغزی می توانند سال ها حفظ شوند و همین امر اجازه مطالعه مراحل پیشرفته بلوغ و عملکرد مغز را می دهند. این اسفروئیدها می توانند تکوین جنینی مناطق مختلفی از مغز مانند قشر مغز را به خوبی شبیه سازی کنند. در این مطالعه محققین نشان داده اند که اسفروئیدهای مختص هر منطقه از مغز می توانند در کنار یکدیگر قرار گرفته با یکدیگر ادغام شوند و ساختارهای مغزی موسوم به brain assembloids را تولید کنند.
محققان نشان داده اند که این اسفروئیدهای اختصاصی مناطق مغزی می توانند سال ها حفظ شوند و همین امر اجازه مطالعه مراحل پیشرفته بلوغ و عملکرد مغز را می دهند. این اسفروئیدها می توانند تکوین جنینی مناطق مختلفی از مغز مانند قشر مغز را به خوبی شبیه سازی کنند. در این مطالعه محققین نشان داده اند که اسفروئیدهای مختص هر منطقه از مغز می توانند در کنار یکدیگر قرار گرفته با یکدیگر ادغام شوند و ساختارهای مغزی موسوم به brain assembloids را تولید کنند. این ساختارها می توانند برای بررسی فرایندهای تکوین مغزی که پیش از این مطالعه آن ها سخت بود مانند مهاجرت سلولی، ارتباطات سلولی طولانی مدت و تشکیل مدارهای عصبی مورد استفاده قرار گیرند. از این brain assembloids می تواند برای مطالعه بیماری های عصبی روانی مانند اوتیسم، سندرم تیموتی و ... که مکانیسم های مولکولی و سلولی آن ها به خوبی شناخته نشده است استفاده کرد.
این ساختارها می توانند برای بررسی فرایندهای تکوین مغزی که پیش از این مطالعه آن ها سخت بود مانند مهاجرت سلولی، ارتباطات سلولی طولانی مدت و تشکیل مدارهای عصبی مورد استفاده قرار گیرند. از این brain assembloids می تواند برای مطالعه بیماری های عصبی روانی مانند اوتیسم، سندرم تیموتی و ... که مکانیسم های مولکولی و سلولی آن ها به خوبی شناخته نشده است استفاده کرد. Reference:https://medicalxpress.com/news/2020-04-d-tissue-unprecedented-insight-human.html
Reference:https://medicalxpress.com/news/2020-04-d-tissue-unprecedented-insight-human.html -
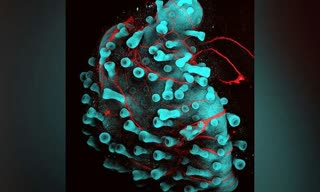
تولید ارگانوئیدهای پوستی حاوی مو به کمک سلول های بنیادی
 ارگانوئیدهای، گروه های سلولی کوچک رشد یافته و سازمان یافته در آزمایشگاه هستند که برای مدل سازی اندام های واقعی طراحی می شوند و در مطالعه ای جدید محققین سعی در ایجاد ارگانوئیدهای پوست داشته اند. آن ها توانسته اند برای اولین بار ارگانوئیدهای پوست انسانی را از سلول های بنیادی پرتوان تولید کنند و این در حالی است که این پوست ها حتی ویژگی مانند داشتن مو را نیز دارا بودند.
ارگانوئیدهای، گروه های سلولی کوچک رشد یافته و سازمان یافته در آزمایشگاه هستند که برای مدل سازی اندام های واقعی طراحی می شوند و در مطالعه ای جدید محققین سعی در ایجاد ارگانوئیدهای پوست داشته اند. آن ها توانسته اند برای اولین بار ارگانوئیدهای پوست انسانی را از سلول های بنیادی پرتوان تولید کنند و این در حالی است که این پوست ها حتی ویژگی مانند داشتن مو را نیز دارا بودند. در این پژوهش محققان توانسته اند با شبیه سازی مراحل تکوینی اولیه پوست انسان، ارگانوئیدهای پوستی را تولید کنند که دارای ضمائم پوستی از جمله فولیکول های مو هستند. دسترسی به این ارگانوئیدهای پوستی می تواند زمینه را برای درک بهتر تکوین پوست و مو هموار کنند و در مطالعات مربوط به ریزش مو کمک کننده باشد.
در این پژوهش محققان توانسته اند با شبیه سازی مراحل تکوینی اولیه پوست انسان، ارگانوئیدهای پوستی را تولید کنند که دارای ضمائم پوستی از جمله فولیکول های مو هستند. دسترسی به این ارگانوئیدهای پوستی می تواند زمینه را برای درک بهتر تکوین پوست و مو هموار کنند و در مطالعات مربوط به ریزش مو کمک کننده باشد. -

بیماری ALS و سلول درمانی

 بیماری ALS یا اسکلروز جانبی آمیوتروفیک ، Amyotrophic lateral sclerosis یا بیماری لوگهریگ یک بیماری نورونهای حرکتی یا MND یا Motor Neuron Disease است که موجب تخریب پیشرونده و غیرقابل ترمیم در دستگاه عصبی مرکزی (مغز و نخاع) و دستگاه عصبی محیطی میشود.
بیماری ALS یا اسکلروز جانبی آمیوتروفیک ، Amyotrophic lateral sclerosis یا بیماری لوگهریگ یک بیماری نورونهای حرکتی یا MND یا Motor Neuron Disease است که موجب تخریب پیشرونده و غیرقابل ترمیم در دستگاه عصبی مرکزی (مغز و نخاع) و دستگاه عصبی محیطی میشود. اسکلروز جانبی آمیوتروفیک شایعترین بیماری نورونهای حرکتی (MND) میباشد که در حقیقت در ALS نشانههای فلج مرکزی و محیطی تواماً ایجاد میشود.
اسکلروز جانبی آمیوتروفیک شایعترین بیماری نورونهای حرکتی (MND) میباشد که در حقیقت در ALS نشانههای فلج مرکزی و محیطی تواماً ایجاد میشود. بروز بیماری دونفر در هر صد هزار نفر میباشد و اغلب افراد بین چهل تا شصت سال را درگیر میسازد. بیماری ماهیت پیشرونده دارد و اغلب بیماران بعد از دو تا پنج سال فوت میکنند ولی گاه دورههای توقف بیماری وجود دارد؛ که باعث میشود ۱۰ درصد از بیماران تا ۱۰ سال زنده بمانند. از آنجایی که این بیماری تنها به اعصاب حرکتی آسیب میرساند، بنابراین هیچ اختلالی در بینایی، بساوایی، شنوایی، چشایی و بویایی فرد به وجود نخواهد آمد و جالب این که اعصاب حرکتی مؤثر در حرکت چشمها و مثانه برای مدتهای طولانی از حمله عامل بیماری مصون خواهند
بروز بیماری دونفر در هر صد هزار نفر میباشد و اغلب افراد بین چهل تا شصت سال را درگیر میسازد. بیماری ماهیت پیشرونده دارد و اغلب بیماران بعد از دو تا پنج سال فوت میکنند ولی گاه دورههای توقف بیماری وجود دارد؛ که باعث میشود ۱۰ درصد از بیماران تا ۱۰ سال زنده بمانند. از آنجایی که این بیماری تنها به اعصاب حرکتی آسیب میرساند، بنابراین هیچ اختلالی در بینایی، بساوایی، شنوایی، چشایی و بویایی فرد به وجود نخواهد آمد و جالب این که اعصاب حرکتی مؤثر در حرکت چشمها و مثانه برای مدتهای طولانی از حمله عامل بیماری مصون خواهند
ماند.
 Riluzole
Riluzole
تنها داروی مورد تائید سازمان غذا و داروی آمریکا برای کنترل و بهبود شرایط بیماران مبتلا به این بیماری است. درمان های رایج و مورد بررسی برای بیماری اسکلروز جانبی آمیوتروفیک:
درمان های رایج و مورد بررسی برای بیماری اسکلروز جانبی آمیوتروفیک:
 درمان با استفاده از آنتاگونیست های گلوتامات که موفق ترین راهکار درمانی در کارآزمائی های بالینی
درمان با استفاده از آنتاگونیست های گلوتامات که موفق ترین راهکار درمانی در کارآزمائی های بالینی
 آنتی اکسیدان تراپی
آنتی اکسیدان تراپی
 راهکارهای ایمنوتراپي
راهکارهای ایمنوتراپي
 استفاده از سلول های بنیادی مزانشیمی مشتق از مغز استخوان
استفاده از سلول های بنیادی مزانشیمی مشتق از مغز استخوان
 استفاده از سلول های بنیادی جنینی و پرتوان القائی
استفاده از سلول های بنیادی جنینی و پرتوان القائی ۳۷ کارآزمائی بالینی از درمان این بیماری با استفاده از سلول های بنیادی مختلف در پایگاه های جستجو کارآزمائی بالینی ثبت شده است که از این میان استفاده از سلول های بنیادی مزانشیمی مشتق از مغز استخوان در فاز 1 و 2 کارآزمائی بالینی در 70 درصد از بیماران بهبود شرایط زندگی و کاهش اثرات پیش رونده را نشان داده است.
۳۷ کارآزمائی بالینی از درمان این بیماری با استفاده از سلول های بنیادی مختلف در پایگاه های جستجو کارآزمائی بالینی ثبت شده است که از این میان استفاده از سلول های بنیادی مزانشیمی مشتق از مغز استخوان در فاز 1 و 2 کارآزمائی بالینی در 70 درصد از بیماران بهبود شرایط زندگی و کاهش اثرات پیش رونده را نشان داده است. Reference:
Reference:
Serhiy Forostyak, et al., Neuroprotective Potential of Cell-Based Therapies in ALS: From Bench to Bedside. Front Neurosci. 2017; 11: 591. -

استفاده از فناوری پرینت سه بعدی برای تولید بافت استخوانی
 پرینت زیستی یک رویکرد نوظهور در تولید زیست موادی مانند هیدروژل است که آن ها را سلول و فاکتورهای رشد ترکیب می کند و از این مخلوط برای تولید ساختارهای شبه بافتی که بافت های طبیعی را تقلید می کنند، استفاده می کند. یکی از کاربردهای این فناوری می تواند طراحی و تولید گرافت های استخوانی با توجه به نیاز فرد باشد، به طوری که بتواند ناحیه آسیب دیده را به خوبی پوشش دهد. پرینت زیستی نیازمند زیست موادی است که بتوانند حامل یا ناقل سلول ها باشد، به خوبی قابل پرینت کردن باشند و بتوانند یک ریز محیط مناسب را برای سلول ها فراهم آورند. اما متاسفانه جوهرهای زیستی موجود از زیست سازگاری، قابلیت پرینت، ثبات ساختاری و عملکردهای مناسب بافتی لازم برخوردار نیستند و به همین دلیل استفاده از آن ها در پیش بالین و بالین با مشکل مواجه است. در پژوهشی جدید، محققان یک جوهر زیستی موسوم به جوهر زیستی در هم تنیدگی یونی-کووالانی مهندسی شده جدید (Nanoengineered Ionic-Covalent Entanglement (NICE)) را تولید کرده اند.
پرینت زیستی یک رویکرد نوظهور در تولید زیست موادی مانند هیدروژل است که آن ها را سلول و فاکتورهای رشد ترکیب می کند و از این مخلوط برای تولید ساختارهای شبه بافتی که بافت های طبیعی را تقلید می کنند، استفاده می کند. یکی از کاربردهای این فناوری می تواند طراحی و تولید گرافت های استخوانی با توجه به نیاز فرد باشد، به طوری که بتواند ناحیه آسیب دیده را به خوبی پوشش دهد. پرینت زیستی نیازمند زیست موادی است که بتوانند حامل یا ناقل سلول ها باشد، به خوبی قابل پرینت کردن باشند و بتوانند یک ریز محیط مناسب را برای سلول ها فراهم آورند. اما متاسفانه جوهرهای زیستی موجود از زیست سازگاری، قابلیت پرینت، ثبات ساختاری و عملکردهای مناسب بافتی لازم برخوردار نیستند و به همین دلیل استفاده از آن ها در پیش بالین و بالین با مشکل مواجه است. در پژوهشی جدید، محققان یک جوهر زیستی موسوم به جوهر زیستی در هم تنیدگی یونی-کووالانی مهندسی شده جدید (Nanoengineered Ionic-Covalent Entanglement (NICE)) را تولید کرده اند. جوهر زیستی NICE ترکیبی از دو فناوری است که به همراه هم موجب تقویت موثرتر این جوهر و تولید ساختارهای قوی تری می شوند. این جوهر زیستی اجازه تولید داربست های قوی می دهد که می توانند در مقیاس مورد نظر و با یک ساختار قابل تحمل برای سلول ها تولید شوند. بارگیری #سلولهای_بنیادی درون این جوهر زیستی برای تولید بافت استخوانی منجر به تولید بافت استخوانی سه بعدی شد که ساختار بافت اسفنجی موجود در استخوان مهره ها را تداعی می کنند. محققین بر این باورند که استفاده از این جوهر زیستی در تولید داربست های استخوانی و بافت های استخوانی می تواند یک رویکرد درمانی موثر برای مشکلات ارتوپدی در آینده ای نزدیک باشد.
جوهر زیستی NICE ترکیبی از دو فناوری است که به همراه هم موجب تقویت موثرتر این جوهر و تولید ساختارهای قوی تری می شوند. این جوهر زیستی اجازه تولید داربست های قوی می دهد که می توانند در مقیاس مورد نظر و با یک ساختار قابل تحمل برای سلول ها تولید شوند. بارگیری #سلولهای_بنیادی درون این جوهر زیستی برای تولید بافت استخوانی منجر به تولید بافت استخوانی سه بعدی شد که ساختار بافت اسفنجی موجود در استخوان مهره ها را تداعی می کنند. محققین بر این باورند که استفاده از این جوهر زیستی در تولید داربست های استخوانی و بافت های استخوانی می تواند یک رویکرد درمانی موثر برای مشکلات ارتوپدی در آینده ای نزدیک باشد.Bio یکی از سایت های معتبر و پرطرفدار پزشکی که بروزترین مطالب رو داره سایت medicalpress هستش..
واقعا سایت خیلی خوبیه..!
پیشنهاد میکنم حتما از مطالبش بچها استفاده کنن نه تنها @تجربیا بلکه تمام @دانش-آموزان-آلاء
میتونین از گوگل ترنسلیت هم برای ترجمه متون استفاده کنین..! -
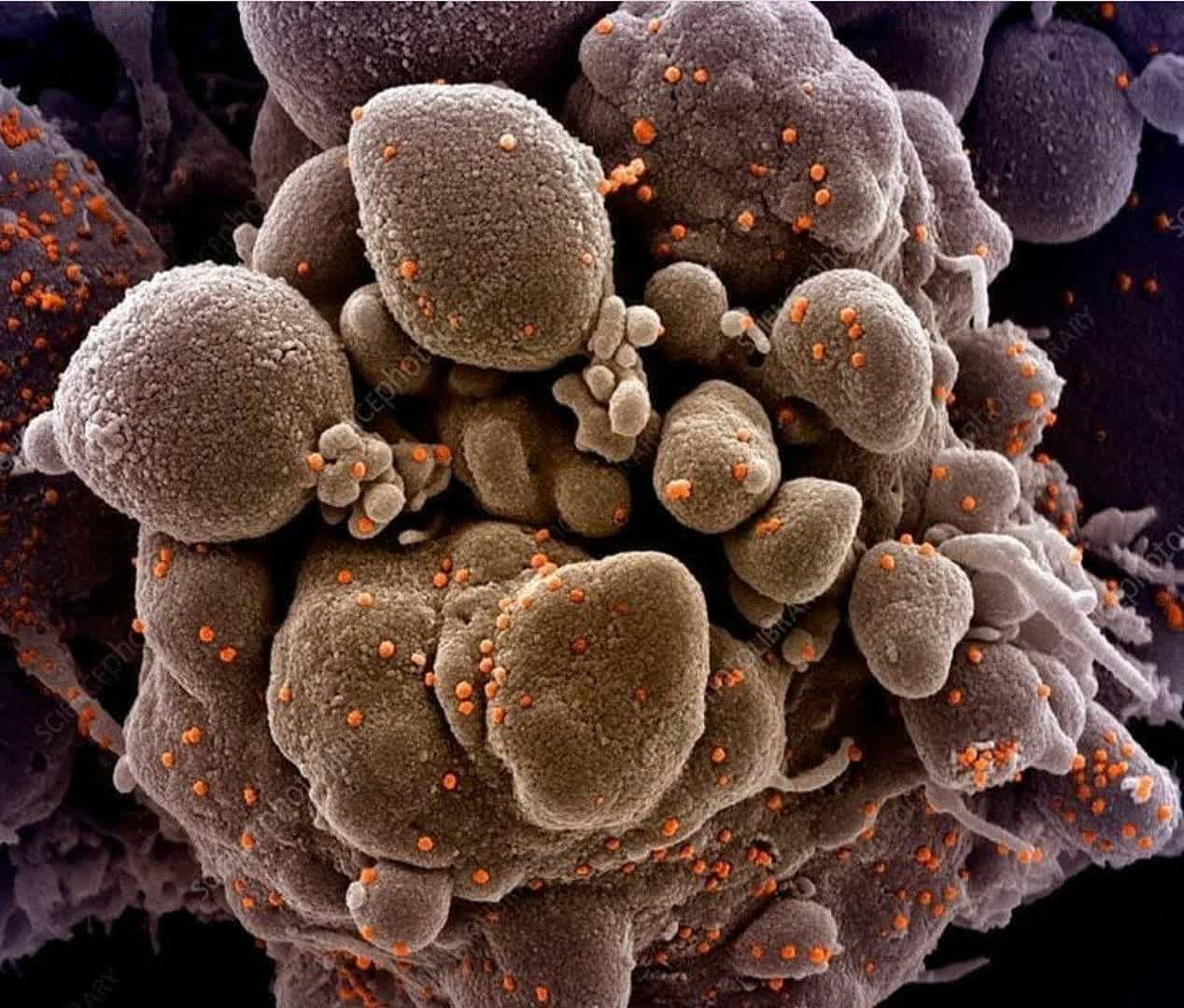
#تصاویر_میکروسکوپی
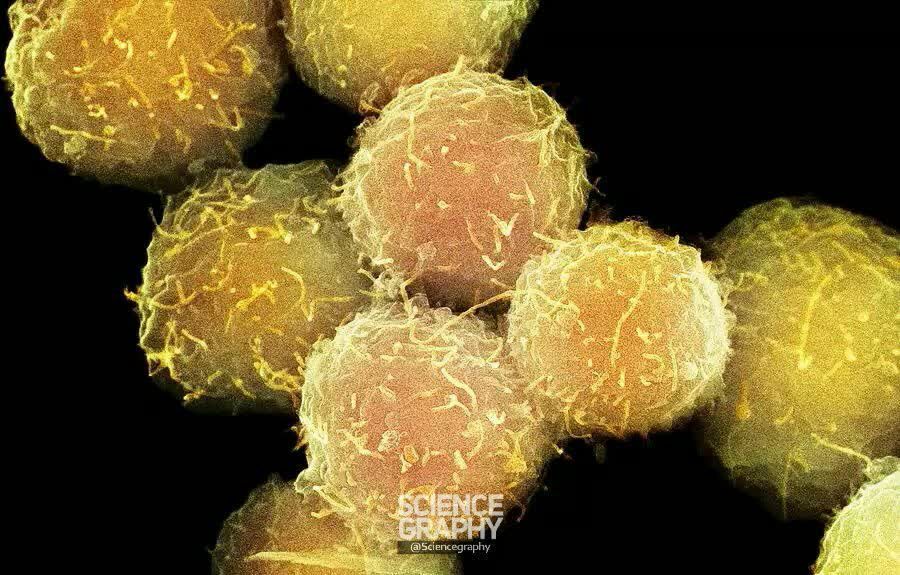
 سلول های آلوده به #کرونا
سلول های آلوده به #کرونا
کوچیکا خود ویروس هستن!
@دانش-آموزان-آلاء -
-
#تصاویر_میکروسکوپی
#سرطان
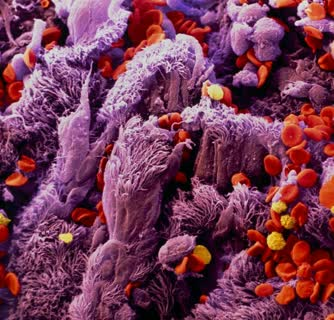
#ریه در تصویر بالا عکس میکروسکوپ الکترونی اپیتلیوم نایژه ریه انسانی که از سرطان رنج می برد ، مشاهده می شود.
در تصویر بالا عکس میکروسکوپ الکترونی اپیتلیوم نایژه ریه انسانی که از سرطان رنج می برد ، مشاهده می شود. این شایع ترین شکل سرطان ریه است که ناشی از استعمال سیگار است. اپیتلیوم یک غشای مخاطی ایجاد می کند که مجاری هوایی ریه را می پوشاند. این شامل توده هایی از مژه های مو مانند (که در اینجا دیده می شود) و سلول های جامی که ترشح مخاط را دارند.
این شایع ترین شکل سرطان ریه است که ناشی از استعمال سیگار است. اپیتلیوم یک غشای مخاطی ایجاد می کند که مجاری هوایی ریه را می پوشاند. این شامل توده هایی از مژه های مو مانند (که در اینجا دیده می شود) و سلول های جامی که ترشح مخاط را دارند. به علت سرطان ، رشد سلول های بی نظم باعث شده این سطح ناهموار شود. سلول های خونی (قرمز) نیز به دلیل خونریزی بیرون آمده اند. رشد سرطانی و سطح ناهموار بدان معنی است که مژه ها ، که بطور معمول برای از بین بردن ذرات به دام افتاده در مخاط ضرب میزنند ، کمتر موثر هستند و راه های هوایی مسدود می شوند.
به علت سرطان ، رشد سلول های بی نظم باعث شده این سطح ناهموار شود. سلول های خونی (قرمز) نیز به دلیل خونریزی بیرون آمده اند. رشد سرطانی و سطح ناهموار بدان معنی است که مژه ها ، که بطور معمول برای از بین بردن ذرات به دام افتاده در مخاط ضرب میزنند ، کمتر موثر هستند و راه های هوایی مسدود می شوند. -

چسب فیبرینی : یا چسب بافتی که حاملی زیستي با منشا انسانی که قابل تخریب بوده و بستر مناسبی برای مهاجرت کراتینوسیتها و نگه داشتن سلول ها در محل ضایعه است و با داشتن خاصیت انعقادی میتواند جلوی خون ریزی و عفونت در منطقه آسیب دیده را کاهش دهد.
 چسب فیبرینی از پلاسمای خون خود فرد یا به صورت تجاری تهیه میشود که البته ممکن است مشکلات انتقال آلودگی ویروسی یا ایجاد التهاب را در پی داشته باشد و اگر از خون بند ناف این چسب را تهیه کرد علایم مذکور رفع میشوند که تولید این محصول از سلول های بنیادی خون بند ناف هم اکنون در مرکز سلول درمانی پژوهشگاه رویان انجام میشود.
چسب فیبرینی از پلاسمای خون خود فرد یا به صورت تجاری تهیه میشود که البته ممکن است مشکلات انتقال آلودگی ویروسی یا ایجاد التهاب را در پی داشته باشد و اگر از خون بند ناف این چسب را تهیه کرد علایم مذکور رفع میشوند که تولید این محصول از سلول های بنیادی خون بند ناف هم اکنون در مرکز سلول درمانی پژوهشگاه رویان انجام میشود. -
#اخبار_جدید_سلولهای_بنیادی
 محققان به دنبال جوان سازی سلول های پیر
محققان به دنبال جوان سازی سلول های پیر محققین در مطالعه ای ، سلول های بنیادی عضلانی موش های پیر را القا کردند تا مجموعه پروتئینی خاصی را بیان کنند که در یک بازه زمانی کوتاه برای تکوین جنینی الزامی هستند و زمانی که آن ها مجددا این سلول ها را به موش های پیر پیوند کردند موجب احیای قدرت آن ها شدند.
محققین در مطالعه ای ، سلول های بنیادی عضلانی موش های پیر را القا کردند تا مجموعه پروتئینی خاصی را بیان کنند که در یک بازه زمانی کوتاه برای تکوین جنینی الزامی هستند و زمانی که آن ها مجددا این سلول ها را به موش های پیر پیوند کردند موجب احیای قدرت آن ها شدند. این پانل پروتئینی که سلول های بنیادی برای بیان آن ها القا شدند فاکتورهای یاماناکا نام دارند که در تولید سلول های بنیادی پرتوان القایی نقش حیاتی را بازی می کنند. این تیم تحقیقاتی در استنفورد نشان دادند که در القای سلول های گرفته شده از انسان های پیر برای بیان فاکتورهای یاماناکا، بسیاری از مشخصه های سلول های پیر معکوس می شوند که این امر منجر به می شود که سلول های بازبرنامه ریزی تا حدی از سلول های جوان قابل تشخیص نباشند.
این پانل پروتئینی که سلول های بنیادی برای بیان آن ها القا شدند فاکتورهای یاماناکا نام دارند که در تولید سلول های بنیادی پرتوان القایی نقش حیاتی را بازی می کنند. این تیم تحقیقاتی در استنفورد نشان دادند که در القای سلول های گرفته شده از انسان های پیر برای بیان فاکتورهای یاماناکا، بسیاری از مشخصه های سلول های پیر معکوس می شوند که این امر منجر به می شود که سلول های بازبرنامه ریزی تا حدی از سلول های جوان قابل تشخیص نباشند. نتایج نشان داد که پیوند این سلول های بازبرنامه ریزی شده به موش های پیر موجب افزایش 20 درصد عمر آن ها در مقایسه با موش های تیمار نشده شد. در واقع ارزیابی های اپی ژنتیکی به عنوان نشانگر سن کرونولوژیک نشان داد که سلول های تیمار شده به طور متوسط در مقایسه با سلول های پیرتر 5/1 تا 5/3 سال جوان تر شده بودند.
نتایج نشان داد که پیوند این سلول های بازبرنامه ریزی شده به موش های پیر موجب افزایش 20 درصد عمر آن ها در مقایسه با موش های تیمار نشده شد. در واقع ارزیابی های اپی ژنتیکی به عنوان نشانگر سن کرونولوژیک نشان داد که سلول های تیمار شده به طور متوسط در مقایسه با سلول های پیرتر 5/1 تا 5/3 سال جوان تر شده بودند. -

 ویتامین ث (اسید آسکوربیک) باعث افزایش تولید سلولهای قلبی از سلولهای بنیادی میشود.
ویتامین ث (اسید آسکوربیک) باعث افزایش تولید سلولهای قلبی از سلولهای بنیادی میشود.
 پژوهشگران پژوهشگاه رویان موفق شدند توانایی تبدیل شدن سلولهای بنیادی جنینی به سلولهای قلبی دارای تپش را با استفاده از ویتامین ث افزایش دهند. این یافته به طور بالقوه میتواند به تهیه سلولهای قلبی از سلولهای بنیادی با بازده بالاتر کمک کند.
پژوهشگران پژوهشگاه رویان موفق شدند توانایی تبدیل شدن سلولهای بنیادی جنینی به سلولهای قلبی دارای تپش را با استفاده از ویتامین ث افزایش دهند. این یافته به طور بالقوه میتواند به تهیه سلولهای قلبی از سلولهای بنیادی با بازده بالاتر کمک کند. آقایان، دکتر تلخابی، دکتر بهاروند، دکتر اقدمی و خانم دکتر پهلوان این پژوهش را طراحی و اجرا کردند.
آقایان، دکتر تلخابی، دکتر بهاروند، دکتر اقدمی و خانم دکتر پهلوان این پژوهش را طراحی و اجرا کردند. لینک دسترسی به اصل مقاله:
لینک دسترسی به اصل مقاله:
http://www.sciencedirect.com/science/article/pii/S0006291X15300528 ویتامین ث یک ویتامین محلول در آب است که در مرکبات نظیر پرتقال به وفور وجود دارد و مصرف آن، کمک شایانی به کارکرد بهتر بدن میکند.
ویتامین ث یک ویتامین محلول در آب است که در مرکبات نظیر پرتقال به وفور وجود دارد و مصرف آن، کمک شایانی به کارکرد بهتر بدن میکند. -
 سلول های بنیادی #پرتوان (نظیر سلول های بنیادی #جنینی و #سلولهای_iPS) اگر مستقیما به بدن تزریق شوند، ایجاد تومور می کنند!
سلول های بنیادی #پرتوان (نظیر سلول های بنیادی #جنینی و #سلولهای_iPS) اگر مستقیما به بدن تزریق شوند، ایجاد تومور می کنند! پژوهشگران هیچ گاه سلول های بنیادی پرتوان را مستقیما به بدن افراد پیوند نمی زنند، چون باعث ایجاد تومور می شوند، در عوض سلول های بنیادی پرتوان را ابتدا به سلول های مدنظر (مثلا سلول های قلبی یا عصبی) تمایز می دهند و سپس سلول های تمایزیافته مشتق از آن ها را به موضع موردنظر پیوند می زنند که دیگر تومورزا نیستند.
پژوهشگران هیچ گاه سلول های بنیادی پرتوان را مستقیما به بدن افراد پیوند نمی زنند، چون باعث ایجاد تومور می شوند، در عوض سلول های بنیادی پرتوان را ابتدا به سلول های مدنظر (مثلا سلول های قلبی یا عصبی) تمایز می دهند و سپس سلول های تمایزیافته مشتق از آن ها را به موضع موردنظر پیوند می زنند که دیگر تومورزا نیستند.
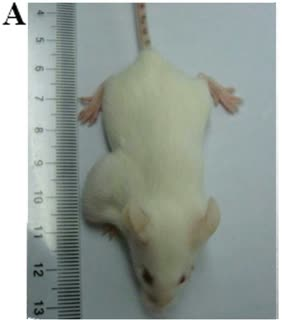
 عکس ضمیمه، تصویر موشی را نشان می دهد که تومور حاصل از پیوند سلول های بنیادی پرتوان را با خود حمل می کند!
عکس ضمیمه، تصویر موشی را نشان می دهد که تومور حاصل از پیوند سلول های بنیادی پرتوان را با خود حمل می کند!










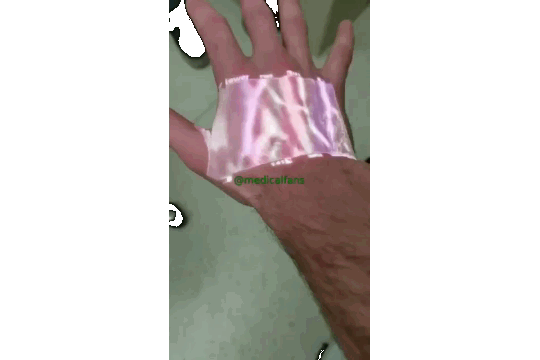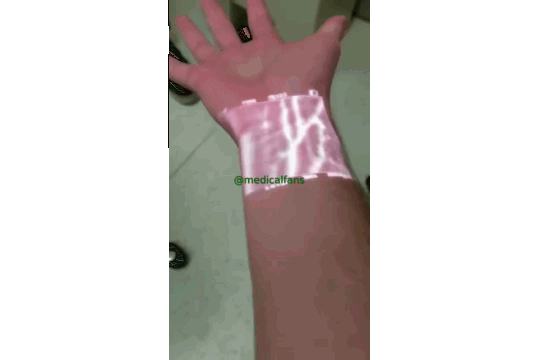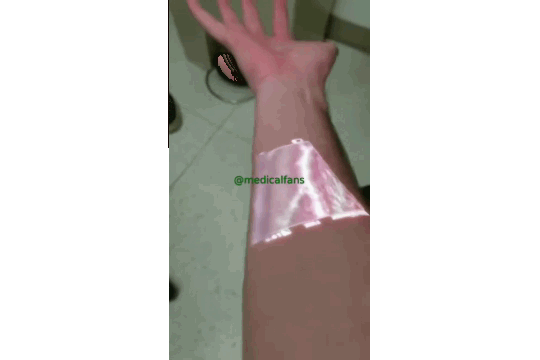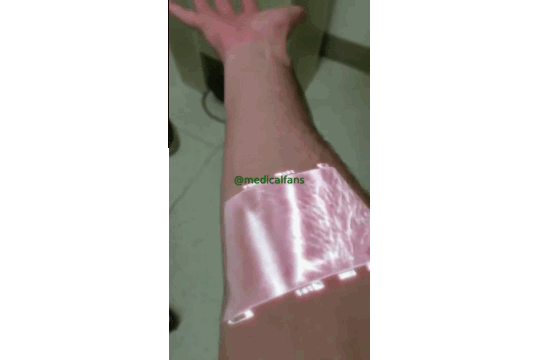
 این فناوری از نور مادون قرمز استفاده می کند ، که توسط خون جذب می شود اما از بافت های اطراف منعکس می شود تا رگ ها تا عمق 15 میلی متر پیدا می کند، و سپس نتایج را بر روی پوست نمایش می دهد.
این فناوری از نور مادون قرمز استفاده می کند ، که توسط خون جذب می شود اما از بافت های اطراف منعکس می شود تا رگ ها تا عمق 15 میلی متر پیدا می کند، و سپس نتایج را بر روی پوست نمایش می دهد.