سلول های بنیادی راهی به آینده
-
در حال حاضر محدودیت های زیادی برای استفاده از سلول های بنیادی با اهداف مختلف از درمان سرطان های خونی گرفته تا اختلالات خونی ارثی وجود دارد که نیازمند پیوند مغز استخوان هستند. سلول های بنیادی خون ساز مسئول خودنوزایی دائمی خون و تولید میلیاردها سلول جدید به صورت روزانه هستند. این سلول های بنیادی خون ساز پتانسیل نامحدودی برای خودنوزایی خودشان در تمام طول عمر فرد دارند و در تمام این مدت انواع مختلف سلول های خون از جمله سلول های ایمنی را تولید می کنند.
با این حال تعداد این سلول ها در مغز استخوان بسیار محدود است و از هر 2500 سلول، یک مورد از آن ها سلول بنیادی خون ساز است. یک راه برای تولید بیشتر سلول های بنیادی خون ساز، یافتن راهی برای افزایش تعداد آن ها در مغز استخوان، جریان خون و خون بند ناف و راه دیگر بازبرنامه ریزی سایر سلول های بنیادی خونی برای تولید سلول های شبه سلول های بنیادی خون ساز است. در این مسیر، محققین از الگوریتمی به نام VIPER برای شناسایی پروتئین هایی که بتوانند سایر سلول های بنیادی خونی را بازبرنامه ریزی کنند استفاده کردند و پروتئینی به نام BAZ2B را شناسایی کردند که قادر است تعداد سلول های بنیادی خون ساز را در خون و خون بند ناف به طور قابل توجهی افزایش دهد.
این پروتئین از طریق بازآرایی مجدد کروماتین عمل می کند و موجب باز شدن مناطق خاصی از ژنوم می شود که پیش از این در دسترس نبودند. پیوند این سلول های بنیادی جدید به مغز استخوان موش هایی که از نظر ایمنی سرکوب شده بودند، کاملا موفقیت آمیز بود. به عقیده محققین پروتئین BAZ2B می تواند مشکل کمبود سلول های بنیادی خون ساز در شرایط درون تنی و هم چنین تکثیر محدود آن ها در شرایط برون تنی را حل کرده و راهگشای استفاده بهتر از آن ها در بالین باشد.
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -

انستیتوی ملی بهداشت و مراقبت انگلستان (NICE) پیش نویس رهنمودهای استفاده از onasemnogene abeparvovec (Zolgensma
 ) برای درمان آتروفی عضلانی نخاع (SMA) در NHS انگلیس منتشر کرد. کنسرسیوم داروهای اسکاتلند (گلاسگو ، اسکاتلند) نیز استفاده از ژن درمانی را که توسط ژن درمانی Novartis (AveXis سابق) ساخته شده است ، تأیید کرده است.
) برای درمان آتروفی عضلانی نخاع (SMA) در NHS انگلیس منتشر کرد. کنسرسیوم داروهای اسکاتلند (گلاسگو ، اسکاتلند) نیز استفاده از ژن درمانی را که توسط ژن درمانی Novartis (AveXis سابق) ساخته شده است ، تأیید کرده است.Meindert Boysen (مرکز ارزیابی فناوری سلامت در NICE) توضیح داد: "SMA یک وضعیت بسیار جدی ، ناتوان کننده و ناراحت کننده است که تأثیرات بسزایی در همه جنبه های زندگی مبتلایان به SMA و خانواده و مراقبان آنها دارد."
دارویی که در حال حاضر توسط NICE برای درمان SMA و SMA نوع 1 ، 2 و 3 قبل از علائم توصیه می شود ، داروی ضد حساسیت الیگونوکلئوتید nusinersen است که باید به طور منظم مصرف شود.
زولگنسما به صورت یک تزریق داخل وریدی تجویز می شود و برای استفاده در نوزادان تا 12 ماهگی با نوع 1 SMA تأیید شده است. در پیش نویس راهنمای NICE همچنین استفاده از زولگنسما در نوزادان دارای SMA پیش از علامت توصیه می شود. برای کودکان 7 تا 12 ماهه ، به دلیل محدود بودن اطلاعات بالینی موجود برای این گروه سنی ، لازم است که یک تیم بالینی چند در مورد نوع درمان آن پژوهش و بررسی کنند.
بویزن نویسنده این پژوهش اذعان داشت: "Zolgensma نشان دهنده یک پیشرفت مهم در درمان SMA است که نه تنها می تواند به کودکان اجازه دهد نقاط عطف مهم مانند نشستن و راه رفتن مستقل را بدست آورند ، بلکه برای برخی از نوزادان که قبل از علائم آنها تشخیص داده می شود ، ممکن است به عنوان یک درمان باشد"
هزینه ژن درمانی برای هر دوز 1.79 میلیون پوند است. بویزن ادامه داد: "همانطور که در بسیاری از روشهای درمانی جدید برای بیماریهای بسیار نادر وجود دارد ، شواهد محدود نشان می دهد که عدم اطمینان در مورد مزایای طولانی مدت زولگنسما وجود دارد."
مارک مک گرگور (کنسرسیوم داروهای اسکاتلندی) نتیجه گیری کرد: "ما انتظار داریم که صنعت داروسازی در جهت بهبود کارایی خود برای ارائه چنین نوآوری های پرهزینه با حداقل هزینه ممکن که برای پایداری سیستم های مراقبت بهداشتی در سراسر جهان ضروری است ، کار کند.
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
محققان دانشگاه اوزاکا (ژاپن) مکانیسم مولکولی را در سلول های بنیادی مغز استخوان کشف کردند که تولید آن ها را پس از شیمی درمانی بهبود می بخشید. این کشف برای اولین بار به تازگی در مجله Experimental Medicineبه چاپ رسیده است.
سلول های بنیادی خونساز (HSPC) باعث ایجاد انواع مختلفی از سلولهای ضروری خون می شود. این سلول ها به دلیل سرعت تقسیم ، به ویژه درمقابل درمان هایی مانند شیمی درمانی آسیب پذیر هستند. با این حال ، HSPC ها پس از آسیب دیدن توانایی بازسازی دارند.
ماسارو ایشی (ماسارو ایشی) (دانشگاه اوزاکا) اظهار داشت: "مغز استخوان عضوی بسیار فعال است زیرا مجبور است به طور مداوم سلول های خونی جدید تولید کند." "هنگامی که عملکرد خود را از دست داد ، مانند زمان شیمی درمانی ، ممکن است شرایط مهلکی مانند کم خونی ، نوتروپنی و خونریزی ایجاد شود. در این مطالعه ، ما می خواستیم درک کنیم که چگونه سلول های بنیادی خون ساز در مغز استخوان پس از آسیب ناشی از شیمی درمانی برای بازیابی عملکرد کامل خود، بازسازی می شوند. "
در مطالعه خود ، این تیم بر سلولهای لنفاوی ذاتی گروه 2 (ILC2s) ( زیرمجموعه سلولهای خونی که توسط HSPC تولید می شوند) تمرکز کرند. این سلول ها ، که برای سیستم ایمنی بدن و ترمیم بافت مهم هستند ، در مغز استخوان یافت می شوند با این حال ، عملکرد دقیق آنها همچنان نامشخص است.
در تلاش برای کشف نقش ILC2 در مغز استخوان ، تیم با استفاده از ماده شیمیایی 5-fluorouracil موش ها را تیمار کردند و سپس پیوند HSPC های آسیب ندیده را در موش ها انجام داد. نتایج نشان داد که HSPC ها تکثیر می یابند و در بازرسی بیشتر مشخص شد که ILC2 ها عامل تحریک کلنی گرانولوسیت-ماکروفاژ (GM-CSF) است که به روند بازسازی HSPC کمک می کند.
این تیم سپس به دنبال این بود که چرا ILC2 ها پس از شیمی درمانی GM-CSF تولید می کنند. با آزمایش های بیشتر ، آنها دریافتند که ILC2 های تولیدی توسط HSPC، با فعالیت اینترلوکین -33 (پروتئینی که توسط سلول های B تولید کننده آنتی بادی پس از آسیب آزاد می شود )، فعال می شوند.
توضیح این مکانیسم پیچیده مولکولی نشان داده است که ILC2s بهبودی HSPC را تسریع می کند و ممکن است به عنوان یک سنسور برای آسیب مغز استخوان عمل کند.
نویسنده این مطالعه ، Takao Sudo (دانشگاه اوزاکا) نتیجه گیری کرد: "این نتایج شگفت زده است که نشان می دهد مغز استخوان پس از شیمی درمانی بازسازی می شود." "نتایج ما ممکن است به توسعه یک رویکرد درمانی جدید برای سرکوب میلوما در اثر شیمی درمانی کمک کند."
Link: https://www.regmednet.com/how-does-bone-marrow-regenerate-following-chemotherapy/
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -

به دنبال همکاری مشترک بین یک گروه مستقر در مرکز تحقیقات سرطان آلمان و آزمایشگاه زیست شناسی مولکولی اروپا (هایدلبرگ ، آلمان) مطالعهای طراحی شد که به استفاده از سلولهای بنیادی القایی (IPSC)برای شناسایی تغییرات ژنتیکی در بیماریها نادر می پرداخت. نتایج این مطالعه که به تازگی در مجله Nature Genetics منتشر شده است، iPSC ها را به عنوان ابزاری بالقوه برای تجزیه و تحلیل انواع تغییرات ژنتیکی و به دنبال آن عملکرد سلول معرفی میکند.
سلولهای بنیادی القایی به سلول هایی گفته می شود که به واسطه فرآیندهای ازمایشگاهی،یک سلول کاملا تمایز یافته همچون سلول پوستی، به یک سلول بنیادی پرتوان تبدیل می شود.این فناوری که در دهه ی اخیر بسیار مورد توجه پژوهشگران قرار گرفته است،دریچه هایی از امید را به در حوزه های تشخیص، درمان گشوده است.
به منظور درک مکانیسم اثر تغییرات ژنتیکی همچون پلی مورفیسمها در بروز بیماریهای وراثتی، تلاشهای قابل توجهی صورت پذیرفت تا مشخص شود که در کدام بافتها می توان این بیماری را با تغییرات فعالیت ژن مرتبط کرد. این آزمایش ها به طور کلی در سلولهای خونی ویا با نمونه برداری از بافت انجام میشود.
الیور استگل (مرکز تحقیقات سرطان آلمان) توضیح داد: "سلولهای بنیادی پرتوان، در بسیاری از موارد برای این منظور مناسب هستند، زیرا آنها تمایز نیافته اند و بنابراین وضعیت اجدادی تمام سلولها را منعکس می کنند." "سلولهای بنیادی به منظور ریشهیابی بیماریهایی که در دوران جنینی رخ میدهند، میتواند موثرتر باشند."
در این مطالعه محققین با بررسی بیش از 1000 دادهی حاصل از توالی یابی سلولهای iPSC، مطالعه گسترده ای بر روی فعالیت بیان ژنی این سلولها انجام دادند. از بین همه ژنهای فعال در iPSC ها ، 67٪ آنها بیان ژنی متفاوتی را در بیماریهای ژنتیکی از خود نشان دادند که عمدتا به بیماریهای خاصی مانند بیماری عروق کرونر قلب و سرطان های ارثی مرتبط بودند.
مارک جان باندر ، نویسنده این تحقیق، اظهار داشت: "ما تعداد زیادی از ارتباطات بین زمینه بیماری ژنتیکی با بیان ژن در سلولهای iPSC گزارش کردیم و از این حجم زیاد تنوع شگفتزده شدیم" باندر ادامه داد: "چنین آزمایشاتی پیشتر غیرممکن بود، زیرا هیچ مجموعه کافی از ترانسکریپتوم مرجع از سلولهای iPSC وجود نداشت." این گروه در حال بررسی پتانسیل آنالیز ترانسکریپتوم iPSC برای ارزیابی تأثیر تغییرات ژنتیکی در تمایز سلولی هستند استفاده کرد."
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
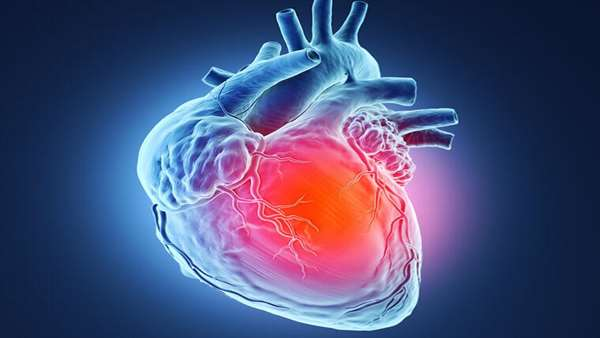
دانشمندان در موسسه تحقیقات پزشکی mount sinani آمریکا نشان داده اند که دسته ای از سلول های بنیادی مشتق شده از جفت که تحت عنوان سلول های cdx2 مثبت شناخته می شوند، می توانند سلول های قلبی را پس از حمله قلبی در مدل های حیوانی کاملا بازسازی کنند. تا قبل از این به نظر می رسید که سلول های cdx2 تنها مسئول تولید جفت در مراحل ابتدایی تکوین جنین هستند و توانایی بازسازی سایر ارگان ها را ندارند.نتایج حاصل از این آزمایش بسیار شگفت انگیز و خیره کننده بود زیرا در هیچ یک از آزمایشات بالینی که تا به حال بر روی درمان های قلبی انسان صورت گرفته، هیچ نوع سلول دیگری در پتری دیش به صورت سلول های قلبی دارای ضربان نبوده است و نکته جالب این بود زمانیکه این سلول ها به جریان خون تزریق می شدند به طرز هوشمندانه ای می دانستند که باید به کجا روند! این نتایج می تواند مسیر پزشکی بازساختی ارگان های دیگر را نیز هموار کند.
https://www.pnas.org/content/116/24/11786
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -

محققان یک روش عمیق و از نظر مقیاس انعطاف پذیر برای هدایت الگوی ولومتریک بیان ژن در بافت های مصنوعی سه بعدی ارائه کرده اند که در آن از مبدل های حرارتی ترموفلوئیدیک برای فعال کردن رونویسی استفاده می کند، رویکردی که آن را به اختصار HEAT می نامند. این روش انتقال حرارت مبتنی بر مایع را در شبکه های چاپ شده در بافت ها اعمال می کند تا تراریخته های قابل القا توسط گرما بیان شونده توسط سلول های تعبیه شده را فعال کند.
محققان نشان داده اند که الگوی بیان ژن می تواند هم از نظر فضایی و هم از نظر پویایی بوسیله ساختارهای مشبک کانال دار متنوع، دمای مایع، جهت جریان مایع و زمان تحریک تنظیم شود. آن ها از این رویکرد برای فعال سازی بیان مکانی و سه بعدی لیگاندهای پروتئین Wnt و تنظیم کننده های Wnt/β-catenin مسیر استفاده کرده اند که از مسیرهای پیام رسانی کلیدی و موثر در تکوین، هموستازی، بازسازی و سرطان در تمام جانوران است.
Reference:https://advances.sciencemag.org/content/6/40/eabb9062
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
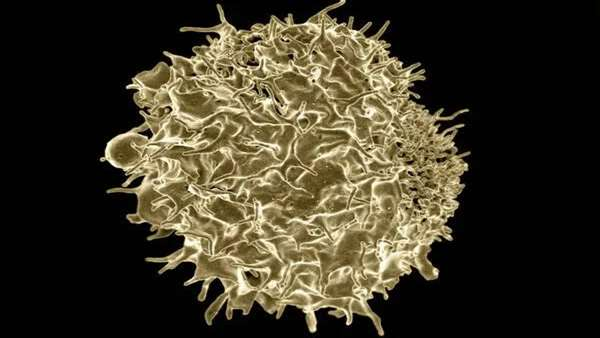
سلول های T برای حفاظت از بدن در برابر عفونت ها و سرطان حیاتی هستند و در این مطالعه جدید محققین روش جدیدی به نام CLInt-Seq را معرفی کرده اند که تکنیک های موجود برای جمع آوری و توالی یابی ژنتیکی سلول های T را به هم ترکیب می کند. بدن ما روزانه میلیون ها میلیون سلول T را تولید می کند و هر کدام از این سلول ها، گیرنده اختصاصی خود را برای شناسایی یک آنتی ژن خاص دارا است. یک گیرنده سلول T ممکن است یک آنتی ژن ویروسی را شناسایی کند که منجر به یک سرماخوردگی معمولی می شود و یک گیرنده دیگر ممکن است آنتی ژنی را شناسایی کند که مربوط به سلول سرطان سینه است. زمانی که سلول T با آنتی ژن مواجه می شود و گیرنده اش آن را شناسایی می کند، شروع به پاسخ می کند که این امر با تولید نسخه های بیشتر از خودش و هم چنین تحریک سایر سلول های ایمنی برای مقابله با آنتی ژن نمود پیدا می کند.
محققین در سراسر دنیا بدنبال روش هایی هستند که سلول های T با گیرنده های هدف قرار دهنده سرطان یا ویروسی مانند SARS-CoV-2 را جداسازی و تکثیر کنند و در ادامه به منظور تقویت سیستم ایمنی بیماران، آن ها را به بیماران بازگردانند. مشکلی که وجود دارد این است که اغلب جمعیت های سلولی که ما به آن ها دسترسی داریم، در خون محیطی شکل می گیرند یا از نمونه هایی بدست می آیند که در سایر بخش های بدن انسان وجود دارند و در نتیجه سلول های T با گیرنده مد نظر به ندرت در این جمعیت ها وجود دارند و باید به دنبال راهی برای برای جداسازی و شناسایی موثر آن ها بود. اغلب روش ها منجر به جمع آوری سلول های T می شود که دارای ناخالصی هستند. اما روشی مانند CLInt-Seq می تواند منجر به شناسایی سلول های T شود که گیرنده های مد نظر محققین را دارا هستند. جداسازی این سلول ها با گیرنده اختصاصی اولین گام محسوب می شود. برای استفاده موثر از این سلول های جداسازی شده، نیاز به آنالیز آن ها با استفاده از توالی یابی mRNA مبتنی بر قطره(droplet) یا Drop-seq است که می تواند بیان mRNA را به طور هم زمان در هزاران سلول منفرد اندازه گیری کند. زمانی که بتوانیم توالی گیرنده سلول T مد نظر را شناسایی کنیم، می توانیم از آن برای ایجاد درمان های موثرتر علیه سرطان، ویروس و ... استفاده کنیم.
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
غضروف مفصلی با داشتن تنها چند میلی متر ضخامت نقش حیاتی را در سیستم عضلانی اسکلتی بازی می کند و مسئول حرکات نرم فرد است. اما مشکلی که وجود دارد این است که در صورت آسیب دیدگی این بخش، بازسازی آن به خوبی صورت نمی گیرد و نیازمند به ایجاد یک درمان موثر برای آن هستیم.
در سال های اخیر تمایل زیادی به استفاده از زیست مواد مختلف برای احیای عملکرد غضروف بوده است، هر چند که نتایج امیدوار کننده ای بدست آمده است اما هیچ کدام قادر نبوده اند که عملکرد غضروفی را تا سطح طبیعی احیا کنند. دکتر سیلیوا نورنبرگر و همکارانش در دانشگاه وین دریافته اند که ماتریکس طبیعی غضروف به عنوان یک زیست ماده برای بهبودی بازسازی غضروف موثر است. به عقیده آن ها، ماتریکس آسلولار شده غضروف می تواند محیط بهینه ای را برای سلول های غضروفی یا سلول های بنیادی فراهم آورد. آن ها این غضروف آسلولار را CartiScaff نامیده اند و نشان داده اند که می تواند موجب تشکیل بافت غضروفی جدید و کارآمد شود.
https://www.thelancet.com/journals/ebiom/article/PIIS2352-3964(20)30572-7/fulltext
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -

محققان دو سیگنال سلولی به نام های Ccr5 و Cxcr6 را با استفاده از مدل های تخریب شبکیه در انسان و موش شناسایی کرده اند. آن ها سلول های بنیادی را برای بیش بیان گیرنده های Ccr5 و Cxcr6 مهندسی ژنتیک کردند. زمانی که این سلول های بنیادی مهندسی شده مجددا به مدل های جانوری پیوند شدند، نرخ بسیار بالایی از مهاجرت به بافت شبکیه در حال تخریب را نشان دادند که مانع از مرگ سلول های آن و حفظ عملکرد شبکیه شد.
این سلول های بنیادی مشتق از مغز استخوان و تغییر یافته زمانی که به شبکیه رسیدند با لایه های آن تلفیق شدند و موجب حفظ عملکرد شبکیه شدند. به عقیده محققین استفاده از سلول های بنیادی تغییر یافته می تواند رویکرد موثری برای احیای بینایی و جلوگیری از تخریب شبکیه باشد.
https://medicalxpress.com/news/2020-12-retinal-transplant-boost-door-eyesight.html
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -

دکتر سيد حسين احمدی تفتی فوق تخصص جراحی قلب در ارتباط با پروژه توسعه فناوری های تکثیر، نگه داشت و پرورش موش های دارای بیماری ام اس گفت: ﭘﺮوژه اي ﮐﻪ در ﺣﺎل ﺣﺎﺿﺮ در کشور اﺟﺮا شده، ﺑﺮاي اوﻟﯿﻦ ﺑﺎر اﻗﺪام ﺑﻪ ﺗﻮﻟﯿﺪ ﻣﻮش M.S ﻧﻤﻮده اﺳﺖ ﮐﻪ اﯾﻦ ﭘﺮوژه ﯾﮑﯽ از ﻣﻬﻤﺘﺮﯾﻦ ﺷﺎﺧﺼﻪﻫﺎ و ﭘﯿﺸﺮﻓﺖﻫﺎ در زﻣﯿﻨﻪ اﻣﻮر ﺗﺤﻘﯿﻘﺎﺗﯽ در ﮐﺸﻮر، ﻣﻨﻄﻘﻪ و ﺟﻬﺎن ﺑﺸﻤﺎر می آید و ﻗﺎدر ﺧﻮاﻫﺪ ﺑﻮد ﺑﺮاي ﮐﺸﻮر ﻋﺰﯾﺰﻣﺎن ﺳﺮﺑﻠﻨﺪي و اﻓﺘﺨﺎر را ﺑﻪ ارﻣﻐﺎن آورد و ﺑﺘﻮاﻧﺪ ﮐﺸﻮر ﻣﺎ را در رده ﮐﺸﻮرﻫﺎي ﺑﺰرگ دﻧﯿﺎ در ﻣﻄﺎﻟﻌﻪ و درﻣﺎن اﯾﻦ ﺑﯿﻤﺎري ﻗﺮار دﻫﺪ. هم اکنون در جهان تنها 3 کمپانی بزرگ بر روی توليد موشهاي ام اس فعالیت می کنند که با توجه به انحصاری بودن و عدم انتقال تکنولوژی و روش تولید نیز کلیه پروژههای تحقیقاتی را تنها در مراکز خود بانجام می رسانند. همچنين با توجه به رشد روز افزون مبتلایان به اين بیماري و هزینههاي سنگين درمان، محققیقن و اساتید خبره در این زمینه را بر این خود باوری قرار داد که بتوانيم در کشور خود اين مدل حیوان را تولید و در اختیار محققین و اساتید کشور برای انجام پروژههای ملی برای درمان این بیماری قرار دهیم.
ﺷﯿﻮع بیماری ام.اس در زﻧﺎن اﯾﺮاﻧﯽ طی پنج سال گذشته ﺳﻪ ﺑﺮاﺑﺮ شده اﺳﺖ ﻫﻤﭽﻨﯿﻦ ﺷﯿﻮع اﯾﻦ ﺑﯿﻤﺎري در ﺑﯿﻦ زﻧﺎن اﯾﺮان ﺑﯿﺶ از ﻣﯿﺎﻧﮕﯿﻦ ﺟﻬﺎﻧﯽ اﺳﺖ ﺑﻪ ﻃﻮرﯾﮑﻪ اﯾﻦ ﺑﯿﻤﺎري در ﺑﯿﻦ زﻧﺎن ايراني نسبت به ﺳﺎﯾﺮ ﮐﺸﻮرﻫﺎ ﺷﯿﻮع دو ﺑﺮاﺑﺮي دارد. همچنين این بیماری اکنون بیشتر در نسلهای جوان ديده شده و این تیم متخصص در ﮐﺸﻮر را بر اين باور قرار داد که ﺑﺎ روﯾﮑﺮد دﻗﯿﻖ اﻗﺪام ﺑﻪ ﺗﻮﻟﯿﺪ اﯾﻦ ﻣﻮشﻫﺎ ﺑﺮاي اﻧﺠﺎم آزﻣﺎﯾﺸﺎت ﺑﺮ روي اﯾﻦ ﺑﯿﻤﺎري نمایند.
ﮐﺸﻮر ﻋﺰﯾﺰ ﻣﺎ ﮐﻪ از ﻟﺤﺎظ ﭘﯿﺸﺮﻓﺖ ﻋﻠﻤﯽ ﺑﻌﻨﻮان ﻗﻄﺐ ﻋﻠﻤﯽ ﻣﻨﻄﻘﻪ ﺷﻨﺎﺧﺘﻪ ﻣﯽ ﺷﻮد ﻧﯿﺎز ﻣﺒﺮم ﺑﻪ ﺗﻮﻟﯿﺪ اﯾﻦ ﺣﯿﻮاﻧﺎت ﺑﺮاي ﺑﺮرﺳﯽﻫﺎي ﺑﺎﻟﯿﻨﯽ اﯾﻦ ﺑﯿﻤﺎري ﺗﻮﺳﻂ ﻣﺤﻘﻘﯿﻦ ﮐﺸﻮر دارد و اﯾﻦ ﮔﺮوه ﺗﺤﻘﯿﻘﺎﺗﯽ ﺑﺎ ﺗﺠﺮﺑﻪ ﻋﻠﻤﯽ و ﭼﻨﺪﯾﻦ ﺳﺎل ﺑﺮرﺳﯽ ﺑﺮوي اﯾﻦ ﭘﺮوژه ﻫﻢ اﮐﻨﻮن اﻗﺪام ﺑﻪ ﺗﻮﻟﯿﺪ اﯾﻦ ﺣﯿﻮاﻧﺎت در اﯾﺮان ﻧﻤﻮد ﮐﻪ اﯾﻦ ﺧﻮد ﯾﮏ ﮔﺎم ﺑﻠﻨﺪ ﺑﺮاي اﻓﺘﺨﺎر آﻓﺮﯾﻨﯽ و ﺳﺮﺑﻠﻨﺪي اﯾﺮان ﻋﺰﯾﺰﻣﺎن ﻣﯽ ﺑﺎﺷﺪ.
ﺑﯿﻤﺎرﯾﻬﺎي ﺻﻌﺐ اﻟﻌﻼج از ﺟﻤﻠﻪMS ﮐﻪ ﺑﻪ دﻧﺒﺎل ﺳﻠﻮلﻫﺎي ﻋﺼﺒﯽ در ﺑﺪن اﻧﺴﺎن ﻫﺴﺘﻨﺪ ﺗﺎ ﺑﺘﻮاﻧﻨﺪ ﺑﻪ آﻧﻬﺎ ﺣﻤﻠﻪ ﮐﺮده و آنها را از ﺑﯿﻦ ﺑﺒﺮﻧﺪ و روشﻫﺎي ﺧﺎص درﻣﺎﻧﯽ ﻧﯿﺰ ﮐﻪ ﺑﺮاي ﻣﺒﺎرزه ﺑﺎ آن وﺟﻮد دارد، ﻣﺜﻞ اﯾﺠﺎد ﯾﮑﺴﺮي ﻧﺎﻧﻮذرات از ﭘﺮوﺗﺌﯿﻦﻫﺎي آﻧﺘﯽ ﺑﺎدي ﮐﻪ ﺧﻮد ﭘﺮوﺗﺌﯿﻦﻫﺎي ﺳﯿﺴﺘﻢ اﯾ ﻤﻨﯽ ﺑﺪن ﻣﯽ ﺑﺎﺷﺪ. اﯾﻦ ﻧﺎﻧﻮ ذرات ﻣﻐﻨﺎﻃﯿﺴﯽ ﻗﺎدر ﺧﻮاﻫﻨﺪ ﺑﻮد ﺑﻪ ﺳﻠﻮلﻫﺎي ﻋﺼﺒﯽ ﻣﺘﺼﻞ و ﺑﺮاﺣﺘﯽ ﻣﯽ ﺗﻮان آنها را ﺑﺎ اﺳﺘﻔﺎده از MRI رد ﯾﺎﺑﯽ ﻧﻤﻮد اﯾﻦ در ﺣﺎﻟﯽ اﺳﺖ ﮐﻪ اﯾﻦ آزﻣﺎﯾﺸﺎت ﻣﯽ ﺑﺎﯾﺴﺘﯽ در ﻣﺮاﺣﻞ اوﻟﯿﻪ ﺑﺮ روي ﺣﯿﻮاﻧﺎت آزﻣﺎﯾﺸﮕﺎﻫﯽ ﻣﻮرد ﻣﻄﺎﻟﻌﻪ و ﺗﺤﻘﯿﻖ ﻗﺮار ﮔﯿﺮد.
ﭘﺮوژه اي ﮐﻪ اﺟﺮا ﮔﺮدید ﺑﺮاي اوﻟﯿﻦ ﺑﺎر در اﯾﺮان اﻗﺪام ﺑﻪ ﺗﻮﻟﯿﺪ ﻣﻮشﻫﺎي ام اس ﻧﻤﻮده اﺳﺖ ﮐﻪ اﯾﻦ ﭘﺮوژه ﯾﮑﯽ از ﻣﻬﻤﺘﺮﯾﻦ ﺷﺎﺧﺼﻪﻫﺎ و ﭘﯿﺸﺮﻓﺖﻫﺎ در زﻣﯿﻨﻪ اﻣﻮر ﺗﺤﻘﯿﻘﺎﺗﯽ در ﮐﺸﻮر، ﻣﻨﻄﻘﻪ و ﺟﻬﺎن ﺑﺸﻤﺎر ﺧﻮاﻫﺪ آﻣﺪ و ﻗﺎدر ﺧﻮاﻫﺪ ﺑﻮد ﺑﺮاي ﮐﺸﻮر ﻋﺰﯾﺰﻣﺎن اﯾﺮان ﺳﺮﺑﻠﻨﺪي و اﻓﺘﺨﺎر را ﺑﻪ ارﻣﻐﺎن آورد و ﺑﺘﻮاﻧﺪ ﮐﺸﻮر ﻣﺎ را در رده ﮐﺸﻮرﻫﺎي ﺑﺰرگ دﻧﯿﺎ در ﻣﻄﺎﻟﻌﻪ و درﻣﺎن اﯾﻦ ﺑﯿﻤﺎري ﻗﺮار دﻫﺪ. ﻫﻢ اﮐﻨﻮن اﺳﺘﺎنﻫﺎي اﺻﻔﻬﺎن، ﺗﻬﺮان و ﻗﻢ ﺑﯿﺸﺘﺮﯾﻦ ﺷﯿﻮع ﺑﯿﻤﺎري ام.اس را در ﮐﺸﻮر ﺑﻪ ﺧﻮد اﺧﺘﺼﺎص داده اﻧﺪ.
برای تولید اصولی و اساسی بیماری M.S در این طرح مدل موشهای C57/BL6 به عنوان مدل بین المللی انتخاب شده است .
در آغاز سال بعد از گروه بندی حیوانات در هر مرحله تزریق را بروی 30 سر موش C57/BL6 را آغاز نموده و گروههای اصلی و گروه بندیهای پشتیبان را آماده و در هر هفته تزریق 30 سر از این حیوانات انجام شد. همچنین بعد از تزریق نیز می بایستی این حیوانات در هر قفس انفرادی ایزوله(فیلتردار) نگهداری و علامتهای بالینی حیوانات بصورت دائم مانیتورینگ شود و نتایج بررسی نیز بصورت گزارش کامل نگارش شود.
در روش توليد و پرورش اين موشهاي M.S مي بايستي نکات مهمي را در نظر داشت و همچنين مي بايستي پروتکلهاي تعريفي ابتدائي مهمي را براي آنها تعريف و اجرا نمود همچنين اين نکته نيز مي بايستي مد نظر قرار گیرد که براي آزمايش بروي موشهاي M.S مي بايستي دو گروه شاهد و پشتيبان انتخاب کرد اين بدين معني است که ما براي هر مرحله از آزمايش خود نياز به 60 سر از اين حيوانات داشتیم که اين خود اهميت و بزرگي اين پروژه نزد محققين را نشان مي دهد همچنين اين نکته نيز لازم بذکر است در زمان آزمايشات تحقيقاتي با توجه به حساسيت بالاي اين پروژه و امکان آلودگي اين حيوانات انجام کليه تحقيقات و آزمايشات بروي اين موشها در محل ايزوله که خود داراي سیستم کلین رومهای حیوانی مي باشد انجام و همچنين موشها هر کدام در قفس هاي مجزا بصورت انفرادي نگهداري و محيط و محققين کار بروي اين حيوانات در يک محيط کلين روم انجام گرفت که ما کليه عمليات ساختماني و اجرائي پروژه را از ابتدا با اين نگرش آغاز نموده و محيط خود را با سطح ايمني بالا براي انجام تحقيقات بروی اين حيوانات آماده نمودیم.
با توجه ﺑﻪ ﺗﻤﺎﻣﯽ ﻣﺒﺎﺣﺚ ذﮐﺮ ﺷﺪه اﯾﻨﺠﺎﻧب ﺑﺎ ﻫﻤﮑﺎري ﺗﯿﻢ ﻣﺘﺨﺼﺺ و ﻣﺠﺮب اﯾﻦ ﻃﺮح را اﺟﺮا ﻧﻤﻮده و ﺑﺎ ﺗﻮﺟﻪ ﺑﻪ اﯾﻨﮑﻪ در ﮐﺸﻮر ﻋﺰﯾﺰﻣﺎن اﯾﺮان ﻃﺮح ﺗﻮﻟﯿﺪ ﻣﻮشﻫﺎي MS ﺑﺮاي ﭘﺮوژهﻫﺎي ﺗﺤﻘﯿﻘﺎﺗﯽ ﺑﺮوي اﯾﻦ ﺑﯿﻤﺎري ﺑﺴﯿﺎر ﺿﺮوري ﻣﯽ ﺑﺎﺷﺪ اﻣﯿﺪوارﯾﻢ ﺑﺘﻮاﻧﯿﻢ ﺑﺎ اﻫﺪاف ﻣﺸﺨﺺ و ﮐﺎرﺑﺮد آن در ﻧﯿﺎزﻫﺎﯾﯽ ﮐﻪ در ﺑﺨﺶﻫﺎي ﻣﺨﺘﻠﻒ از ﺟﻤﻠﻪ ﭘﺰﺷﮑﯽ و درﻣﺎن و ﺗﻮﻟﯿﺪ دارو برای اﯾﻦ ﺑﯿﻤﺎري وﺟﻮد دارد و ﺑﺎ ﺗﻮﺟﻪ ﺑﻪ دﯾﺪﮔﺎه و ﺳﻨﺪ ﭼﺸﻢ اﻧﺪاز 1404 و ﻫﻤﭽﻨﯿﻦ ﺣﻤﺎﯾﺖﻫﺎي ﻣﺴﺌﻮﻟﯿﻦ دﻟﺴﻮز و ﻧﮕﺮش ﻣﺴﺌﻮﻟﯿﻦ ﻣﺤﺘﺮم درﺗﺤﻘﯿﻘﺎت و ﭘﯿﺸﺮو ﺑﻮدن در زﻣﯿﻨﻪﻫﺎي ﻣﺨﺘﻠﻒ ﻋﻠﻤﯽ در دﻧﯿﺎ ﺑﺘﻮاﻧﯿﻢ در اﯾﻦ ﭘﺮوژه ﻣﻠﯽ ﯾﮏ اﻓﺘﺨﺎر دﯾﮕﺮ ﮐﺴﺐ و ﺑﺰرﮔﯽ ﺑﺮاي ﮐﺸﻮر ﻋﺰﯾﺰﻣﺎن اﯾﺮان ﺑﻪ ارﻣﻐﺎن ﺑﯿﺎوریم.
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -

طی یک تحقیق مشترک بین دانشگاه علوم پزشکی هاروارد و دپارتمان فیزیک و تکنولوژی مسکو، برای اولین بار اقدام به استفاده از رباتها در جهت بهینه سازی کشت سلول و ساخت ارگانوئیدها نمودند.
این تحقیق که در مجله Translational Vision Science & Technologyبه چاپ رسید، برای اولین بار از ربات ها و دانش یادگیری ماشین اقدام به کشت سلول های رتینوئید (retina cells) نمودند که در نتیجه تعداد سلول تولید شده و بازدهی آنها افزایش یافت.
این تیم تحقیقاتی به منظور مقایسه عملکرد ربات ها با انسان، دو گروه مجزا برای مقایسه انتخاب نمودند که در یکی از آنها کشت توسط کاربر و در گروه دوم کلیه مراحل توسط رباتها انجام شد.
به جهت بررسی بازدهی هرگروه، سلولهای کشت شده توسط لیبلهای رنگی فلورسانس نشانه گذاری شدند. سپس محققان به اسکن چاهکهای کشت سلول به کمک فناوری پردازش تصویر و زبان برنامه نویسی پایتون پرداختند.
این برنامه قادر است تا قسمت هایی از چاهک کشت سلول را تشخیص دهد که بیشترین میزان رنگ فلورسانس در آن دیده میشود و از انجایی که پروتئین لیبل شده فقط در سلولهای رتینوئید ایجاد میشود، میتوان ادعا کرد که در نواحی با میزان بازتابی بالای رنگ فلورسانس، کشت سلول به خوبی صورت پذیرفته است. همچنین این شناسایی در ارزیابی موفقیت آمیز بودن رشد و بقا ارگانوئید موثر است.
مطابق این تحقیق استفاده از الگوریتمهای اتوماتیک و سیستمهای رباتی، به کمک ایجاد مکانیسم های تحریکی رشد سلولها را ارتقا می بخشد. این سیستم هوشمند باعث شد تا میزان زمان مصرفی پژوهشگر برای کشت سلول را از 2 ساعت به 34 دقیقه کاهش دهد.
در پایان مجری این پروژه اذعان داشت که این روش میتواند افق روشنی از هوشمند سازی در دنیای زیست شناسی باشد چرا که با کشت سلول در مقیاسهای بزرگ و تمایز آنها به سلولهای گوناگون به صورت پربازده (High-Throughput) بستر مناسبی برای بررسی اثرات دارویی و پیوند سلول فراهم میگردد. کشت هوشمند سلولها نه تنها موجب افزایش دقت میشود بلکه هزینههای انسانی را نیز کاهش داده و به دنبال آن محصول بیشتری را تولید میکند.
https://www.regmednet.com/robot-grown-cells-help-to-achieve-faster-organoid-growth-and-selection/
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
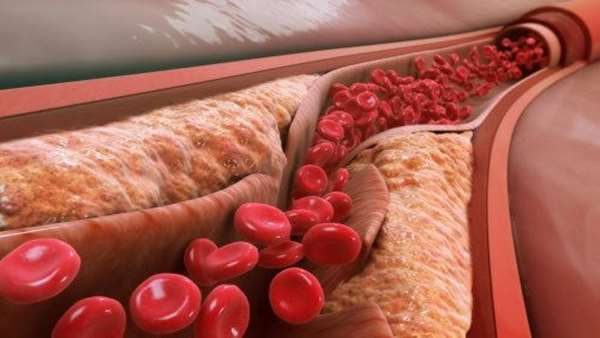
تولید سلول های پیش ساز عروقی القا شده(iVPCs)، به عنوان انقلابی در درمان بیماری های عروقی ایسکمیک معرفی شده اند. این سلول های پیش ساز عروقی القا شده را می توان با استفاده از فاکتورهای رونویسی موسوم به ETS(E-twenty six)، Etv2 و Fli1 تولید کرد.
این سلول ها که حاصل تبدیل مستقیم رده ای هستند و طی کشت های طولانی مدت و در مقیاس وسیع به سلول های سرطانی تبدیل نمی شوند و به همین دلیل می توان آن ها را منبع سلولی مناسبی برای تولید عروق خونی مورد نیاز برای بافت های انسانی پرینت شده سه بعدی مانند قلب و کبد در نظر گرفت. محققین کره ای نشان داده اند که پیوند iVPCs به مدل جانوری ایسکمی اندام حرکتی عقبی موجب تقویت جریان خون می شود و این در حالی است که هیچ توموری شکل نمی گیرد و به همین دلیل می توان آن ها را ابزار درمانی مناسبی برای درمان بیماری های عروقی ایسکمیک در نظر گرفت.
Reference: https://www.ahajournals.org/doi/10.1161/ATVBAHA.119.313684
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
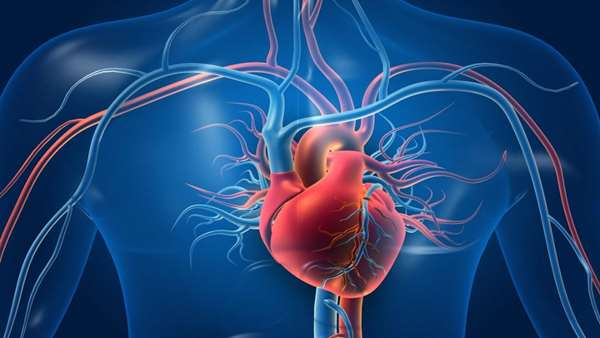
محققان توانسته اند با استفاده از یک فاکتور رونویسی مزودرمی موسوم به Brachyury سلول های بنیادی سازگار برای ترمیم قلبی را تولید کنند. آن ها نشان داده اند که می توان با ترانسفکشن Brachyury با استفاده از تکنیک mRNA مدیفه شده و میکرو کپسوله شده، سلول های بنیادی مزانشیمی معمولی را به سمت سرنوشت قلب سازی پیش برد.
این در حالی است که پیش از این محققین روش ها و پروتکل های چند مرحله ای را برای این امر پشنهاد کرده بودند که زمان بر و هزینه بر بودند و کارایی زیادی نیز نداشتند. اما استفاده از این رویکرد جدید می تواند مسیر تولید سلول های قلب ساز در آزمایشگاه و استفاده از آن ها در بالین را کوتاه سازد.
Reference: https://stemcellsjournals.onlinelibrary.wiley.com/doi/full/10.1002/sctm.20-0193
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
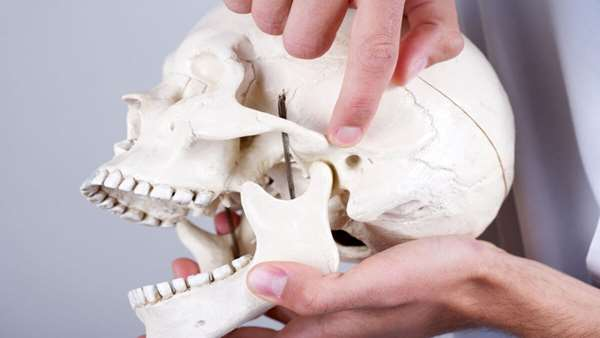
مفصل گیجگاهی-مفصلی(TMJ) که بخش پشتی آرواره پایین را شکل می دهد و آرواره را به جمجمه متصل می کند از نظر آناتومیک پیچیده بوده و با توجه به این که بار زیادی را تحمل می کند از استخوان و غضروف تشکیل شده است. تنها در ایالات متحده حدود 10 میلیون نفر دچار مشکلات مفصل TMJ هستند. درمان فعلی شامل تزریق استروئیدها (برای تسکین درد) و جراحی های بازسازی کننده با استفاده از پروتزها یا بافت های اهدایی است که اغلب قادر به ترمیم مفصل نیستند.
محققین راه حل این مشکل را مهندسی گرافت های غضروف-استخوان TMJ می دانند که دقیقا با شرایط گیرنده یا بیمار از نظر زیستی و آناتومیک مطابقت داشته باشند. در مطالعات جانوری آن ها سلول های بنیادی را از بافت چربی جانور گرفته و آن ها را کشت داده و تکثیر کردند و در ادامه آن ها را برای تمایز به غضروف و سلول های استخوان ساز القا کردند. با الهام گرفتن از تصاویر گرفته شده از نقص در TMJ، آن ها بلوک های از ماتریکس استخوانی که از نظر هندسه و شکل شبیه ناحیه آسیب دیده بود را تولید کردند. در ادامه سلول های استخوان ساز روی این داربست ها کشت داده شدند. این داربست ها درون بیوراکتورها قرار داده شدند تا از رشد سلول ها درون بلوک ها حمایت شود. نتیجه امر تولید بلوک های مفصلی با شکلی دقیقا شبیه ناحیه آسیب دیده مفصل TMJ بود که می تواند نیازهای جانور(و در آینده انسان) را تامین کند.
Reference: https://medicalxpress.com/pdf521882010.pdf
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
پژوهشگران پیش از این مولکولی به نام JNK3 را کشف کرده بودند که یک عامل کلیدی برای افزایش حساسیت سلول های بنیادی کودکان به محیط شان و بازسازی بهترشان در مقایسه با بالغین بود. این کشف تا حدی توضیح می دهد که چرا کودکان ترمیم استخوان سریع تری در مقایسه با بزرگسالان دارند. بر مبنای این یافته آن ها بیوماده جدیدی را تولید کردند که ساختار بافت استخوانی را تقلید می کند و حاوی نانوذراتی است که JNK3 را فعال می کند.
تست این زیست ماده روی مدل های پیش بالینی نشان داد که این زیست ماده می تواند یک ماه بعد از استفاده نواقص استخوانی بزرگ را سریع تر درمان کند و التهاب را کاهش دهد. این زیست ماده جدید در مقایسه با زیست مواد بارگیری شده با داروها به طور بی خطرتر و موثرتری استخوان را ترمیم می کند و عوارض جانبی مربوط به آن ها را نیز ندارد.
Reference:https://www.sciencedirect.com/science/article/pii/S0142961220307869?via%3Dihub
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
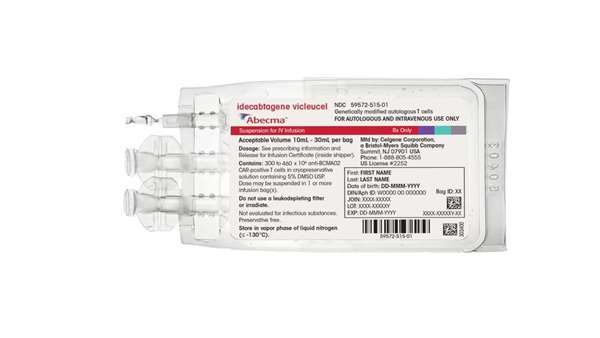
ژندرمانی مبتنی بر سلول Abecma (idecabtagene vicleucel) شرکت سلژن کورپوریشن (زیرمجموعه شرکت بریستول میرز اسکوییب) برای درمان بیماران بزرگسال مبتلا به ملتیپل مایلوما که بیماری آنها به دستکم چهار درمان مختلف پاسخ نداده یا بیماری آنها پس از دریافت این درمانها بازگشته است، تائیدیه سازمان غذا و دارو آمریکا (FDA) را دریافت کرد
ژندرمانی مبتنی بر سلول Abecma نخستین ژندرمانی مبتنی بر سلول تائید شده توسط FDA برای درمان ملتیپل مایلوما است.
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
چگونه بیماریهای بدخیم با روشهای نوین درمان میشود؟!
روشهای درمانی پیشرفتهای که مبتنی بر فناوری سلولهای بنیادی است، درمان بیماریهای مهلک و صعبالعلاجی چون سرطان را از پای در میآورند.
نامش هم که برده میشود، لرزه بر اندام میاندازد و نگرانی میآورد. سرطان، که بلای جان جهان شده و در انواع گوناگونی تکثیر یافته، به یکی از مشکلات نظام سلامت در تمامی کشورهای دنیا بدل شده است.
از میان تمامی سرطانها، تومورهای بدخیم مغزی معمولا به درمان پاسخ مناسبی نشان نمی دهند و یا به علت موقعیت خاص قرارگیری در مغز، دارورسانی یا تابش پرتو به آنها با مشکل مواجه می شود. بنابراین، میزان مرگ و میر در مبتلایان به تومورهای بدخیم مغزی بیشتر و درمان آنها با مشکلات بیشتری مواجه است.
استفاده از سلولها علیه سلولها
پیشرفتهای دانشی و فناورانه در سالهای اخیر به ویژه در حوزه سلولهای بنیادی، موجب شده است تا درمان بیماران سرطانی نیز ابعادی تازه را تجربه کند.
استفاده از سلول های ایمنی برای درمان تومورهای مغزی بارقههای امید به درمان را در این بیماران و سایر مبتلایان به سرطان افزایش دهد. این کار توسط دانشگاهها و شرکتهای دانشبنیان داخلی آغاز شد و فناوری جداسازی و فعالسازی سلولهای ایمنی توسط فناوران کشور به دست آمد. با این فناوری، هدفگیری سلول های تومور مغزی در محیط آزمایشگاه و نیز مدل های پیش بالینی ممکن شد.
نتایج پژوهشهای پیش بالینی و بالینی در مراکز پژوهشی و تحقیقاتی کشور از جمله پژوهشگاه رویان برای بیماران مبتلا به تومور مغزی شد. به استحصال موفقیتآمیز سلولهای ایمنی در شرایط کاملا تمیز منجر شد. سلول های کشنده طبیعی از خون دهندگان جداسازی و تقویت می شدند تا بتوانند سلول توموری را هدف گیری کنند. پس از تایید صحت و سلامت سلول ها، سلولها به بیماران تزریق شد و عوارض ناشی از تزریق این سلول ها در بیماران بررسی می شد تا ایمنی این روش درمانی مورد ارزیابی قرار بگیرد.
نتیجه بررسی این نوع درمان بر پنج بیمار مبتلا به تومور مغزی گلیوبلاستوما نشان داد که کاربرد این سلول ها ایمن است و عوارضی برای بیمار ندارد. در حال حاضر پژوهشگاه رویان تحقیق برای استفاده از این سلول ها در هدف گیری سلول های توموری در سرطان تخمدان و ملانوما را در دست اجرا دارد. چنانچه در این زمینه نیز نتایج موفقیت آمیز باشد، انجام کارآزمایی های بالینی برای نوع پیشرفته از سرطان تخمدان و سرطان بدخیم پوستی آغاز خواهد شد.
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -
در حالی که واکسیناسیون گسترده بهترین راه برای مقابله با پاندمی COVID-19 محسوب می شود اما قطعا نیاز به درمان هایی که بتوانند ویروس را مهار کنند یا بیماری را درمان کنند هیچ گاه منتفی نخواهد شد. این پروتئین یک واریته از ACE2( آنزیم مبدل آنژیوتانسین 2) است که گیرنده ای برای ورود کروناویروس به سلول های انسانی است. این پروتئین سنتزی با پروتئین اسپایک یا S ویروس کرونا برهمکنش می کند و با اتصال به آن مانع از اتصال ویروس به گیرنده ACE2 واقعی در غشای سلولی می شود. این پروتئین در ارگانوئیدهای کلیوی انسانی تست شد و مشاهده شد که بخوبی می تواند به صورت رقابتی مانع از آلودگی سلول های کلیوی به ویروس کرونا شود. گام بعدی مطالعه انجام فازهای بالینی استفاده از این پروتئین برای تایید ایمنی و کارایی آن خواهد بود.
https://medicalxpress.com/news/2021-02-protein-neutralizes-covid-tiny-human.html
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -

دانشمندان دانشکده پزشکی وارویک در دانشگاه وارویک (کاونتری ، انگلستان) کشف کرده اند که کاهش سلول های پیش ساز قطره در پوشش رحم ممکن است منجر به ناتوانی بارداری به صورت مکرر شود. این تحقیق که اخیراً در مجله STEM CELLS منتشر شده است، مدعی است که با مهار این نقصان میتوان مانع از بروز این ناباروریها شد.
در طی یک بارداری معمولی ، پوشش رحم، که به عنوان آندومتر شناخته می شود کاملاً خود را بازسازی میکند. به دنبال این فرآیند ، سلولهای استرومایی آندومتر به سلولهای جداگانه و ویژهای تبدیل میشوند که قابلیت انعطاف پذیری رحم را فراهم و رشد سریع جنین را ممکن میسازد.
لذا برای مقابله با این موضوع، در ابتدا تیم Brosnens گروهی از سلولهای مزانشیمی بسیار تکثیر یافته (hPMC) موجود در پنجره کاشت جنین را شناسایی کردند تا به عنوان هدف درمانی، مورد توجه قرار گیرند.
همچنین نویسنده این مقاله اذعان داشت: "یافته های ما نشان میدهد که hPMC از سلولهای بنیادی مشتق شده از مغز استخوان بوده که به طور متناوب در گردش بوده و در زمان کاشت جنین در پوشش رحم ورود پیدا میکنند. لذا به نظر میرسد این سلولها در حاملگی بسیار مهم هستند تا بتوانند جفتی را که به سرعت در حال رشد است جای دهند. ما همچنین دریافتیم که این سلولهای نادر اما بسیار متخصص در پوشش رحم زنان باردار مکرر وارد می شوند."
بنابراین این نتایج نشان می دهد که hPMC نقش مستقیمی در تشکیل یک ارتباط قوی بین مادر و جنین دارد.
Siobhan Quenby (از دانشگاه وارویک) ، یکی از محققین این پژوهش اینگونه بیان داشت که: "این یافته ها بسیار هیجان انگیز است." "ما قبلاً نشان داده ایم که میتوانیم این سلولهای بسیار تکثیر یافته را در پوشش رحم قبل از بارداری افزایش دهیم. این یافتههای جدید نشان میدهد که چرا این سلولهای بسیار تکثیر یافته برای جلوگیری از سقط جنین و احتمالاً زایمان زودرس (دو اختلال ویرانگر بارداری که بسیاری از زنان و زوجها را در سراسر جهان تحت تأثیر قرار می دهد) میتوانند مهم باشند. "
https://www.regmednet.com/depleting-decidual-precursor-cells-linked-with-pregnancy-loss/
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470 -

بیماری Batten به دلیل جهش در ژن CLN3 رخ می دهد که روی کروموزوم 16 قرار دارد. اغلب کودکان مبتلا به این بیماری بخشی از ژن شان از بین رفته است که همین امر مانع از تولید پروتئین های خاص می شود. از دست رفتن بینایی در اوایل چهار سالگی شروع می شود و روی یادگیری و رفتار فرد نیز اثراتی را بر جای می گذارد و آن ها در نهایت بین سنین 15 تا 30 سالگی می میرند.
به خوبی مشخص شده است که از دست رفتن بینایی در لیپوفوشینوز سروئید عصبی ناشی از تخریب بافت های حس کننده نور در شبکیه است. با این حال یکی از موانع مطالعه از دست رفتن بینایی در بیماری Batten این است که مدل های موشی جهش در ژن CLN3، نمی توانند تخریب شبکیه یا از دست رفتن بینایی را در انسان ها به خوبی تقلید کنند و ارزیابی بافت چشم بعد از مرگ نیز به دلیل تخریب گسترده سلول های شبکیه برای مطالعه بافت چشم مناسب نیست. یک ابزار مناسب برای مطالعه بیماری Batten استفاده از سلول های خود بیمار است. محققین در دانشگاه روچستر سلول های پوستی بیماران را به سلول های بنیادی پرتوان القایی انسانی بازبرنامه ریزی کردند. در ادامه این سلول ها به سلول های شبکیه ای تمایز داده شده اند که دارای جهش CLN3 بودند.
با استفاده از این مدل سلولی انسانی جدید، برای اولین بار نشان داده شده است که عملکرد مناسب CLN3 برای ساختار سلول های اپی تلیوم رنگ دانه دار شبکیه لازم است. این لایه اپی تلیومی برای تغذیه سلول های گیرنده نوری شبکیه ضروری است و در نتیجه برای حفظ بقا و عملکرد آن ها نیز حیاتی است. درک این امر که عملکرد نامناسب سلول های اپی تلیومی رنگ دانه دار شبیکه می تواند منجر به از دست رفتن سلول های گیرنده نوری در بیماری باتن شود می تواند گام اولیه ای در جهت درمان این بیماری باشد.
Reference:https://medicalxpress.com/news/2021-02-vision-loss-batten-disease.html
اینجا

 میتونی بی واسطه با سلول های بنیادی حرف بزنی!
میتونی بی واسطه با سلول های بنیادی حرف بزنی!

https://forum.alaatv.com/post/1396470









 🧫
🧫