سلول های بنیادی راهی به آینده
-
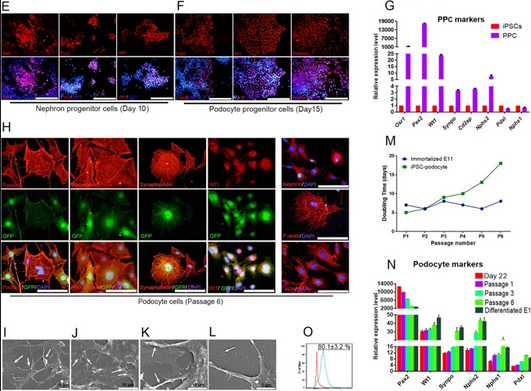
محققان پژوهشگاه رویان و همکارانشان در راستای درمان آسیبهای وارده به نفرون از پودوسیتهای حاصل از تمایز سلولهای بنیادی پرتوان القایی در رفع عارضه «پروتئینوریا» (ترشح پروتئین در ادرار) در مدل آزمایشگاهی استفاده کردند.(2)به منظور یافتن روشی برای درمان آسیبهای وارده به نفرون به دنبال از دست رفتن پودوسیتها، دکتر حسین بهاروند، دکتر ناصر اقدمی، دکتر رضا مقدسعلی، امین احمدی، دکتر نصیری، دکتر رهبر قاضی و همکارانشان در پژوهشگاه رویان، دانشگاه تهران و دانشگاه علوم پزشکی تبریز، پژوهشی را طراحی کردند که طی آن ابتدا با تزریق آنتیبادی علیه پودوسیت به حیوان آزمایشگاهی (موش) و تخریب این سلولها مدل آزمایشگاهی پروتئینوریای شدید ساخته شد؛ سپس پودوسیتها در شرایط آزمایشگاهی از تمایز سلولهای بنیادی پرتوان القایی موش تولید و به مدلهای آزمایشگاهی بیماری پیوند زده شدند.
نتایج این پژوهش که در نشریه بینالمللی Scientific Reports به چاپ رسیده است، نشان داد، پیوند پودوسیتهای دارای عملکرد مشتق از سلولهای بنیادی پرتوان القایی به مدل آزمایشگاهی، باعث جایگیری سلولهای مذکور در گلومرولهای آسیب دیده و منجر به بهبودی پروتئینوریا و تغییرات بافت ایجاد شده، میشود.
نتایج این پژوهش شواهدی را فراهم کرد که نشان میدهد بهکارگیری سلولهای کلیوی مشتق از سلولهای بنیادی پرتوان القایی میتواند به عنوان یک استراتژی درمانی مناسب برای بیماریهای گلومرولی مطرح باشد.
-
محققان پژوهشگاه رویان در راستای کمک به درمان مبتلایان به دیابت موفق به تمایز سلولهای بنیادی پرتوان انسانی به سلولهای پیشساز پانکراس، سلولهای مزانشیمی و سلولهای اندوتلیالی و پیوند شبه بافتهای تولید شده در مدل حیوانی شدند.(1)
نتایج این پژوهش نشان می دهد امکان تولید شبه بافت تولید کننده انسولین در بازه زمانی کوتاه و با هزینه مناسب در شرایط آزمایشگاهی وجود دارد و با پژوهش های بیشتر می توان از این روش در درمان مبتلایان به دیابت استفاده کرد. -
محققان پژوهشگاه رویان در راستای کمک به درمان مبتلایان به دیابت موفق به تمایز سلولهای بنیادی پرتوان انسانی به سلولهای پیشساز پانکراس، سلولهای مزانشیمی و سلولهای اندوتلیالی و پیوند شبه بافتهای تولید شده در مدل حیوانی شدند.(2)
دیابت نوع یک، اختلالی در سیستم ایمنی است که با تخریب سلولهای موجود در جزایر لانگرهانس لوزالمعده، منجر به کاهش ترشح انسولین و بالا رفتن قند خون میشود. با وجود تجویز انسولین، تنظیم دقیق قند خون در بیماران امکانپذیر نیست و در دراز مدت عوارضی مانند مشکلات قلبی عروقی، اختلالات کلیوی، مشکلات بینایی، زخم در پا و … ایجاد میشود که در مواردی جان بیمار را تهدید میکند.برای غلبه بر این مشکل، جدا کردن جزایر لانگرهانس از بیماران مرگ مغزی و پیوند آن به بیماران دیابتی بهعنوان روش درمانی پیشنهاد و انجام شد، اما کمبود اهدا کننده مانع از گسترش و همه گیر شدن این روش درمانی شده است.
-
محققان پژوهشگاه رویان در راستای کمک به درمان مبتلایان به دیابت موفق به تمایز سلولهای بنیادی پرتوان انسانی به سلولهای پیشساز پانکراس، سلولهای مزانشیمی و سلولهای اندوتلیالی و پیوند شبه بافتهای تولید شده در مدل حیوانی شدند.(3)
تولید سلولهای انسولینساز در شرایط آزمایشگاهی می تواند کمبود اهدا کننده را جبران کند، امکان همهگیر شدن این درمان را فراهم کند، اما تولید سلول انسولین ساز دارای عملکرد در شرایط آزمایشگاهی دشوار و پرهزینه است و پیوند آنان نیز با مشکلاتی مانند تأمین اکسیژن کافی روبه روست.به منظور غلبه بر این مشکل دکتر حسین بهاروند، دکتر یاسر تهمتنی، آناهیتا سلطانیان و همکارانشان در پژوهشگاه رویان در پژوهشی سلولهای بنیادی پرتوان انسانی را به سلولهای پیشساز پانکراس، سلولهای مزانشیمی و سلولهای اندوتلیالی تمایز دادند. سپس این سه رده سلولی را در شرایط خاص و با نسبت مشخص در کنار هم کشت دادند. سه رده سلولی به صورت خودبهخودی سازمان یافته شکل سه بعدی و منسجمی یافتند. سپس این شبه بافتهای تولید شده در شرایط آزمایشگاهی به حیوان مدل پیوند زده شد تا توان ایجاد عروق و تولید انسولین توسط آنان بررسی شود.
نتایج این پژوهش که در مجله بینالمللی Cellular Physiology به چاپ رسیده است، نشان داد، شبه بافتها در بدن حیوان مدل تمایز مییابد، دارای عروق خونی میشود و انسولین انسانی تولید و ترشح میکنند.
#ایرانی
-
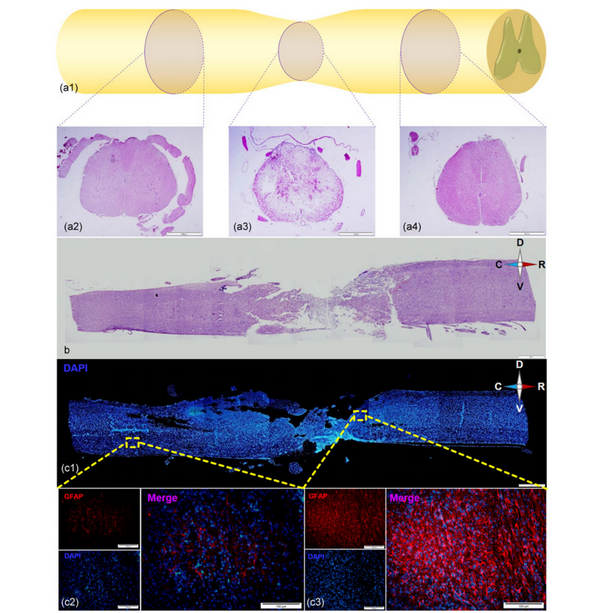
یافته جدید پژوهشگران ایرانی در ترمیم ضایعات نخاعی(1)یافته های تحقیق پژوهشگران ایرانی حاکی از اثربخشی بالای استفاده از کلرید لیتیم به تنهایی یا همزمان با پیوند سلولهای بنیادی عصبی در ترمیم ضایعات نخاعی در حیوان مدل آزمایشگاهی است.درمان ضایعات نخاعی سالها یکی از اهداف پژوهشگران علوم سلولی بوده است. تلاشهای متعددی برای ترمیم نخاع آسیب دیده و بازیابی توان حرکتی مبتلایان صورت گرفته اما هیج یک منجر به درمان قطعی این عارضه نشده اند.
#ایرانی
-

یافته جدید پژوهشگران ایرانی در ترمیم ضایعات نخاعی(2)
سلولدرمانی همواره به عنوان یک روش درمانی برای درمان ضایعات نخاعی مطرح بوده است. کلرید لیتیم نیز به عنوان مادهای موثر در بهبود وضعیت نخاع و افزایش واسطههای عصبی شناخته میشود. به منظور یافتن روشی برای ترمیم ضایعات نخاعی، دکتر سحر کیانی، دکتر حسین بهاروند، عطیه محمد شیرازی، هدی صدرالسادات، راضیه جابری، زهرا نقدآبادی، دکتر مهدی فردمنش و همکارانشان در پژوهشگاه رویان، دانشگاه تربیت مدرس و دانشگاه صنعتی شریف، پژوهشی را طراحی کردند که طی آن اثر پیوند سلولهای بنیادی عصبی در کنار استفاده از کلریدلیتیم بر زندهمانی، تقسیم و تمایز سلول ها در مدل آزمایشگاهی (رت) دارای ضایعه نخاعی مورد بررسی قرار گرفت.#ایرانی
-

یافته جدید پژوهشگران ایرانی در ترمیم ضایعات نخاعی(3)
در این پژوهش ابتدا در حیوانات مدل آزمایشگاهی ضایعه نخاعی ایجاد شد. سپس مدلهای ایجاد شده به چهار گروه تقسیم شدند: گروه کنترل که هیچ درمانی دریافت نمیکرد، گروهی که سلولهای بنیادی عصبی به آنان پیوند زده شد، گروهی که کلرید لیتیم دریافت میکرد و گروهی که پیوند سلولهای بنیادی عصبی و کلرید لیتیم را همزمان دریافت میکرد.براساس این تحقیق که در مجله بینالمللی Cellular Physiology ارائه شده گروهی که سلولهای بنیادی عصبی و کلرید لیتیم را همزمان دریافت کرده بود و گروه دریافت کننده کلرید لیتیم به تنهایی، به صورت معنیداری در توان حرکتی خود بهبود یافتند. همچنین بررسیهای بافت شناسی نشان داد، سلولهای بنیادی عصبی پیوند شده تمایز یافته و در طول نخاع مهاجرت کردهاند. علاوه بر این، سلولهای بیان کننده نستین در گروه دریافت کننده کلرید لیتیم به شکل معنیداری بیشتر از سایر گروهها تقسیم و تکثیر یافته بودند.
نتایج این پژوهش نشان داد، استفاده از کلرید لیتیم به تنهایی یا همزمان با پیوند سلولهای بنیادی عصبی بهترین اثر را در ترمیم و بازیابی توان حرکتی مدلهای دچار ضایعه نخاعی و القاء ترمیم درونزاد دارد.
#ایرانی
دانش-آموزان-آلاء
تجربیا -
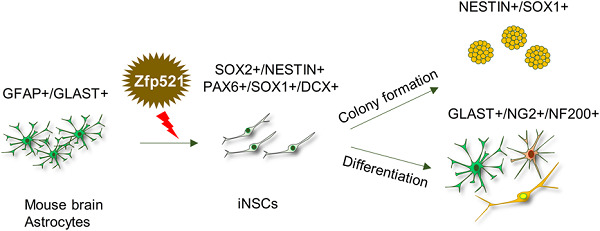
موفقیت محققان رویان در تولید سلولهای بنیادی عصبی از سلول های ستاره ای با تنها یک عامل القایی(1)تحقیقات محققان پژوهشگاه رویان نشان میدهد پروتئین هستهای Zfp521 به تنهایی برای تبدیل آستروسیتهای بالغ برداشت شده از مغز به سلولهای بنیادی عصبی القایی کافی است.
تلاشهای بسیاری برای ترمیم ضایعات وارد شده به دستگاه عصبی مرکزی و بیماریهای فرسایشی سیستم عصبی صورت گرفته، اما هنوز درمانی قطعی برای این مشکلات یافت نشده است.
یکی از سلولهای پرشمار در دستگاه عصبی مرکزی آستروسیتها (سلولهای ستارهای) هستند. خصوصیات این سلولها باعث شده است که بهعنوان منبع مناسبی برای تولید سلولهای بنیادی عصبی به شمار روند. با این وجود همچنان تلاشها برای تولید سلولهای بنیادی عصبی از آستروسیتها با تنها یک عامل القایی و بدون محرکهای خارجی به نتیجه مطلوب نرسیده بود.
#ایرانی -

موفقیت محققان رویان در تولید سلولهای بنیادی عصبی از سلول های ستاره ای با تنها یک عامل القایی(1)
برای غلبه بر این مشکل، دکتر حسین بهاروند، دکتر سحر کیانی، معصومه زارعی خیرآبادی و همکارانشان در پژوهشگاه رویان، پژوهشی را طراحی کردند که نشان داد پروتئین هستهای Zfp521 به تنهایی برای تبدیل آستروسیتهای بالغ برداشت شده از مغز به سلولهای بنیادی عصبی القایی کافی است.نتایج این پژوهش که در مجله بینالمللی Cellular Physiology به چاپ رسیده است، نشان داد، سلولهای بنیادی عصبی القایی که با استفاده از پروتئین Zfp521 از آستروسیتها ایجاد شدند به مدت طولانی توان خودنوزایی خود را حفظ کردند، چندتوان بودند و میتوانستند از سلولهای گوناگون دستگاه عصبی تمایز یابند. علاوه بر این، کشت تنها یکی از این سلولهای بنیادی عصبی حاصل، منجر به ایجاد کلنی در شرایط کشت آزمایشگاهی میشد.
این پژوهش نشان داد میتوان از Zfp521 برای تبدیل آستروسیتها به سلولهای بنیادی عصبی در بدن فرد (In Vivo) پس از ایجاد ضایعات عصبی با هدف درمانی استفاده کرد.
#ایرانی
دانش-آموزان-آلاء
تجربیا -

گوش، مناسبترین بافت برداشت سلولهای بنیادی در ترمیم ضایعات غضروفی(1)با توجه به تعدد منابع تأمین سلولهای بنیادی مزانشیمی، این که کدام نوع از این سلولها برای ترمیم ضایعات غضروفی مناسبتر هستند، سوالی است که پاسخ به آن حائز اهمیت خواهد بود.
پژوهشهای بالینی فراوانی در خصوص استفاده از سلولهای بنیادی مزانشیمی در ترمیم ضایعات غضروفی صورت گرفته است.
با هدف پاسخ به این سوال، دکتر اسلامی نژاد، محمد علی خلیلی فر، دکتر قاسم زاده، دکتر بهاروند و همکارانشان در پژوهشگاه رویان و دانشگاه علوم پزشکی بابل، پژوهشی را طراحی کردند که طی آن سلولهای بنیادی مزانشیمی از مغز استخوان، بافت چربی و گوشهای خرگوش برداشت شد و در شرایط آزمایشگاهی کشت و تکثیر یافتند.
سرعت تکثیر و توان تمایزی این سلولها به سلولهای غضروفی (کندروسیت) و ایجاد تجمعات غضروفی با روشهای آزمایشگاهی بررسی و مقایسه شد. سپس، به منظور مقایسه توان ترمیمی، ضایعه غضروفی در حیوان مدل آزمایشگاهی (خرگوش) ایجاد و سلولهای بنیادی مزانشیمی ذکر شده در داربست کلاژنی به محل ضایعه پیوند زده شد.
#ایرانی -

گوش، مناسبترین بافت برداشت سلولهای بنیادی در ترمیم ضایعات غضروفی(2)
نتایج این پژوهش که در مجله بینالمللی یاخته (cell journal) به چاپ رسیده است، نشان داد، با آنکه سلولهای بنیادی مزانشیمی برداشت شده از بافت چربی بالاترین سرعت تکثیر را دارند اما نسبت تمایز به کندروسیت در آنان پایین است. سلولهای بنیادی مزانشیمی برداشت شده از گوش بهترین بازده را در سرعت تکثیر و تمایز به کندروسیت نشان دادند. همچنین نتایج پیوند به مدل آزمایشگاهی نشان داد سلول های بنیادی مزانشیمی برداشت شده از مغز استخوان و گوش که در داربست کلاژنی قرار داده شده بودند، ۴ هفته پس از پیوند به شکل موثری منجر به ترمیم ضایعه غضروفی شدند.نتایج این پژوهش نشان داد، گرچه اثر ترمیمی سلولهای مزانشیمی برداشت شده از گوش مشابه مغز استخوان است، اما با توجه به سهولت برداشت و سرعت بالای تکثیر گزینه مناسبتری برای ترمیم بالینی ضایعات غضروفی هستند.
#ایرانی -
#اخبار_جدید
:beginner: چینیها به جای سلولهای بنیادی مغز از نمونه ادرار استفاده میکنند.
:pushpin: در فضولات انسانی سلولهای دفع شده زیادی وجود دارند. دانشمندان دریافتهاند که این سلولها میتوانند منبع قدرتمندی از سلولها برای بررسی بیماریها باشند و موجب اجتناب از برخی از مشکلات ناشی از استفاده از سلولهای بنیادی شوند.
:small_blue_diamond: بخشی از فضولاتی که هر روز آنها را با کشیدن سیفون روانه شبکه فاضلاب میکنید، میتوانند منبع قدرتمندی از سلولهای مغزی برای بررسی بیماریها باشند، و شاید حتی یک روز بتوان از آنها در درمان بیماریهای از بین برنده دستگاه عصبی هم استفاده کرد.به گزارش نیچر، دانشمندان به روش نسبتا سادهای دست یافتهاند تا سلولهای دفع شده از طریق دستگاه ادراری را به نورونهای باارزش تبدیل کنند.
:small_orange_diamond: به گفته دانشمندان فایده تهیه سلولها به این شیوه این است که ادرار را میتوان از تقریبا همه بیماران گرفت. -

ویتامین D مانع از رفتن کروناییها به بخش مراقبتهای ویژه میشود !:ok_hand:🏻:white_small_square:محققان اسپانیایی متوجه شدند که دادن ویتامین D به بیماران کرونایی مانع از رفتن آنها به آیسییو میشود. دز داده شده در روز اول ۵۵ میکروگرم و دادن دو دوز ۲۷ میکروگرمی در روزهای سوم و هفتم باعث شد تا وضعیت کروناییها در اسپانیا بهتر شود
- این در حالی است که محدودیت تعریف شده هفتگی روی ۷۰ میکروگرم است اما دادن دز بالا میتواند به بیماران کرونایی کمک کننده باشد
#کرونا
#سلامت -
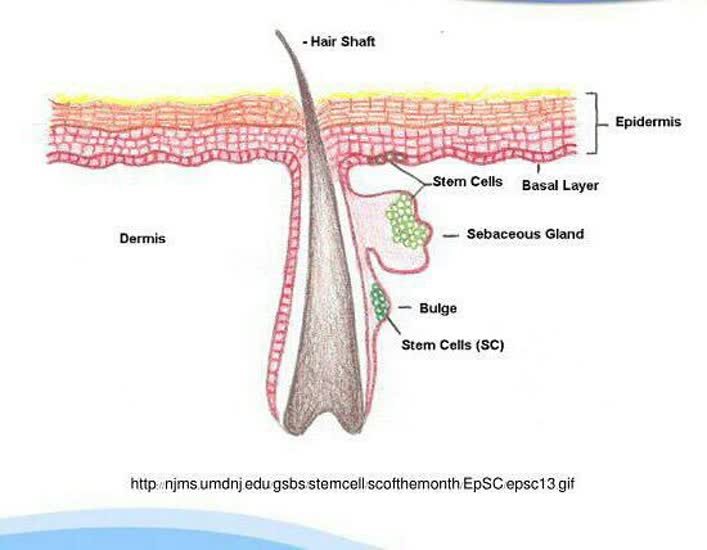
:beginner:نماي شماتيك از محل حضور سلول هاي بنيادي در پوست و ضمائم آن
:small_orange_diamond:سلول های بنیادی اپیدرمال، از جمله سلول های هستند که به دلیلی سهولت دسترسی و جداسازی نسبتا راحت، در حوزه تحقیق، تشخیص و درمان پرکاربرد هستند.
:small_orange_diamond:این سلول ها که به راحتی از یک بیوپسی پوست بدست می آیند، که به دلایل متعددی از جمله توان تکثیر بالا و پتانسیل پایین برای تومورزائی و اختلالات اپی ژنتیکی پرکاربرد است و برخلاف مشکلات اخلاقی کاربرد سلول های پرتوان القائی و سلول های بنیادی مشتق از جنین، استفاده از آنها منع اخلاقی ندارد.
دانش-آموزان-آلاء -
:beginner: روشی جدید برای مطالعه روند تکوین ریه ها
:small_orange_diamond:محققان در مطالعه ای نشان داده اند که چگونه الگوی منشعب اندامی مانند ریه طی تکوین بوجود می آید. در ریه وجود ساختار منشعب با ایجاد یک افزایش نسبت سطح به حجم، سطح تبادلات گازی با جریان خون را افزایش می دهد.
:small_orange_diamond:محققان در مطالعه ای نشان داده اند که چگونه الگوی منشعب اندامی مانند ریه طی تکوین بوجود می آید. در ریه وجود ساختار منشعب با ایجاد یک افزایش نسبت سطح به حجم، سطح تبادلات گازی با جریان خون را افزایش می دهد. برای شناسایی دلیل این فرایند، محققان روی نیروهایی فوکوس کردند که موجب می شوند کلامپ های سلولی موجود در جنین با الگویی درخت مانند در ریه نوزاد رشد کنند.
:small_orange_diamond:آن ها دریافته اند که سیگنال های فیزیکی مشتق از سلول های عضلانی صاف، سلول های پوشاننده مجاری هوایی در حال تکوین را برای جدا شدن و تولید دو انشعاب جدید القا می کنند. آن ها نشان داده اند که سلول های عضلات صاف، رشد اولیه ترین انشعابات مجاری هوایی را شکل می دهند، این فرایند زمانی اتفاق می افتد که جوانه ریوی شروع به رشد به درون شاخه اصلی مجرای هوایی می کند. در جنین در حال تکوین، سلول های عضلات صاف یک پوشش شش وجهی که پیرامون ریه در حال رشد را فرا گرفته است را شکل می دهند، منقبض می شوند و سلول های اپی تلیالی را برای تشکیل چین های اندام بالغ فشرده می سازند.
:globe_with_meridians: Reference:https://medicalxpress.com/news/2020-04-nature-reveals-lung.html
-

🔰استراتا گرافت، جایگزین پوستی تولید شده توسط کشت شبیه سازی شده ی ارگان از سلول های کراتینوسیت انسانی است که بصورت یک لایه سلول اپیدرمال انسانی هوادهی شده است که شبیه به لایه شاخی پوست است.🔸این محصول به لحاظ مرفولوژی، بیان مارکرهای تمایزی، غشای پایه، عملکرد حفاظتی در مقابل نفوذ باکتری ها و بیان مارکرهای ایمنولوژیکی بر روی آن بسیار شبیه پوست انسان است و این مسله باعث اهمیت و امکان رقابت این محصول با سایر محصولات قدیمی تر موجود در بازار شده است.
.
🔸استراتاگرافت، در کلینیکال ترایال های نوع 1 و 2 بعنوان یک پوشش موقت برای بیماران با سوختگی کمتر از 5 درصد از سطح بدن بررسی شد. در این مطالعه، واکنش های سیستم ایمنی نیز در یک مطالعه مقایسه ای و تصادفی مورد بررسی قرار گرفت. -

🔸ویژگی های ایمنولوژیکی این جایگزین های پوستی بیولوژیک قبل و بعد از استفاده در بیماران مبتلا به زخم مورد بررسی قرار گرفته است. بیماران حساس شده به حضور سلول های کشت داده شده از سل لاین کراتینوست های انسانی، قبل و بعد از پیوند با استراتاگرفت از طریق توانائی این سلول ها در القای تکثیر لنفوسیت ها، آمادگی و توانمندی القای لیز به واسطه سلول های کشنده طبیعی بیمار و میزان ایجاد واکنش های اختصاصی بر علیه آنتی بادی های موجود بر روی سلول های مذکور مورد بررسی قرار گرفتند. همچنین مطالعات تکمیلی هیستولوژیکی در بستر زخم ها پس از گذشت یک هفته انجام شد.
🔸نتایج این مطالعات نشان داد که این جایگزین پوستی واکنش های ایمنولوژیک و التهابی را در بیماران بخصوص بیمارانی که درصد زیادی از پوست بدنشان را از دست داده اند و مورد پیوند قرار گرفتنه اند را فعال نمیکند. نتایج کارآزمائی های بالینی فاز دو نشان دهنده ی امنیت و کارائی پوست ایجاد شده پس از پیوند در مدت زمان طولانی تر بود.🛑❌نهایتا این محصول در 18 جولای 2017 تحت حمایت قانون درمان قرن 21 آمریکا که اجازه ورود سریعتر محصولات حوزه پزشکی بازساختی به بازار تحت شرایط کنترل شده را می دهد، مجوز سازمان غذا و داروی آمریکا را دریافت کرد.
-
مهندسی بافت عروق خونی(1)::small_orange_diamond:در اوایل دهه 1950،پیشگامان این حوزه، پروتز هایی عروقی از موادی مانند ابریشم، نایلون و پلی اتیلن ترفتالات PET ( با نام تجاری داکرون) ساختند.
:small_orange_diamond:در طول سال های بعد از مواد سنتزی مانند پلی تترافلوئورو اتیلن بسط داده شده ePTFE جهت جایگذاری شریان های بزرگ استفاده شد اما این مواد در ترمیم عروق با قطر کوچک یعنی عروقی با قطر کمتر از 6 میلی متر موفق نبودند.
:small_orange_diamond:عدم موفقیت پیوند عروق با قطر کوچکتر به علت تشکیل لخته یا هایپرپلازی سلول های لایه اینتیمای رگ در مناطق آناستوموز یا محل انشعاب عروق است و این پدیده به علت عدم انطباق پیوند و شریان طبیعی و یا آسیب به دیواره شریان ایجاد میشود.
-
مهندسی بافت عروق خونی(2):
:small_orange_diamond:عدم موفقیت پروتز های عروقی به دلیل ناتوانی آنها در انتقال فشار های دینامیک عروق، عدم توانایی در واکنش به انقباض عروق و انطباق با جریان خون نیز ممکن است رخ دهد.
:small_orange_diamond:به علاوه، پروتز های عروقی توانایی ترمیم، بازسازی و رشد را ندارند و در نتیجه قابلیت کاربرد آنها برای بیماران کم سن و سال دارای نقص های مادرزادی خاص با محدودیت مواجه است.
:small_orange_diamond:با توجه به نقص های پیوند های عروقی، محققان به روش های مهندسی بافت جهت طراحی عروق خونی روی آوردند.