اسید و باز
-
سلام بچه ها
سوال اولم تا همینجاشو راهنماییم کنین که ph رو چطور به دست آوردین.منظورم محاسبات ریاضیشه برای من با کتاب فرق داره ولی جواب یکسانه.حس میکنم من شانسی به جواب درست رسیدم
دانش-آموزان-آلاء
-
سلام بچه ها
سوال اولم تا همینجاشو راهنماییم کنین که ph رو چطور به دست آوردین.منظورم محاسبات ریاضیشه برای من با کتاب فرق داره ولی جواب یکسانه.حس میکنم من شانسی به جواب درست رسیدم
دانش-آموزان-آلاء
banoo
من اینطوری حل کردم
-
banoo
من اینطوری حل کردم
m.jafari9877
من متوجه شدم اما میشه برام راه سوالو توضیح بدین؟کاملا ریاضیه و ساده است ولی من الان یه تیکه از حواسم پریده. الان عکسشو میفرستم -
m.jafari9877
من متوجه شدم اما میشه برام راه سوالو توضیح بدین؟کاملا ریاضیه و ساده است ولی من الان یه تیکه از حواسم پریده. الان عکسشو میفرستمده به توان منفی ph میشه همون غلطت یون هیدرونیوم
ده به توان منفی poh هم میشه همون غلطت یون هیدروکسیدخب نسبت این دوتارو بهمون داده 10 به توان 10.4
تقسیم میکنیم به هم
بعد ما هر کسری رو معکوس کنیم توان هاشون توی یه منفی ضرب میشن دیگه
منم همین کارو کردم
برعکس کردم توان هارو قرینه کردم
بعد ده به توان poh تقسیم بر ده به توان ph کنیم، میشه پایه رو نوشت، توان بالایی رو منهای پایینی کرد
میشه ده به توان poh منهای ph که دیگه همش کلا ریاضه از عکسی که دادم معلومه بقیش -
ده به توان منفی ph میشه همون غلطت یون هیدرونیوم
ده به توان منفی poh هم میشه همون غلطت یون هیدروکسیدخب نسبت این دوتارو بهمون داده 10 به توان 10.4
تقسیم میکنیم به هم
بعد ما هر کسری رو معکوس کنیم توان هاشون توی یه منفی ضرب میشن دیگه
منم همین کارو کردم
برعکس کردم توان هارو قرینه کردم
بعد ده به توان poh تقسیم بر ده به توان ph کنیم، میشه پایه رو نوشت، توان بالایی رو منهای پایینی کرد
میشه ده به توان poh منهای ph که دیگه همش کلا ریاضه از عکسی که دادم معلومه بقیشm.jafari9877 در اسید و باز گفته است:
ده به توان منفی ph میشه همون غلطت یون هیدرونیوم
ده به توان منفی poh هم میشه همون غلطت یون هیدروکسیدخب نسبت این دوتارو بهمون داده 10 به توان 10.4
تقسیم میکنیم به هم
بعد ما هر کسری رو معکوس کنیم توان هاشون توی یه منفی ضرب میشن دیگه
منم همین کارو کردم
برعکس کردم توان هارو قرینه کردم
بعد ده به توان poh تقسیم بر ده به توان ph کنیم، میشه پایه رو نوشت، توان بالایی رو منهای پایینی کرد
میشه ده به توان poh منهای ph که دیگه همش کلا ریاضه از عکسی که دادم معلومه بقیشراه شما رو متوجه شدم
ببخشین که اینقدر نوشتین
من مشکلم با راه کتابه که چطور از توان 2 همچین استفاده ای کرده
اینو میشه بگین؟ -

نظر خودمو با مداد زیرش نوشتم
حس میکنم یه سوتی ریزی دادم :|
خلاصه این چیزی از ارزشام کم نمیکنهbanoo
:)))))
روش جدید برای حل تست ابداع کردین =)) -
m.jafari9877 در اسید و باز گفته است:
ده به توان منفی ph میشه همون غلطت یون هیدرونیوم
ده به توان منفی poh هم میشه همون غلطت یون هیدروکسیدخب نسبت این دوتارو بهمون داده 10 به توان 10.4
تقسیم میکنیم به هم
بعد ما هر کسری رو معکوس کنیم توان هاشون توی یه منفی ضرب میشن دیگه
منم همین کارو کردم
برعکس کردم توان هارو قرینه کردم
بعد ده به توان poh تقسیم بر ده به توان ph کنیم، میشه پایه رو نوشت، توان بالایی رو منهای پایینی کرد
میشه ده به توان poh منهای ph که دیگه همش کلا ریاضه از عکسی که دادم معلومه بقیشراه شما رو متوجه شدم
ببخشین که اینقدر نوشتین
من مشکلم با راه کتابه که چطور از توان 2 همچین استفاده ای کرده
اینو میشه بگین؟banoo توان دو نیست کههه
فهمیدم که چیو نفهمیدینننببینید اون این کارو کرده بذارید با عکس بگم...
-
banoo
:)))))
روش جدید برای حل تست ابداع کردین =)) -
banoo توان دو نیست کههه
فهمیدم که چیو نفهمیدینننببینید اون این کارو کرده بذارید با عکس بگم...
m.jafari9877 در اسید و باز گفته است:
banoo توان دو نیست کههه
فهمیدم که چیو نفهمیدینننببینید اون این کارو کرده بذارید با عکس بگم...
مرسییی
میدونم سوتی دادم ولی باید میپرسیدم
الان روحم آروم میگیره -
m.jafari9877 در اسید و باز گفته است:
banoo توان دو نیست کههه
فهمیدم که چیو نفهمیدینننببینید اون این کارو کرده بذارید با عکس بگم...
مرسییی
میدونم سوتی دادم ولی باید میپرسیدم
الان روحم آروم میگیره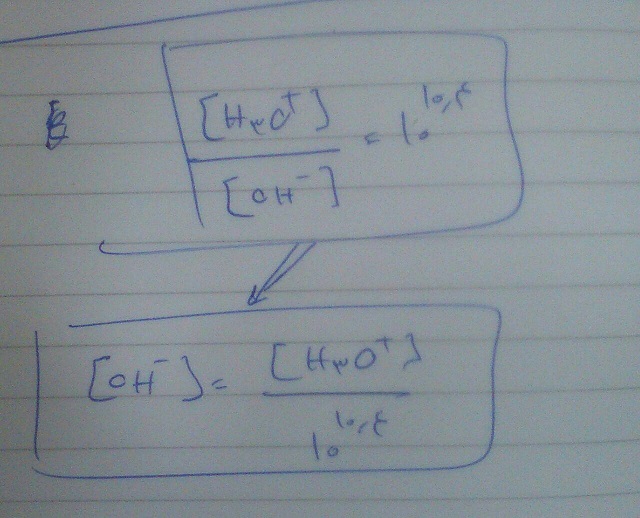
از نسبت استفاده کرده
بعد کلن به جای غلطت هیدروکسید (همون oh) همونی که نتیجه گرفتم رو گذاشته
بعد دیگه یه مجهول میمونه که اونم غلطت هیدرونیوم هست و به دست میاد -

ببخشین کیفیت بده
من جواب مد نظر خودمو تو گزینه ها پیدا نکردم
طبق جدول کتاب درسی ص 67 قدرت اسید HCL بیشتر از H2SO4 و HF هم که کلا اسید ضعیفه
پس باید مقایسه ی pH اینا بشه pH HF > pH H2SO4>pH HCL
ولی همچین چیزی تو گزینه ها نیست
کجای کارم اشتباهه؟
دانش-آموزان-آلاء -

ببخشین کیفیت بده
من جواب مد نظر خودمو تو گزینه ها پیدا نکردم
طبق جدول کتاب درسی ص 67 قدرت اسید HCL بیشتر از H2SO4 و HF هم که کلا اسید ضعیفه
پس باید مقایسه ی pH اینا بشه pH HF > pH H2SO4>pH HCL
ولی همچین چیزی تو گزینه ها نیست
کجای کارم اشتباهه؟
دانش-آموزان-آلاءدلیل این ابهام به خاطر داشتن دو تا هیدروژن اسیدی هست
ببینید ما طبق تعریف داریم :ده به توان منفی ph با mna برابره
خب n برای سولفوریک اسید 2 هست اما برای هیدروکلریک اسید 1 هست
من اگه باشم گزینه ی 3 رو انتخاب میکنم -
دلیل این ابهام به خاطر داشتن دو تا هیدروژن اسیدی هست
ببینید ما طبق تعریف داریم :ده به توان منفی ph با mna برابره
خب n برای سولفوریک اسید 2 هست اما برای هیدروکلریک اسید 1 هست
من اگه باشم گزینه ی 3 رو انتخاب میکنمm.jafari9877 در اسید و باز گفته است:
دلیل این ابهام به خاطر داشتن دو تا هیدروژن اسیدی هست
ببینید ما طبق تعریف داریم :ده به توان منفی ph با mna برابره
خب n برای سولفوریک اسید 2 هست اما برای هیدروکلریک اسید 1 هست
من اگه باشم گزینه ی 3 رو انتخاب میکنمگزینه ی3 جوابه طبیعتا
حرفتونم قبول دارم.این با اون جدول تناقض نداره درسته؟
جدول طبق K مرتب شده
اما اینجوری حس میکنم یه چیزو اشتباه یاد گرفتم.من فکر میکنم قدرت اسیدی با pH نسبت عکس داره اما گویا باید تصحیش کنم وبگم غلظت یون هیدرونیوم با pH نسبت عکس داره -
m.jafari9877 در اسید و باز گفته است:
دلیل این ابهام به خاطر داشتن دو تا هیدروژن اسیدی هست
ببینید ما طبق تعریف داریم :ده به توان منفی ph با mna برابره
خب n برای سولفوریک اسید 2 هست اما برای هیدروکلریک اسید 1 هست
من اگه باشم گزینه ی 3 رو انتخاب میکنمگزینه ی3 جوابه طبیعتا
حرفتونم قبول دارم.این با اون جدول تناقض نداره درسته؟
جدول طبق K مرتب شده
اما اینجوری حس میکنم یه چیزو اشتباه یاد گرفتم.من فکر میکنم قدرت اسیدی با pH نسبت عکس داره اما گویا باید تصحیش کنم وبگم غلظت یون هیدرونیوم با pH نسبت عکس دارهbanoo آفرین دقیقا همینطوره
اصلا اینو یادتون باشه:ph کمتر -> غلظت هیدرونیوم بیشتر
poh کمتر -> غلظت هیدروکسید بیشتر -
banoo آفرین دقیقا همینطوره
اصلا اینو یادتون باشه:ph کمتر -> غلظت هیدرونیوم بیشتر
poh کمتر -> غلظت هیدروکسید بیشترm.jafari9877 در اسید و باز گفته است:
banoo آفرین دقیقا همینطوره
اصلا اینو یادتون باشه:ph کمتر -> غلظت هیدرونیوم بیشتر
poh کمتر -> غلظت هیدروکسید بیشترالان اگه توی این سوال جای سولفوریک اسید فسفریک اسید بود چی میشد؟
فسفریک اسید اسید ضعیفه منتهی 3 مرحله یونش داره چی میشد اینطوری؟ -
سلام بچه ها
سوال اولم تا همینجاشو راهنماییم کنین که ph رو چطور به دست آوردین.منظورم محاسبات ریاضیشه برای من با کتاب فرق داره ولی جواب یکسانه.حس میکنم من شانسی به جواب درست رسیدم
دانش-آموزان-آلاء
-
m.jafari9877 در اسید و باز گفته است:
banoo آفرین دقیقا همینطوره
اصلا اینو یادتون باشه:ph کمتر -> غلظت هیدرونیوم بیشتر
poh کمتر -> غلظت هیدروکسید بیشترالان اگه توی این سوال جای سولفوریک اسید فسفریک اسید بود چی میشد؟
فسفریک اسید اسید ضعیفه منتهی 3 مرحله یونش داره چی میشد اینطوری؟banoo
نه دیگه فسفریک اسید خیلییی ضعیفه
فاصله ی سولفوریک اسید و هیدروکلریک اسید فقط یه خونه است و برای ka هردوتاشون هم نوشته خیلی بزرگ
ولی فسفریک اسید خییییلی ضعیفه
ده به توان منفی 3 داره اصلا -
banoo
نه دیگه فسفریک اسید خیلییی ضعیفه
فاصله ی سولفوریک اسید و هیدروکلریک اسید فقط یه خونه است و برای ka هردوتاشون هم نوشته خیلی بزرگ
ولی فسفریک اسید خییییلی ضعیفه
ده به توان منفی 3 داره اصلاm.jafari9877 در اسید و باز گفته است:
banoo
نه دیگه فسفریک اسید خیلییی ضعیفه
فاصله ی سولفوریک اسید و هیدروکلریک اسید فقط یه خونه است و برای ka هردوتاشون هم نوشته خیلی بزرگ
ولی فسفریک اسید خییییلی ضعیفه
ده به توان منفی 3 داره اصلاپس اینطوری شد که اگه خیلی به هم نزدیک بودن و همچین وضعی بود هیدروژن اسیدی توی غلظت لحاظ میشه و توی pH هم تاثیر میزاره.
حله
مرسییییی



