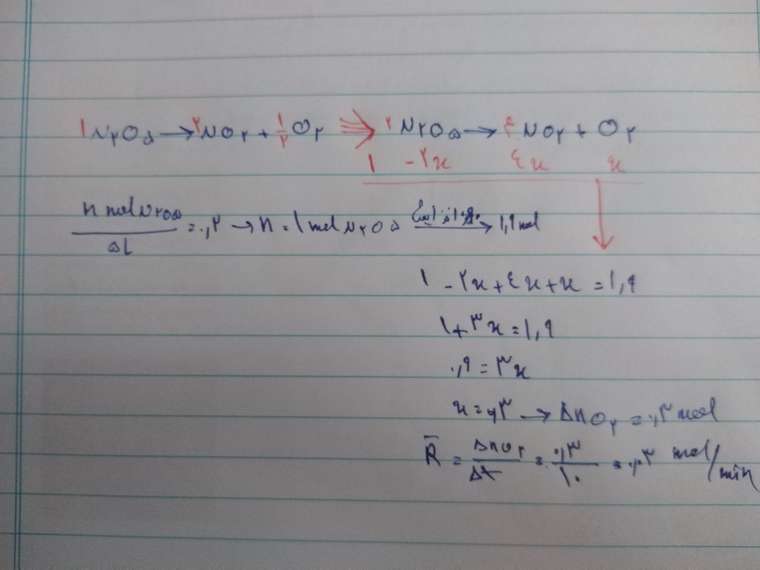سوال شیمی > مبحث>سینتیک
-
سلام. این سوال رو یکی میشه با راه حل برام حل کنه؟
"غلظت اولیه N2O5 در یک ظرف پنج لیتری برابر 0.2 مولار است. با فرض این که در مدت 10 دقیقه شمار مول های موجود در ظرف به اندازه 90 درصد افزایش یابد ، سرعت متوسط واکنش موازنه نشده ی : O2 + NO2 <--- N2O5 برحسب مول بر دقیقه کدام است؟" -
سلام. این سوال رو یکی میشه با راه حل برام حل کنه؟
"غلظت اولیه N2O5 در یک ظرف پنج لیتری برابر 0.2 مولار است. با فرض این که در مدت 10 دقیقه شمار مول های موجود در ظرف به اندازه 90 درصد افزایش یابد ، سرعت متوسط واکنش موازنه نشده ی : O2 + NO2 <--- N2O5 برحسب مول بر دقیقه کدام است؟" -

درسته? -
هر دو درسته. من با تناسب حل میکنم 0.06 در میارم. چرا غلطه؟ روش اینه :
میگم با توجه به ضرایب استوکیومتری 2 مول واکنش دهنده داریم که میشن 5 مول فراورده. یعنی 3 مول افزایش داریم. که میشه 150 درصد افزایش. تناسب میبندم در نهایت میشه 1.2 مول. که اگر بر ده و ضریب استوکیومتری تقسیم کنم میشه 0.06. -
هر دو درسته. من با تناسب حل میکنم 0.06 در میارم. چرا غلطه؟ روش اینه :
میگم با توجه به ضرایب استوکیومتری 2 مول واکنش دهنده داریم که میشن 5 مول فراورده. یعنی 3 مول افزایش داریم. که میشه 150 درصد افزایش. تناسب میبندم در نهایت میشه 1.2 مول. که اگر بر ده و ضریب استوکیومتری تقسیم کنم میشه 0.06.@Danter-group یه مول واکنش دهنده داریم
-
@Danter-group یه مول واکنش دهنده داریم
-
@Danter-group
ربطی به ضریبش نداره، غلظتش 0.2 هست که با توجه به حجم ظرف میشه 1 مول -
@Danter-group
ربطی به ضریبش نداره، غلظتش 0.2 هست که با توجه به حجم ظرف میشه 1 مول -
@Danter-group ضریبای واکنش دهنده ها نشوندهنده مقدار مصرفیشون و ضریب فراورده ها هم نشوندهنده مقدار تولیدیشون هست
البته تو واکنشای تعادلی فرق داره -
@Danter-group ضریبای واکنش دهنده ها نشوندهنده مقدار مصرفیشون و ضریب فراورده ها هم نشوندهنده مقدار تولیدیشون هست
البته تو واکنشای تعادلی فرق داره -
@Amir-Bernousi خب دیگه منم با توجه به همین تناسب بستم. با توجه به ضریبا 3 مول افزایش داریم که تقسیم بر 2 مول فراورده اولیه میشه 150 درصد که اگر با 90 در صد مقایسه کنیم میشه 1.2 مول فراورده.
@Danter-group 3
کلا 1 مول واکنش دهنده داریم، 90 درصد هم زیاد بشه میشه 1.9 مول نه بیشتر
ملاک مقدار واکنش دهندس -
@Amir-Bernousi خب دیگه منم با توجه به همین تناسب بستم. با توجه به ضریبا 3 مول افزایش داریم که تقسیم بر 2 مول فراورده اولیه میشه 150 درصد که اگر با 90 در صد مقایسه کنیم میشه 1.2 مول فراورده.
-
@Danter-group 3
کلا 1 مول واکنش دهنده داریم، 90 درصد هم زیاد بشه میشه 1.9 مول نه بیشتر
ملاک مقدار واکنش دهندس