سلول های بنیادی راهی به آینده
-
:red_circle: سلول های بنیادی #چندتوان (multipotent stem cells)(1)
:small_red_triangle_down:سلول های بنیادی چندتوان سلول هایی هستند که علاوه بر قابلیت خودنوزایی (یعنی تولید یک سلول بنیادی دیگر مثل خود)، می توانند بسته به شرایط محیطی، چند نوع یا چندین نوع سلول تمایزیافته (یعنی غیربنیادی) مختلف را تولید کنند.
:eight_spoked_asterisk: به عنوان مثال، سلول های بنیادی خونساز (hematopoietic stem cells) از جمله سلول های بنیادی چندتوان هستند چون علاوه بر خود، می توانند چند نوع سلول تمایزیافته متفاوت را بسازند. برخی از سلول های تمایزیافته که توسط سلول های بنیادی خونساز تولید می شوند، عبارتند از:
:small_red_triangle:گلبول های قرمز خون (که مسئول حمل اکسیژن به بافت ها هستند)
:small_red_triangle:انواع گلبول های سفید خون (که مسئول مبارزه با میکروب ها هستند) شامل:
— نوتروفیل ها
— ائوزینوفیل ها
— بازوفیل ها
— منوسیت ها
— لنفوسیت های T و B
— و غیره
:small_red_triangle:پلاکت ها (که به تشکیل لخته خون و انعقاد خون در هنگام بریدگی یا پارگی رگ خونی کمک می کنند)
:small_red_triangle:و برخی دیگر از سلول های بافت خون -
🔴 سلول های بنیادی #چندتوان (multipotent stem cells)(2)
:eight_spoked_asterisk: مغز استخوان شامل سلولهای بنیادی سوماتیکی است که میتوانند به انواع سلولهای موجود در خون مانند گلبولهای سفید، قرمز و پلاکتها تبدیل شوند. این سلولها برای دوباره تولید کردن سلولهای خونی ضروری هستند.
:eight_spoked_asterisk: همچنین سلول های بنیادی عصبی که در یکی از مطالب پیشین معرفی شدند، از جمله سلول های بنیادی چندتوان هستند، چرا که علاوه بر تکثیر نامحدود خود، قادرند نورون ها، الیگودندروسیت ها و آستروسیت ها را ایجاد کنند.
-
🔴 سلول های بنیادی #چندتوان (multipotent stem cells)(3)
:white_check_mark: نکته مهم: سلول های بنیادی چندتوان اگر چه ممکن است انواع متعددی از سلول های مختلف را تولید کنند، اما با این وجود «پرتوان» خوانده نمی شوند، چون انواع سلول های مختلفی که توسط سلول های بنیادی چندتوان تولید می شوند، همگی در یک دودمان سلولی جای می گیرند. مثلا سلول های بنیادی خونساز فقط سلول های موجود در خون را تولید می کنند، نه سلول های استخوانی و غیره را. سلول های بنیادی پرتوان را در ادامه معرفی خواهیم کرد.
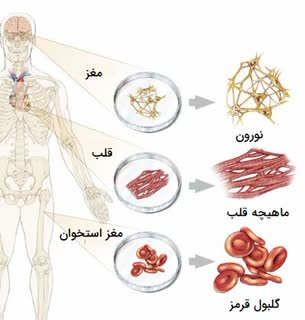
:pushpin: مثالهایی از تمایز سلولهای #چندتوان
-

:pushpin:تاثیر استرس بر #سلولهای_بنیادی بدن ما
:low_brightness: سلول های بنیادی با دو ویژگی «بقا و #تکثیر طولانی مدت» و «توانایی #تمایز» شناخته می شوند. مشخص شده است که برخی از شرایط، تاثیرات مخربی بر سلول های بنیادی دارند.
:low_brightness: گروهی از محققان، تاثیر استرس اکسایشی را بر «زنده مانی»، «طول تلومر» و «تکثیر» سلول های بنیادی #مزانشیمی که از جمله سلول های بنیادی بسیار مهم در بدن ما هستند، ارزیابی کردند. آن ها مشاهده کردند که استرس، پیرشدن سلول های بنیادی مزانشیمی را تسریع می کند و قدرت تکثیر آن ها را کاهش می دهد، ضمن این که باعث کاهش طول تلومر می شود. #تلومر، به بخش انتهایی کروموزوم ها می گویند که نقش مهمی در سلامت ما و سلولهایمان دارد.
:link: مقاله مربوطه :point_down:
:globe_with_meridians: http://www.sciencedirect.com/science/article/pii/S0014482711000784:loudspeaker: در نتیجه، استرس احتمالا به سایر سلول های بنیادی ما هم آسیب وارد میکند.
-
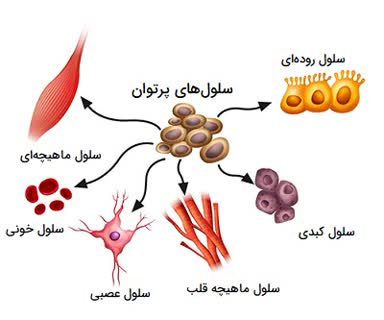
:red_circle: سلولهای بنیادی #پرتوان (pluripotent stem cells)(1)
:small_orange_diamond: سلول های بنیادی پرتوان سلول هایی هستند که علاوه بر قابلیت خودنوزایی (یعنی تولید یک سلول بنیادی دیگر مثل خود)، می توانند همه انواع سلول تمایزیافته بدن را تولید کنند. در واقع، در سختگیرانه ترین تعریف، سلول های بنیادی پرتوان باید بتوانند تحت شرایط خاص و مناسب، یک موجود کامل مثل انسان را بسازند یعنی همه 200 نوع سلول موجود در بدن انسان چه بنیادی و چه غیربنیادی. پس سلول های بنیادی پرتوان باید بتوانند نه تنها همه انواع سلول های خونی، بلکه همه انواع سلول های دستگاه عصبی، همه انواع سلول های دستگاه ماهیچه ای و قلبی و همه انواع سلول های پوستی و دستگاه گوارش و غیره را بسازند.
-
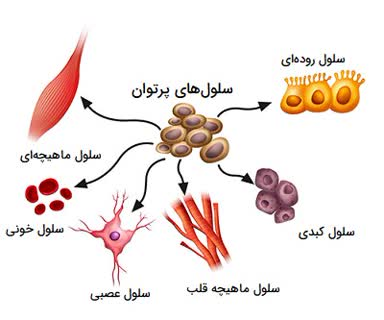
:red_circle: سلولهای بنیادی #پرتوان (pluripotent stem cells)(2)
:eight_spoked_asterisk: به عنوان مثال، سلول های بنیادی جنینی (embryonic stem cells) که از جنین های مرحله بلاستوسیست (یعنی جنینی که به اندازه یک «نقطه روی کاغذ» است و هنوز در رحم مادر مستقر نشده است) تهیه می شوند، از جمله سلول های بنیادی پرتوان هستند چون علاوه بر خود، قادرند تمام انواع سلولهای تمایزیافته بدن را بسازند.
:small_blue_diamond: سلول های بنیادی پرتوان، بخاطر این که قادرند به طور نامحدود در آزمایشگاه زنده بمانند و تکثیر شوند و همچنین از این جهت که می توانند همه انواع سلول های دیگر را بسازند، کاربردهای زیست-پزشکی بسیاری دارند.
-
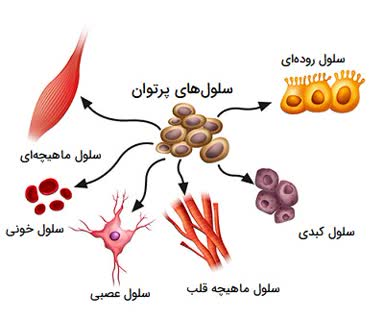
🔴 سلولهای بنیادی #پرتوان (pluripotent stem cells)(3)
:small_orange_diamond: در آزمایشگاه، این سلولها تحت شرایطی کشت داده میشوند که قابلیت تمایز در آنها به طور موقت مهار شود و بتوانند به صورت نامحدود تکثیر پیدا کنند. سلولهای بنیادی پرتوان، پروتئین ای-کادهرین را به مقدار زیادی تولید میکنند که باعث میشود سلولها به هم بچسبند و مجموعههای سلولی موسوم به #کلونی را همانند آنچه که در شکل میبینید، ایجاد کنند.
در بسیاری از سلولهای دیگر، وقتی سلولها در اثر تقسیم پی در پی به یکدیگر میرسند، پیامی به درون آنها مخابره میشود تا دست از تقسیم شدن بردارند. اما در سلولهای بنیادی پرتوان، سازوکاری وجود دارد که به سلولها اجازه میدهد در عین اتصال به یکدیگر برای طولانی مدت به تکثیر خود ادامه دهند. -
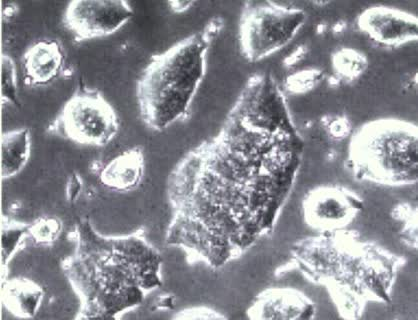
:beginner: سلولهای بنیادی جنینی موشی، نوعی از سلولهای بنیادی #پرتوان هستند:bangbang:
:pushpin:منبع عکس: مقاله دکتر مرادی و همکاران
Moradi et al, Small-RNA sequencing reveals Dlk1-Dio3 locus-embedded microRNAs as major drivers of ground state pluripotency, 2017, Stem Cell Reports -
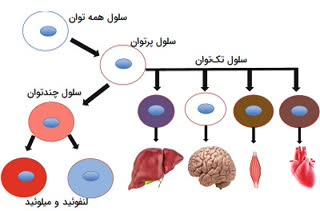
:red_circle: سلول های بنیادی #همهتوان (totipotent stem cells)(1)
:small_orange_diamond: سلول های بنیادی همهتوان سلولهایی هستند که علاوه بر قابلیت خودنوزایی (یعنی تولید یک سلول بنیادی دیگر مثل خود)، می توانند نه تنها تمام سلول های تمایزیافته موجود در بدن را بسازند (یعنی نه تنها پرتوان هستند و می توانند یک بدن کامل را به تنهایی ایجاد کنند)، بلکه قادرند سلول های تشکیل دهنده پرده های خارج جنینی از جمله آمنیون (که جنین را در برمی گیرد)، کیسه زرده (که در مقطعی از زندگی جنین، خون سازی انجام می دهد) و جفت (رابط غذایی مادر و جنین) را تولید کنند.
-
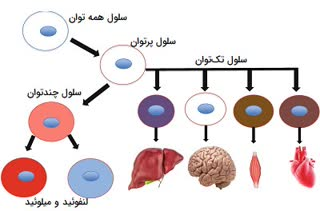
🔴 سلول های بنیادی #همهتوان (totipotent stem cells)(2)
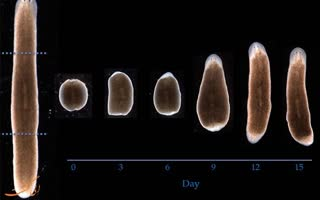
:eight_spoked_asterisk: یک نوع کرم پهن به نام #پلاناریا وجود دارد که اگر آن را دهها بلکه صدها قطعه بکنید، هر قطعه اش قادر است یک کرم پهن کامل و سالم را ایجاد کند و این بخاطر حضور سلول های بنیادی خاصی در بافت های مختلف بدن این کرم است که همه توان هستند.
:small_orange_diamond: در انسان، فقط خود سلول تخم و همچنین سلول های جنین سه چهار روزه انسان (حداکثر تا مرحله «مورولا»)، همه توان هستند، یعنی نه تنها جنین، بلکه بافت های خارج جنینی نظیر جفت را نیز می توانند ایجاد کنند. اما پس از این مرحله، فقط سلول های پرتوان (pluripotent) در جنین دیده می شوند. سلول های پرتوان را قبلا تعریف کردیم.
-
https://www.aparat.com/v/tmTc1
تشکیل کولونی سلول های بنیادی -

:eight_spoked_asterisk: درمان ضایعات نخاعی با الهام از گکوها
:small_blue_diamond:گکوها مانند بسیاری از مارمولکها توانایی این را دارند تا برای فرار از شکارچیها دم خود را جدا کرده و مجددا با کمک ستون فقرات آن را ایجاد کنند. این موجودات این کار را سریعتر از هر مارمولک و در ظرف 30 روز انجام میدهند. در حال حاضر یک گروه از محققان از دانشگاه کانادایی "گولف" با الهام از این روش قصد دارند تا این کار را در انسانها تکرار کنند.
یافتههای این محققان میتواند به بهبود صدمات نخاعی در انسانها منجر شود. -
🔰 تلاش محققان برای ساخت خون به کمک سلول های بنیادی
🔸در مطالعه ای مروری محققین تلاش های اخیر در زمینه تولید سلول های بنیادی خون ساز با پتانسیل پیوند طولانی مدت از سلول های بنیادی پرتوان را مرور کرده اند و این سلول های بنیادی را سنگ بنای مهمی در جهت تولید سلول های خونی دانسته اند. هم چنین در این مطالعه محققین دو خانواده مهم از فاکتورهای رونویسی را در خون سازی و تمایز به سمت سلول های خونی مهم شمرده اند که شامل پروتئین های Homeobox(HOX) و GATA است. به نظر می رسد که این پروتئین ها تنظیم کننده های کلیدی مسیر خون سازی باشند و با کنترل زمانی و مکانی دقیق بیان آن ها بتوان سلول های بنیادی خون ساز دارای عملکردی را تولید کرد که قابلیت پیوند طولانی مدت را داشته باشند.Reference:http://www.eurekaselect.com/node/175820/article/hematopoietic-differentiatio
-

:white_check_mark: روش های مختلف انتقال و #پیوند #سلول_های_بنیادی به بدن بیمار
:round_pushpin:برخی از انواع سلول های بنیادی مانند «سلول های بنیادی خون ساز» مدتها است که به بدن بیماران نیازمند پیوند می شوند، اما برخی دیگر هنوز در مراحل تحقیقاتیِ آزمایشگاهی و حیوانی هشتند.
:round_pushpin:برای انتقال و پیوند سلول های بنیادی به درون بدن بیمار مورد نظر، چند مسیر وجود دارد که مهمترین مسیرهای انتقال سلول های بنیادی عبارتند از:
:hotsprings: تزریق موضعی در داخل بافت موردنظر: مزیتش این است که فقط بافت مورد نظر، پیوند سلول بنیادی را دریافت می کند!
:hotsprings: تزریق سیستمیک و عمومی به داخل خون: مزیتش راحت تر بودن آن است و نیز این که بسیاری از سلول ها که داخل خون تزریق می شوند، می توانند از خون خارج شده و به بافت موردنظر وارد شوند و اگر به بافت های دیگری وارد شوند، معمولا زنده نمی مانند.
:hotsprings: انتقال از راه خرناس کشیدن (بینی): در لینک زیر می توانید خبر مربوط به این راه انتقال جدید راببینید که احتمالا برای انتقال سلول های عصبی مناسب باشد!
http://www.bonyannews.ir/News/ID/20574 -

:red_circle: فرق سلول های #سرطانی با #سلولهای_بنیادی :beginner:
✍ سلول های سرطانی دارای تکثیر سریع و افسارگسیخته بوده و حاوی آسیب های ژنتیکی نسبتا زیادی در DNA خود هستند، این در حالی است که سلول های بنیادی اگرچه ممکن است تکثیر سریع داشته باشند، اما تکثیر آن ها تحت کنترل بدن است و معمولا آسیب ژنتیکی شاخصی نشان نمی دهند.
✍ سلول های سرطانی برخلاف سلول های بنیادی، کمتر به دستورات تنظیمی بدن پاسخ می دهند و بی ملاحظه بارها و بارها تکثیر شده و توده های سرطانی ایجاد می کنند که بخاطر ایجاد مزاحمت فیزیکی و فقر مواد مغذی برای بافت های سالم بدن، باعث نارسایی اندام های مجاور در بدن می شود.
✍ سرعت تکثیر سلول های سرطانی معمولا از اغلب سلول های بنیادی بیشتر است.
-
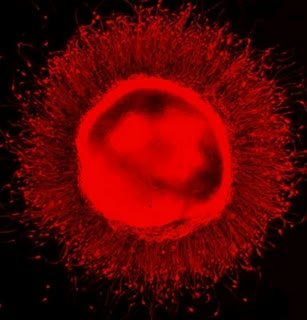
#تصاویر_میکروسکوپی
#سلولهای_بنیادی_عصبی:closed_book: این عکس از یک نوروسفر است که در واقع یک توپ متمرکز از سلولهای بنیادی عصبی است که به صورت معلق در محیط مایع رشد می کنند. هنگامی که نوروسفرها را روی یک ظرف پتری قرار می دهیم، سلولهای بنیادی عصبی به صفحه چسبیده و شروع به مهاجرت می کنند و این الگوی آفتابگردان زیبا را ایجاد می کنند.
:green_book: سلولهای بنیادی عصبی سرانجام به سلولهای مغزی موسوم به نورونها، آستروسیتها و الیگودندروسیتها تکامل می یابند.
-
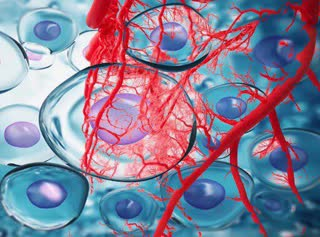
#اخبار_جدید_سلولهای_بنیادی
:beginner:ساخت پوست دارای عروق:beginner::small_blue_diamond: پوستهایی که در حال حاضر در دسترس قرار دارند، بیشتر شبیه به چسب زخم هستند. اگرچه این پوستها میتوانند به ترمیم بهتر زخم کمک کنند اما نهایتا اتصال آنها به بدن از بین میرود و هرگز با سلولهای میزبان ادغام نمیشوند. یکی از موانع به کار گرفتن این پوستها، عدم قابلیت آن ها برای ایجاد رگزایی های جدید است.
:small_orange_diamond: محققان، سالها به بررسی این موضوع پرداختهاند. آنها در پژوهش پیشین خود نشان دادند که میتوان دو نوع سلول انسانی را به جوهر زیستی اضافه کرده و سپس آنها را به صورت ساختارهای مشابه پوست پرینت کرد. این محققان در پروژه جدید خود نشان دادند که اگر عناصر اصلی از جمله سلولهای اندوتلیالی را با کلاژن حیوانی و سلولهای ساختاری دیگر ادغام کنند، سلولها طی چند هفته، تعامل بیولوژیکی را با سیستم عروقی آغاز میکنند. هنگامی که پژوهشگران، این پوست جدید را برای مدل های موشی استفاده کردند. رگهای خونی آن توانستند ارتباط و تعامل را با رگهای بدن موش برقرار کنند. این اتفاق بسیار مهمی در زمینه مهندسی بافت پوست محسوب می شود زیرا همانگونه که میدانیم، انتقال خون و مواد مغذی به عضو پیوند زده شده میتواند آن را زنده نگه دارند.
:globe_with_meridians:Reference:https://www.eurekalert.org/pub_releases/2019-11/rpi-lsc110119.php
-
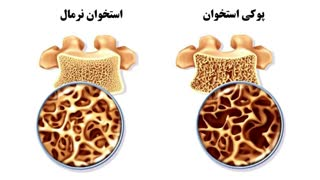
:beginner: آیا #سلول_درمانی می تواند در پوکی استخوان موثر باشد؟:beginner:
:small_blue_diamond: بیش از 200 میلیون نفر در سراسر دنیا مبتلا به استئوپروز یا #پوکی_استخوان هستند. این بیماری استخوانهای بدن را ضعیف کرده و موجب شکستگی آنها میشود.
:small_orange_diamond: درمانهای فعلی، تنها پیشرفت بیماری را کند میکنند و درمان کاملی برای آن وجود ندارد.
:small_blue_diamond: به تازگی محققان دانشگاه تورنتو کانادا از #سلولهای_بنیادی مزانشیمی برای درمان پوکی استخوان استفاده کردهاند. در بررسیهای این دانشگاه، تزریق سلولهای بنیادی توانسته به میزان قابل توجهی، قدرت استخوانها را بازگرداند.
:small_orange_diamond: اخیرا محققان پژوهشگاه رویان نیز یک مطالعه بالینی در زمینه تاثیر سلولهای بنیادی در درمان پوکی استخوان انجام دادهاند.